परमाणु कक्षकों का संकरण। आणविक कक्षा की विधि की अवधारणा। बाइनरी होमोन्यूक्लियर अणुओं के लिए आणविक कक्षा के गठन के ऊर्जा आरेख। जब एक रासायनिक बंधन बनता है, तो परस्पर क्रिया करने वाले परमाणुओं के गुण बदल जाते हैं, मुख्य रूप से उनकी बाहरी कक्षाओं की ऊर्जा और व्यवसाय।
सामाजिक नेटवर्क पर काम साझा करें
यदि यह कार्य आपको शोभा नहीं देता है, तो पृष्ठ के नीचे समान कार्यों की एक सूची है। आप खोज बटन का भी उपयोग कर सकते हैं
पेज 13
लेबेदेव यू.ए. व्याख्यान 0 2
व्याख्यान #0 2
रसायनिक बंध। रासायनिक बंधन के लक्षण: ऊर्जा, लंबाई, बंधन कोण। रासायनिक बंधन के प्रकार। संचार ध्रुवीयता। सहसंयोजक बंधन की प्रकृति के बारे में क्वांटम-यांत्रिक विचार। वैलेंस बॉन्ड की विधि की अवधारणा। परमाणु कक्षकों का संकरण।- (सी यिग्मा) और  (पीआई) -बॉन्ड। अणुओं का ज्यामितीय विन्यास। किसी अणु के द्विध्रुव का विद्युत आघूर्ण। आणविक कक्षा की विधि की अवधारणा। बाइनरी होमोन्यूक्लियर अणुओं के लिए आणविक कक्षा के गठन के ऊर्जा आरेख। सिग्मा (
(पीआई) -बॉन्ड। अणुओं का ज्यामितीय विन्यास। किसी अणु के द्विध्रुव का विद्युत आघूर्ण। आणविक कक्षा की विधि की अवधारणा। बाइनरी होमोन्यूक्लियर अणुओं के लिए आणविक कक्षा के गठन के ऊर्जा आरेख। सिग्मा ( ) और पाई (
) और पाई (  ) -आणविक कक्षाएँ। दीया- और पैरामैग्नेटिक अणु।
) -आणविक कक्षाएँ। दीया- और पैरामैग्नेटिक अणु।
अनुस्मारक
श्रोडिंगर समीकरण। - तरंग क्रिया।
ई \u003d एफ (एन, एल, एम, एस)।
रसायनिक बंध। रासायनिक बंधन के लक्षण: ऊर्जा, लंबाई, बंधन कोण।
हमने पृथक परमाणुओं के इलेक्ट्रॉनिक स्तरों की संरचना पर विचार किया है। व्यवहार में ये बहुत दुर्लभ वस्तुएं हैं। एकमात्र अपवाद अक्रिय गैस आर्गन है जिसका इलेक्ट्रॉनिक सूत्र 1 . हैएस 2 2 एस 2 2 पी 6 3 एस 2 3 पी 6 . और यद्यपि यह वातावरण में "केवल" 0.93% वॉल्यूम है, आप में से प्रत्येक सचमुच एक सांस में लगभग तीन सौ क्विंटल आर्गन परमाणुओं को "निगल" लेता है।
अन्य सभी पदार्थ और सामग्री जिनके साथ हम व्यवहार करते हैं उनमें शामिल हैंरासायनिक रूप से बाध्यपरमाणु। एक दूसरे के साथ मुक्त परमाणुओं की बातचीत से अणुओं, आयनों और क्रिस्टल का निर्माण होता है। ये "शास्त्रीय" रासायनिक वस्तुएं हैं। हाल ही में, हालांकि, नैनोस्ट्रक्चर, सतह यौगिकों, बर्थोलाइड्स और कई अन्य व्यावहारिक रूप से महत्वपूर्ण "गैर-शास्त्रीय" रासायनिक वस्तुओं जैसी वस्तुओं ने एक महत्वपूर्ण भूमिका हासिल कर ली है।
रासायनिक बंधन परमाणुओं के बाहरी इलेक्ट्रॉन कोशों में इलेक्ट्रॉनों की परस्पर क्रिया के कारण होता है।वे कक्षक जो रासायनिक बंध के निर्माण में भाग लेते हैं, कहलाते हैंसंयोजकता कक्षक तथा उन पर स्थित इलेक्ट्रॉन संयोजकता इलेक्ट्रॉन होते हैं।
जब एक रासायनिक बंधन बनता है, तो परस्पर क्रिया करने वाले परमाणुओं के गुण बदल जाते हैं और सबसे बढ़कर, उनकी बाहरी कक्षाओं की ऊर्जा और अधिभोग।
जब एक रासायनिक बंधन बनता है, तो वैलेंस ऑर्बिटल्स में इलेक्ट्रॉनों की कुल ऊर्जा मुक्त परमाणुओं में उनकी ऊर्जा से कम होती है। ऊर्जा में इस अंतर को रासायनिक बंधन ऊर्जा कहा जाता है।
एक विशिष्ट रासायनिक बंधन ऊर्जा सैकड़ों kJ/mol है।
रासायनिक बंधन की एक महत्वपूर्ण मात्रात्मक विशेषता इसकी लंबाई है।बंधन की लंबाई अणु की स्थिर अवस्था में रासायनिक रूप से बंधे परमाणुओं के नाभिक के बीच की दूरी है।
एक रासायनिक बंधन की विशिष्ट लंबाई नैनोमीटर का दसवां हिस्सा होता है। 1
यदि दो या दो से अधिक अन्य परमाणु किसी दिए गए परमाणु के साथ परस्पर क्रिया करते समय अणु के निर्माण में भाग लेते हैं, तो इसकी ज्यामितीय संरचना या रासायनिक संरचना के बारे में प्रश्न उठता है। ए.एम. बटलरोव द्वारा अणुओं की रासायनिक संरचना के सिद्धांत की नींव रखी गई थी 2
जटिल अणुओं की संरचना की सबसे महत्वपूर्ण मात्रात्मक विशेषताओं में से एक हैबंधन कोण - एक परमाणु से निकलने वाले रासायनिक बंधों की दो दिशाओं से बनने वाला कोण।
रासायनिक बंधन के प्रकार। संचार ध्रुवीयता।
संयोजकता इलेक्ट्रॉनों की परस्पर क्रिया की प्रकृति और अन्योन्यक्रिया के दौरान बनने वाले कक्षकों के प्रकार के अनुसार,रासायनिक बंधन निम्नलिखित मुख्य प्रकारों में विभाजित हैं:सहसंयोजक (ध्रुवीय और गैर-ध्रुवीय), आयनिक, दाता-स्वीकर्ता, हाइड्रोजन और अंतर-आणविक (जिसे वैन डेर वाल्स भी कहा जाता है)।
1916 में वापस, अमेरिकी रसायनज्ञ जी.एन. लुईस 3 इस विचार को व्यक्त किया कि एक इलेक्ट्रॉन जोड़ी द्वारा एक रासायनिक बंधन बनता है, जिसे ग्राफिक रूप से एक वैलेंस लाइन द्वारा दर्शाया जाता है:
एफ + एफ = एफ 2 (एफ-एफ)।
यदि परमाणुओं की वैद्युतीयऋणात्मकता समान होती है, तो ऐसे बंधन को गैर-ध्रुवीय कहा जाता है। अगर अलग - ध्रुवीय।
जब एक ध्रुवीय सहसंयोजक बंधन बनता है, तो परमाणु एक अतिरिक्त चार्ज प्राप्त करते हैं - उच्च इलेक्ट्रोनगेटिविटी वाले परमाणु के लिए नकारात्मक और कम इलेक्ट्रोनगेटिविटी वाले परमाणु के लिए सकारात्मक:
एच + सीएल = एचसीएल ( 
 )
)
मामले में जब परस्पर क्रिया करने वाले परमाणुओं की वैद्युतीयऋणात्मकता में अंतर बड़ा होता है, तो बंधनआयनिक माना जाता है:
ना + सीएल \u003d NaCl (ना + सीएल -)।
यदि बंधन बनाने वाला इलेक्ट्रॉन जोड़ी बातचीत से पहले परमाणुओं में से एक का था, तो ऐसे बंधन को दाता-स्वीकर्ता बंधन कहा जाता है। एक परमाणु जिसने एक इलेक्ट्रॉन जोड़ी प्रदान की है उसे दाता कहा जाता है, और एक परमाणु जिसने इसे एक मुक्त कक्षीय में स्वीकार कर लिया है उसे स्वीकर्ता कहा जाता है।
दाता-स्वीकर्ता बांड की उपस्थिति विशेष रूप से विशेषता है।डी - मुक्त या आंशिक रूप से भरी हुई धातुडी -ऑर्बिटल्स जटिल यौगिक बनाते हैं।
हम अन्य प्रकार के संचार के बारे में बाद में बात करेंगे।
सहसंयोजक बंधन की प्रकृति के बारे में क्वांटम-यांत्रिक विचार।
आधुनिक दृष्टिकोण से, सभी परस्पर क्रिया करने वाले परमाणुओं के सभी इलेक्ट्रॉनों के क्वांटम यांत्रिक संपर्क के दौरान एक सहसंयोजक बंधन उत्पन्न होता है। लेकिन, जैसा कि हमने व्याख्यान संख्या 1 में कहा था, अणुओं में कई इलेक्ट्रॉनों की कक्षाओं का वर्णन करने वाले श्रोडिंगर समीकरण का कोई सटीक समाधान नहीं है। एक रासायनिक बंधन के क्वांटम-मैकेनिकल विवरण का कार्य इस तथ्य से सुगम होता है कि इसके गठन के दौरान आंतरिक और बाहरी इलेक्ट्रॉन गोले पर स्थित इलेक्ट्रॉनों की भूमिका काफी भिन्न होती है।
इसलिए, रासायनिक बंधन का वर्णन करने के लिए विभिन्न अनुमानित तरीकों को बनाना संभव था।
क्वांटम रसायन विज्ञान में लागू कार्यक्रमों का एक समृद्ध शस्त्रागार है जो अणुओं और आयनों की एक विस्तृत श्रेणी के लिए उच्च सटीकता के साथ गणना करना संभव बनाता है। 4
हालांकि, अभी भी कोई सार्वभौमिक और पर्याप्त सटीक क्वांटम-रासायनिक एल्गोरिदम नहीं है।
रासायनिक यौगिकों की संरचना की गुणात्मक समझ के लिए दो विधियों का उपयोग किया जाता है -संयोजकता बांड विधि (एमवीएस)और आणविक कक्षीय विधि (MO)।
वैलेंस बॉन्ड की विधि की अवधारणा। अणुओं का ज्यामितीय विन्यास। किसी अणु के द्विध्रुव का विद्युत आघूर्ण।
संयोजकता बंधों की विधि की मुख्य अभिधारणाएँ हैं:
1. एक एकल सहसंयोजक रासायनिक बंधन दो वैलेंस इलेक्ट्रॉनों द्वारा किया जाता है जो दो कक्षाओं पर कब्जा कर लेते हैं - प्रत्येक परस्पर क्रिया करने वाले परमाणुओं में से एक। इस मामले में, वैलेंस जोड़ी बनाने वाले इलेक्ट्रॉनों के स्पिन विपरीत होना चाहिए (बंधन विरोधी समानांतर स्पिन वाले इलेक्ट्रॉनों द्वारा बनाया गया है)।
2. प्रारंभिक परमाणु कक्षक (AO) अणु की संरचना में भी अपना आकार बनाए रखते हैं।
3. ऑर्बिटल्स के ओवरलैप के कारण बॉन्ड बनता है, जिससे इंटरेक्टिंग परमाणुओं के नाभिक के बीच इलेक्ट्रॉन घनत्व में उस दिशा में वृद्धि होती है जो अधिकतम ओवरलैप प्रदान करती है।
जलवाष्प अणु में MHS द्वारा रासायनिक बंध के निर्माण पर विचार करें -एच2ओ.
एक अणु एक ऑक्सीजन परमाणु से बना होता हैहे और दो हाइड्रोजन परमाणुएच . ऑक्सीजन परमाणु का इलेक्ट्रॉनिक सूत्र 1एस 2 2 एस 2 2 पी 4 . बाहरी ऊर्जा स्तर में 6 इलेक्ट्रॉन होते हैं। सबलेवल 2एस भरा हुआ है। सबलेवल 2 . परपी में से एक पर पी -ऑर्बिटल्स (मान लें)पीयू ,) एक इलेक्ट्रॉन युग्म है, और अन्य दो पर (पी एक्स और पी जेड ) - एक अयुग्मित इलेक्ट्रॉन। यह वे हैं जो एक रासायनिक बंधन के निर्माण में भाग लेंगे।

हाइड्रोजन परमाणु का इलेक्ट्रॉनिक सूत्र 1एस 1 . हाइड्रोजन में एकएस -इलेक्ट्रॉन जिसकी कक्षीय रूपरेखा एक गोला है, और यह ओवरलैप में भाग लेगापी - ऑक्सीजन कक्षीय, एक रासायनिक बंधन बनाता है। कुल ऐसाएसपी पानी के अणु में दो ओवरलैप होंगे। और अणु की संरचना इस तरह दिखेगी:

जैसा कि चित्र से देखा जा सकता है, पानी के अणु में कुल्हाड़ियों के साथ निर्देशित दो सहसंयोजक रासायनिक बंधन होते हैंजेड और एक्स . इसलिए, इस मॉडल में आबंध कोण 90 . हैके विषय में . प्रयोग से पता चलता है कि यह कोण 104.5 . हैओ
बिना किसी गणना के सरलतम गुणात्मक मॉडल के लिए काफी अच्छा मेल!
ऑक्सीजन की मुल्लिकेन वैद्युतीयऋणात्मकता 3.5 है, और हाइड्रोजन की 2.1 है। इसलिए, प्रत्येक बंधन ध्रुवीय होगा, और चार्ज - ऑक्सीजन पर होगा, और
- ऑक्सीजन पर होगा, और + - हाइड्रोजन पर, अर्थात्। विद्युत आवेश के तीन केंद्र बनते हैं। अणु में दो विद्युत द्विध्रुव बनते हैं।
+ - हाइड्रोजन पर, अर्थात्। विद्युत आवेश के तीन केंद्र बनते हैं। अणु में दो विद्युत द्विध्रुव बनते हैं।
एक द्विध्रुवीय दो समान आवेश होते हैं जो एक परिमित दूरी से अलग होते हैं।मैं एक दूसरे से। एक द्विध्रुवीय एक द्विध्रुवीय क्षण की विशेषता है
 =
=

द्विध्रुव एक सदिश है जो ऋणात्मक ध्रुव से धनात्मक ध्रुव की ओर निर्देशित होता है। जल के एक अणु में दो द्विध्रुव आघूर्ण आबंध बनते हैं, जो मिलाने पर अणु का कुल द्विध्रुव आघूर्ण देते हैं। एमवीएस मॉडल के अनुसार पानी के अणु के द्विध्रुवीय क्षणों की योजना का रूप है:

इस बात पर जोर देना महत्वपूर्ण है कि बंधन द्विध्रुवीय क्षण वेक्टर रूप से जुड़ते हैं और कुल द्विध्रुवीय क्षण अणु की ज्यामिति पर निर्भर करता है। जैसा कि आप देख सकते हैं, इस मामले में, इस तथ्य के कारण कि बांड एक दूसरे से समकोण पर निर्देशित होते हैं, अणु समग्र रूप से ध्रुवीय हो जाता है। और प्रयोग इसकी पुष्टि करता है - पानी के अणु का द्विध्रुवीय क्षण 1.84 डेबी है। (1 डेबी बराबर 0.33*10-29 सी * एम)
अणुओं में बंधों की ज्यामितीय संरचना बहुत विविध हो सकती है। बांड विमान और अंतरिक्ष दोनों में स्थित हो सकते हैं, विभिन्न विन्यासों (त्रिकोणीय, टेट्रागोनल, हेक्सागोनल पिरामिड, द्विपिरामिड, पिरामिड से बने छल्ले, आदि) के त्रि-आयामी निकायों के रूप में अणु बनाते हैं।
पाठ्यपुस्तक में रासायनिक बंधों की संरचना और अणुओं की ज्यामिति के बीच संबंध के बारे में और पढ़ें पृष्ठ 119-128)।
 - (सी यिग्मा) और
- (सी यिग्मा) और  (पीआई) -बॉन्ड।
(पीआई) -बॉन्ड।
आइए बंधों के निर्माण में कक्षकों के अतिव्यापन पर लौटते हैं। हमारे उदाहरण मेंअधिकतम ओवरलैप का क्षेत्रएस और पी ऑर्बिटल्स परमाणुओं के केन्द्रों को जोड़ने वाली रेखा पर स्थित है। इस प्रकार के आवरण को कहते हैं -सम्बन्ध।
-सम्बन्ध।
एक अन्य मामले पर विचार करें - ऑक्सीजन अणु O2 . जैसा कि हमने देखा, ऑक्सीजन परमाणु में दो होते हैंपी ऐसे ऑर्बिटल्स जिनमें इलेक्ट्रॉन होते हैं जो एक रासायनिक बंधन बना सकते हैं। ऑक्सीजन का प्रसिद्ध संरचनात्मक सूत्रओ = ओ . ऑक्सीजन अणु में दोहरा बंधन होता है। उनमें से एक वह है जिस पर अभी चर्चा की गई है। -कनेक्शन। और दूसरा? यह पता चला है कि दूसरा बंधन एक अन्य प्रकार के कक्षीय ओवरलैप के कारण बनता है, जिसे कहा जाता है
-कनेक्शन। और दूसरा? यह पता चला है कि दूसरा बंधन एक अन्य प्रकार के कक्षीय ओवरलैप के कारण बनता है, जिसे कहा जाता है -संचार।
-संचार।
इसकी अवधारणा  और
और  एफ. हंड द्वारा दिए गए कनेक्शन।
एफ. हंड द्वारा दिए गए कनेक्शन।
शिक्षा पर  -ऑर्बिटल्स के बंधन इस तरह से ओवरलैप होते हैं कि दो अतिव्यापी क्षेत्र बनते हैं, और वे उस समतल के संबंध में सममित रूप से स्थित होते हैं जिस पर परस्पर क्रिया करने वाले परमाणुओं के नाभिक स्थित होते हैं।
-ऑर्बिटल्स के बंधन इस तरह से ओवरलैप होते हैं कि दो अतिव्यापी क्षेत्र बनते हैं, और वे उस समतल के संबंध में सममित रूप से स्थित होते हैं जिस पर परस्पर क्रिया करने वाले परमाणुओं के नाभिक स्थित होते हैं।
ज्यामितीय रूप से यह इस तरह दिखता है:

कृपया ध्यान दें कि -कनेक्शन छोटे भागों से बनता हैपी -ऑर्बिटल्स, जिसमें "इलेक्ट्रॉन क्लाउड" का घनत्व अधिक होता है, और इसलिए यह बंधन अधिक मजबूत होता है
-कनेक्शन छोटे भागों से बनता हैपी -ऑर्बिटल्स, जिसमें "इलेक्ट्रॉन क्लाउड" का घनत्व अधिक होता है, और इसलिए यह बंधन अधिक मजबूत होता है -सम्बन्ध। वास्तव में, प्रयोग से पता चलता है कि कार्बन यौगिकों में, ईथेन C 2 एच 6 (सीएच 3 - सीएच 3 - एक
-सम्बन्ध। वास्तव में, प्रयोग से पता चलता है कि कार्बन यौगिकों में, ईथेन C 2 एच 6 (सीएच 3 - सीएच 3 - एक  -बॉन्ड), एथिलीन सी 2 एच 4 (सीएच 2 \u003d सीएच 2 - एक
-बॉन्ड), एथिलीन सी 2 एच 4 (सीएच 2 \u003d सीएच 2 - एक  - संचार और एक
- संचार और एक  -बॉन्ड) और एसिटिलीन सी 2 एच 2 (सी एनएस एच - एक
-बॉन्ड) और एसिटिलीन सी 2 एच 2 (सी एनएस एच - एक  - कनेक्शन और दो
- कनेक्शन और दो  -बॉन्ड) उनकी टूटना ऊर्जा क्रमशः 247, 419 और 515 kJ/mol है।
-बॉन्ड) उनकी टूटना ऊर्जा क्रमशः 247, 419 और 515 kJ/mol है।
अब हम एमवीएस अभिधारणाओं की सूची को पूरा कर सकते हैं:
4.
यदि अणु में कई (डबल और ट्रिपल) बॉन्ड बनते हैं, तो उनमें से एक होगा - संचार, और अन्य -
- संचार, और अन्य - -सम्बन्ध)।
-सम्बन्ध)।
ध्यान दें कि कनेक्शन मेंडी- और एफ -धातु, अन्य प्रकार के बंधों का निर्माण संभव है - -बॉन्ड, जब चार स्थानिक क्षेत्रों में ओवरलैप होता है और समरूपता का तल परमाणुओं के नाभिक को जोड़ने वाली रेखा के लंबवत होता है।
-बॉन्ड, जब चार स्थानिक क्षेत्रों में ओवरलैप होता है और समरूपता का तल परमाणुओं के नाभिक को जोड़ने वाली रेखा के लंबवत होता है।
परमाणु कक्षकों का संकरण।
जब रासायनिक बंधन बनते हैं, तो एक महत्वपूर्ण घटना हो सकती है, जिसे कहा जाता हैकक्षीय संकरण।
बेरिलियम परमाणु पर विचार करेंहोना . इसका इलेक्ट्रॉनिक सूत्र 1 . हैएस 2 2 एस 2 . इस तथ्य को देखते हुए कि बेरिलियम के सभी इलेक्ट्रॉनों को जोड़ा जाता है, ऐसे परमाणु को रासायनिक रूप से निष्क्रिय गैसों की तरह व्यवहार करना चाहिए - रासायनिक बातचीत में प्रवेश नहीं करना चाहिए।
हालांकि, आइए बेरिलियम परमाणु के इलेक्ट्रॉन विवर्तन आरेख को ध्यान से देखें:

यह आरेख से देखा जा सकता है कि बेरिलियम परमाणु में भरे हुए 2 . के अतिरिक्त हैएस -3 और मुक्त कक्षक 2पी -ऑर्बिटल्स! सच है, इन कक्षकों की ऊर्जा 2 . की ऊर्जा से अधिक हैएस -ऑर्बिटल्स प्रति परिमाण इ . लेकिन यह ऊर्जा रासायनिक बंधन के निर्माण के दौरान निकलने वाली ऊर्जा से छोटी और कम होती है। इसलिए, परमाणु एक ऊर्जावान रूप से अनुकूल अंतिम स्थिति प्राप्त करने के लिए बातचीत के दौरान अपने ऑर्बिटल्स को पुनर्व्यवस्थित करता है। ऐसी पुनर्व्यवस्था के लिए, किसी दिए गए परमाणु के साथ परस्पर क्रिया करने वाले कणों की गतिज ऊर्जा का उपयोग किया जाता है। रासायनिक गतिकी के प्रश्नों पर चर्चा करते समय हम इस ऊर्जा स्रोत के बारे में अधिक विस्तार से बात करेंगे। 5
इ . लेकिन यह ऊर्जा रासायनिक बंधन के निर्माण के दौरान निकलने वाली ऊर्जा से छोटी और कम होती है। इसलिए, परमाणु एक ऊर्जावान रूप से अनुकूल अंतिम स्थिति प्राप्त करने के लिए बातचीत के दौरान अपने ऑर्बिटल्स को पुनर्व्यवस्थित करता है। ऐसी पुनर्व्यवस्था के लिए, किसी दिए गए परमाणु के साथ परस्पर क्रिया करने वाले कणों की गतिज ऊर्जा का उपयोग किया जाता है। रासायनिक गतिकी के प्रश्नों पर चर्चा करते समय हम इस ऊर्जा स्रोत के बारे में अधिक विस्तार से बात करेंगे। 5
इस पुनर्व्यवस्था को कक्षकों का संकरण कहा जाता है, क्योंकि इस प्रक्रिया के दौरान कक्षकों के "दो प्रकार" से एक नया उत्पन्न होता है।
तरंग कार्यों की भाषा में, इसका वर्णन मूल तरंग कार्यों के परिणामस्वरूप ऑर्बिटल्स के हाइब्रिड तरंग फ़ंक्शन से संबंधित समीकरण द्वारा किया जाता है।
गठित संकर कक्षकों की संख्या संकरण प्रक्रिया में भाग लेने वाले कक्षकों की संख्या के बराबर है।
ग्राफिक रूप से, इस प्रक्रिया को निम्नलिखित आरेख द्वारा दर्शाया जा सकता है:

ध्यान दें कि संकरण के लिए आवश्यक ऊर्जाई हाइब्रिड संकरण कक्षकों के बीच ऊर्जा अंतर से कमइ।
हाइब्रिड ऑर्बिटल्स के पदनाम में, मूल ऑर्बिटल्स के पदनाम बनाए रखे जाते हैं। तो, इस मामले में (परमाणुहोना ), एक को संकरित करेंएस और एक पी -ऑर्बिटल, और दोनों हाइब्रिड ऑर्बिटल्स को के रूप में दर्शाया गया हैएसपी -कक्षीय। केवल दो कक्षकों के संकरण की आवश्यकता इस तथ्य के कारण है कि बेरिलियम परमाणु के बाहरी ऊर्जा स्तर में केवल दो इलेक्ट्रॉन होते हैं।
अन्य मामलों में, जब कई समान ऑर्बिटल्स संकरण में भाग लेते हैं, तो उनकी संख्या को एक घातांक के साथ चिह्नित किया जाता है। उदाहरण के लिए, एक को संकरण करते समयएस और दो पी तीन कक्षक प्राप्त होते हैंसपा 2 -ऑर्बिटल्स, और एक को संकरण करते समयएस और तीन पी -ऑर्बिटल्स - चारएसपी 3 ऑर्बिटल्स।
विचाराधीन मामले में, हंड के नियम के अनुसार, बेरिलियम परमाणु को दो अयुग्मित इलेक्ट्रॉन और दो सहसंयोजक रासायनिक बंधन बनाने की क्षमता प्राप्त होती है।
संकर कक्षकों का गठनएस, पी और यहां तक कि डी -ऑर्बिटल्स आकार में थोड़ा भिन्न होते हैं और इस तरह दिखते हैं ("असममित डम्बल"):

ध्यान दें कि संकर कक्षकों की संख्या उनके निर्माण में शामिल कक्षकों की संख्या के बराबर होती हैसंकरण कक्षकों की संख्या और प्रकार की परवाह किए बिना।
अंतरिक्ष में संकर कक्षकों का स्थान उनकी संख्या से निर्धारित होता है।
विशेष रूप से, बेरिलियम परमाणु में दो संकर होते हैंएसपी कक्षक एक सीधी रेखा के अनुदिश स्थित होते हैं (180 . के कोण पर)हे ), जो समान रूप से आवेशित इलेक्ट्रॉनों की प्रवृत्ति से मेल खाती है जो उन्हें एक दूसरे से जितना संभव हो सके दूर ले जाने के लिए कब्जा कर लेते हैं:

अधिक संयोजकता बांड और संकरण की विधि के बारे में यहां पढ़ा जा सकता है:
http://center.fio.ru/method/resources/Alikberovalyu/2004/stroenie/gl_10.html#104
अणु में अक्सर एक इलेक्ट्रॉन जोड़ी ("अकेला इलेक्ट्रॉन जोड़ी") द्वारा कब्जा कर लिया जाता है। ऐसे ऑर्बिटल्स रासायनिक बंधों के निर्माण में भाग नहीं लेते हैं, लेकिन अणु की ज्यामितीय संरचना को प्रभावित करते हैं।
एमवीएस के संशोधन, ऐसे ऑर्बिटल्स के प्रभाव को ध्यान में रखते हुए, वैलेंस ऑर्बिटल्स (वीईपीआर) के इलेक्ट्रॉन जोड़े के प्रतिकर्षण का सिद्धांत कहा जाता है और आप इसे पाठ्यपुस्तक में पृष्ठ 124 - 128 पर परिचित कर सकते हैं।
आणविक कक्षा की विधि की अवधारणा।
हमने एमवीएस के ढांचे के भीतर एओ संकरण की घटना पर विचार किया है। यह पता चला कि रासायनिक बंधों के गहन मॉडलिंग के लिए संकरण का विचार भी उपयोगी है। यह उनके विवरण की दूसरी विधि का आधार है, जिसे हमारे पाठ्यक्रम में माना जाता है - विधिआण्विक कक्षक(एमओ)।
इस पद्धति का मुख्य अभिधारणा यह दावा है कि परमाणुओं के एओ एक दूसरे के साथ बातचीत करते हुए अपना व्यक्तित्व खो देते हैं और सामान्यीकृत एमओ बनाते हैं, अर्थात। कि अणुओं में इलेक्ट्रॉन किसी विशेष परमाणु से "संबंधित" नहीं होते हैं, लेकिन पूरे आणविक संरचना में यांत्रिक रूप से क्वांटम को स्थानांतरित करते हैं।
एमओ पद्धति की कई किस्में हैं जो बी . को ध्यान में रखती हैंके विषय में अधिक या कम कारक और, तदनुसार, कमोबेश गणितीय रूप से जटिल। सबसे सरल सन्निकटन है जो केवल इलेक्ट्रॉन संपर्क के रैखिक प्रभावों को ध्यान में रखता है। इस सन्निकटन को MO LCAO (परमाणु कक्षकों का रैखिक संयोजन) विधि कहा जाता है।
क्वांटम यांत्रिकी की भाषा में, दो ऑर्बिटल्स की परस्पर क्रिया के सबसे सरल मामले के लिए यह कथन इस प्रकार लिखा गया है:
कहाँ  - एमओ तरंग समारोह,
- एमओ तरंग समारोह, पहले परमाणु के AO का तरंग फलन है,
पहले परमाणु के AO का तरंग फलन है, दूसरे परमाणु के AO का तरंग फलन है,ए और बी MO की समग्र संरचना में दिए गए AO के योगदान को दर्शाने वाले संख्यात्मक गुणांक हैं।
दूसरे परमाणु के AO का तरंग फलन है,ए और बी MO की समग्र संरचना में दिए गए AO के योगदान को दर्शाने वाले संख्यात्मक गुणांक हैं।
चूंकि एक रैखिक बहुपद दाईं ओर लिखा जाता है, इसलिए MO विधि के इस संशोधन को LCAO कहा जाता है।
समीकरण से देखा जा सकता है किजब दो AO परस्पर क्रिया करते हैं, तो दो MO प्राप्त होते हैं. उनमें से एक कहा जाता हैबाध्यकारी एमओ, और दूसरा - एमओ को ढीला करना।
उन्हें ऐसा नाम क्यों मिला, यह चित्र से स्पष्ट है, जो एक अणु में ऑर्बिटल्स के ऊर्जा आरेख को दर्शाता है:

जैसा कि आंकड़े से देखा जा सकता है, बाध्यकारी एमओ में प्रारंभिक एओ की ऊर्जा से कम ऊर्जा होती है, और ढीले एमओ में उच्च ऊर्जा होती है। (क्रमश,)। स्वाभाविक रूप से, न्यूनतम ऊर्जा के सिद्धांत के अनुसार, एक अणु में इलेक्ट्रॉन बंधन बनने पर सबसे पहले बंधन कक्षीय पर कब्जा कर लेंगे।
सामान्य तौर पर, बातचीत करते समय N AO N MO बन जाता है।
सिग्मा (  ) और पाई (
) और पाई (  ) -आणविक कक्षाएँ।
) -आणविक कक्षाएँ।
MO LCAO पद्धति का उपयोग करके मात्रात्मक गणना के परिणामस्वरूप, यह पता चला कि की अवधारणाएँ और
और  MO LCAO विधि में कक्षकों की समरूपता को भी संरक्षित किया जाता है।
MO LCAO विधि में कक्षकों की समरूपता को भी संरक्षित किया जाता है।
यहाँ रूपरेखा कैसी दिखती है -बाइंडिंग (के रूप में चिह्नित)
-बाइंडिंग (के रूप में चिह्नित) या और
या और  एमओ एलसीएओ विधि में -ढीला (या के रूप में निरूपित) ऑर्बिटल्स:
एमओ एलसीएओ विधि में -ढीला (या के रूप में निरूपित) ऑर्बिटल्स:

और यहाँ रूपरेखा कैसी दिखती है - बाध्यकारी (
- बाध्यकारी (  ) और
) और  - ढीला करना (
- ढीला करना (  *
) MO LCAO विधि द्वारा ऑर्बिटल्स:
*
) MO LCAO विधि द्वारा ऑर्बिटल्स:


बाइनरी होमोन्यूक्लियर अणुओं के लिए आणविक कक्षा के गठन के ऊर्जा आरेख।
जटिल अणुओं के लिए आणविक ऑर्बिटल्स की ऊर्जा की गणना करना जिसमें विभिन्न तत्वों (हेट्रोन्यूक्लियर अणु) के नाभिक शामिल हैं, आधुनिक कंप्यूटरों के लिए भी एक जटिल कम्प्यूटेशनल कार्य है। इसलिए, व्यक्तिगत अणुओं की प्रत्येक गणना एक अलग रचनात्मक कार्य है।
फिर भी, यह पता चला कि डी.आई. मेंडेलीव की आवधिक प्रणाली की दूसरी अवधि के तत्वों के द्विआधारी होमोन्यूक्लियर अणुओं के लिए ऊर्जा आरेख सार्वभौमिक है और इसका रूप है:

कभी-कभी साहित्य तत्वों के लिए अलग-अलग चित्र देता हैबी ,सी,एन और बाद मेंओ, एफ, नी हालांकि, अणु के चुंबकीय गुणों का अध्ययनबी2 अल्ट्रालो तापमान पर ऊर्जा आरेखों के रूप को जटिल बनाने की आवश्यकता की स्पष्ट रूप से पुष्टि नहीं करते हैंबी, सी, एन।
दीया- और पैरामैग्नेटिक अणु। एमओ एलसीएओ के अनुसार बांडों की बहुलता।
वीएस विधि की तुलना में एमओ एलसीएओ विधि के गंभीर लाभों में से एक अणुओं के चुंबकीय गुणों का अधिक सही विवरण है और विशेष रूप से, आणविक ऑक्सीजन के पैरामैग्नेटिज्म की व्याख्या। 6
आइए एमएचएस के अनुसार ऑक्सीजन अणु की संरचना को याद करें, जिस पर हमने पहले विचार किया था। इस संरचना के अनुसार सभी संयोजकता इलेक्ट्रॉन और और
और  -एक अणु में बंधन O2 इलेक्ट्रॉन जोड़े बनाते हैं और अणु का कुल चक्रण शून्य होता है।
-एक अणु में बंधन O2 इलेक्ट्रॉन जोड़े बनाते हैं और अणु का कुल चक्रण शून्य होता है।
MO LCAO विधि के अनुसार इस अणु के ऑर्बिटल्स की संरचना, उपरोक्त ऊर्जा आरेख के अनुसार इलेक्ट्रॉनों MO से भरकर प्राप्त की जाती है:

जैसा कि इस आरेख से देखा जा सकता है, ऑक्सीजन अणु में प्रतिबाधा पर दो अयुग्मित इलेक्ट्रॉन होते हैं और
और  कक्षक उनके चुंबकीय क्षण जुड़ते हैं और अणु का कुल चुंबकीय क्षण देते हैं। प्रयोग से पता चलता है कि ऑक्सीजन अणु का चुंबकीय क्षण 2.8 . है
कक्षक उनके चुंबकीय क्षण जुड़ते हैं और अणु का कुल चुंबकीय क्षण देते हैं। प्रयोग से पता चलता है कि ऑक्सीजन अणु का चुंबकीय क्षण 2.8 . है (इलेक्ट्रॉन का आंतरिक चुंबकीय क्षण है 1
(इलेक्ट्रॉन का आंतरिक चुंबकीय क्षण है 1 ) इस बात को ध्यान में रखते हुए कि कुल चुंबकीय क्षण में आंतरिक इलेक्ट्रॉनिक क्षण के अलावा कक्षीय एक भी शामिल है, मात्रात्मक समझौता एमओ विधि की वैधता के पक्ष में बहुत ही स्पष्ट रूप से गवाही देता है।
) इस बात को ध्यान में रखते हुए कि कुल चुंबकीय क्षण में आंतरिक इलेक्ट्रॉनिक क्षण के अलावा कक्षीय एक भी शामिल है, मात्रात्मक समझौता एमओ विधि की वैधता के पक्ष में बहुत ही स्पष्ट रूप से गवाही देता है।
चुंबकीय क्षण की उपस्थिति में पदार्थ बन जाता हैअनुचुंबकीय -यह "चुंबक द्वारा आकर्षित" है। 7 चुंबकीय क्षण की अनुपस्थिति में, पदार्थप्रतिचुंबकीय - यह चुंबकीय क्षेत्र द्वारा "बाहर धकेल दिया" जाता है. 8
चुंबकीय गुणों के अलावा, MO LCAO के ऊर्जा आरेखों के विश्लेषण से यह निर्धारित करना संभव हो जाता हैएक रासायनिक बंधन (सीएस या पीएस) की बहुलता (या क्रम)।
केएस \u003d ½ (एन संबंध - एन रेज़र)
जहां एन जुड़ा हुआ है बॉन्डिंग ऑर्बिटल्स में इलेक्ट्रॉनों की कुल संख्या है;एन रेसो एंटीबॉडी ऑर्बिटल्स में इलेक्ट्रॉनों की कुल संख्या है)।
हमने सहसंयोजक रासायनिक बंधों की अभिव्यक्ति और विवरण के विभिन्न मामलों पर विचार किया है। यह मुख्य प्रकार का रासायनिक बंधन है, क्योंकि अधिकांश रासायनिक तत्वों में इसकी घटना का कारण होता है - वैलेंस इलेक्ट्रॉनों की उपस्थिति।
हालाँकि, परमाणुओं के परस्पर क्रिया के कुछ मामलों में, विशेष परिस्थितियाँ उत्पन्न होती हैं जो विशेष प्रकार के बंधनों को जन्म देती हैं, जिन पर हम अगले व्याख्यान में विचार करेंगे।
जिसमें किसी दिए गए बंधन का एक मोल टूट जाता है। यह माना जाता है कि प्रारंभिक पदार्थ और प्रतिक्रिया उत्पाद 1 एटीएम के दबाव और 25 0 सी के तापमान पर एक काल्पनिक आदर्श गैस के अपने मानक राज्यों में हैं। एक रासायनिक बंधन की ऊर्जा को तोड़ने के लिए समानार्थी हैं: बंधन ऊर्जा, द्विपरमाणुक अणुओं की पृथक्करण ऊर्जा, रासायनिक बंधन निर्माण ऊर्जा।
एक रासायनिक बंधन की तोड़ने वाली ऊर्जा को विभिन्न तरीकों से परिभाषित किया जा सकता है, उदाहरण के लिए
मास स्पेक्ट्रोस्कोपिक डेटा (मास स्पेक्ट्रोमेट्री) से।
विभिन्न यौगिकों में रासायनिक बंधों की टूटने वाली ऊर्जा संदर्भ पुस्तक में परिलक्षित होती है।
रासायनिक बंधों की टूटने वाली ऊर्जा एक रासायनिक बंधन की ताकत की विशेषता है।
| मिश्रण | मिश्रण | बॉन्ड ब्रेकिंग एनर्जी, kcal/mol | |
|---|---|---|---|
| एच-हो | 104,2 | सीएच3-एच | 104 |
| हो-हो | 119 | सीएच 3 सीएच 2-एच | 98 |
| सीएच 3 ओ-एच | 102 | (सीएच 3) 2 सीएच-एच | 94,5 |
| सी 6 एच 5 ओ-एच | 85 | (सीएच 3) 3 सी-एच | 91 |
| एफ एच | 135,8 | सी 6 एच 5-एच | 103 |
| सीएल-एच | 103,0 | सीएच 2 \u003d सीएच-एच | 103 |
| ब्र-हो | 87,5 | एचसी≡सी-एच | 125 |
| मैं-हो | 71,3 | एच 2 एन-एच | 103 |
C-C बंधन को तोड़ने की ऊर्जा।
यह सभी देखें
टिप्पणियाँ
विकिमीडिया फाउंडेशन। 2010.
देखें कि "केमिकल बॉन्ड ब्रेकिंग एनर्जी" अन्य शब्दकोशों में क्या है:
यह उस कार्य के बराबर है जो एक अणु को दो भागों (परमाणु, परमाणुओं के समूह) में विभाजित करने और उन्हें एक दूसरे से अनंत दूरी पर हटाने के लिए खर्च किया जाना चाहिए। उदाहरण के लिए, यदि ई. एक्स माना जाता है। साथ। H3CH H एक मीथेन अणु में, तो ऐसे ... ... महान सोवियत विश्वकोश
एक एक्ज़ोथिर्मिक प्रतिक्रिया गर्मी की रिहाई के साथ एक रासायनिक प्रतिक्रिया है। एक एंडोथर्मिक प्रतिक्रिया के विपरीत। रासायनिक प्रणाली में ऊर्जा की कुल मात्रा को मापना या गणना करना अत्यंत कठिन है... विकिपीडिया
Fig.1. संयोजकता बांड के सिद्धांत के ढांचे में ट्रिपल बांड ट्रिपल बांड एक अणु में तीन आम बाध्यकारी इलेक्ट्रॉन जोड़े के माध्यम से दो परमाणुओं का एक सहसंयोजक बंधन है। ट्रिपल बॉन्ड की दृश्य संरचना की पहली तस्वीर दी गई थी ... विकिपीडिया
अल्कोहल की एक विशिष्ट विशेषता लाल (ऑक्सीजन) और ग्रे (हाइड्रोजन) में हाइलाइट की गई आकृति में एक संतृप्त कार्बन परमाणु पर हाइड्रॉक्सिल समूह है। अल्कोहल (लैटिन से ... विकिपीडिया
सी (कार्बोनियम), तत्वों की आवर्त सारणी के आईवीए उपसमूह (सी, सी, जीई, एसएन, पीबी) का एक गैर-धातु रासायनिक तत्व। यह प्रकृति में हीरे के क्रिस्टल (चित्र 1), ग्रेफाइट या फुलरीन और अन्य रूपों के रूप में होता है और कार्बनिक का हिस्सा है ... ... कोलियर इनसाइक्लोपीडिया
रसायन विज्ञान में बांड ऊर्जा एक महत्वपूर्ण अवधारणा है। यह दो गैस परमाणुओं के बीच एक सहसंयोजक बंधन को तोड़ने के लिए आवश्यक ऊर्जा की मात्रा निर्धारित करता है। यह अवधारणा आयनिक बंधों पर लागू नहीं होती है। जब दो परमाणु मिलकर एक अणु बनाते हैं, तो कोई यह निर्धारित कर सकता है कि उनके बीच का बंधन कितना मजबूत है - यह उस ऊर्जा को खोजने के लिए पर्याप्त है जिसे इस बंधन को तोड़ने के लिए खर्च किया जाना चाहिए। याद रखें कि एक परमाणु में बाध्यकारी ऊर्जा नहीं होती है, यह ऊर्जा अणु में दो परमाणुओं के बीच बंधन की ताकत को दर्शाती है। किसी भी रासायनिक प्रतिक्रिया के लिए बांड ऊर्जा की गणना करने के लिए, बस टूटे हुए बांडों की कुल संख्या निर्धारित करें और इससे बनने वाले बांडों की संख्या घटाएं।
कदम
भाग 1
टूटे और बने बंधों को पहचानें- सिंगल, डबल और ट्रिपल केमिकल बॉन्ड के ब्रेक को एक टूटा हुआ बॉन्ड माना जाता है। हालांकि इन बंधनों में अलग-अलग ऊर्जाएं होती हैं, प्रत्येक मामले में एक बंधन को टूटा हुआ माना जाता है।
- यही बात सिंगल, डबल या ट्रिपल बॉन्ड के निर्माण पर भी लागू होती है। ऐसे प्रत्येक मामले को एक नए कनेक्शन के गठन के रूप में माना जाता है।
- हमारे उदाहरण में, सभी बॉन्ड सिंगल हैं।
-
निर्धारित करें कि समीकरण के बाईं ओर कौन से लिंक टूटे हुए हैं।एक रासायनिक समीकरण के बाईं ओर अभिकारक होते हैं, और यह उन सभी बंधनों का प्रतिनिधित्व करता है जो प्रतिक्रिया के परिणामस्वरूप टूटते हैं। यह एक एंडोथर्मिक प्रक्रिया है, यानी रासायनिक बंधनों को तोड़ने में एक निश्चित मात्रा में ऊर्जा लगती है।
- हमारे उदाहरण के लिए, प्रतिक्रिया समीकरण के बाईं ओर एक एच-एच बंधन और एक बीआर-बीआर बंधन होता है।
-
समीकरण के दाईं ओर बनने वाले बंधों की संख्या गिनें।प्रतिक्रिया उत्पादों को दाईं ओर दिखाया गया है। समीकरण का यह हिस्सा रासायनिक प्रतिक्रिया के परिणामस्वरूप बनने वाले सभी बंधनों का प्रतिनिधित्व करता है। यह एक ऊष्माक्षेपी प्रक्रिया है और यह ऊर्जा छोड़ती है (आमतौर पर ऊष्मा के रूप में)।
- हमारे उदाहरण में, समीकरण के दाईं ओर दो H-Br बांड हैं।
भाग 2
बाध्यकारी ऊर्जा की गणना करें-
आवश्यक बाध्यकारी ऊर्जा खोजें।ऐसी कई तालिकाएँ हैं जो विभिन्न प्रकार के यौगिकों के लिए बाध्यकारी ऊर्जाओं को सूचीबद्ध करती हैं। ऐसी सारणियाँ इंटरनेट पर या रसायन शास्त्र पर एक संदर्भ पुस्तक पर पाई जा सकती हैं। यह याद रखना चाहिए कि गैसीय अवस्था में अणुओं के लिए बाध्यकारी ऊर्जा हमेशा दी जाती है।
-
टूटे हुए बंधों की संख्या से बंध ऊर्जा को गुणा करें।कई प्रतिक्रियाओं में, एक बंधन को कई बार तोड़ा जा सकता है। उदाहरण के लिए, यदि एक अणु में 4 हाइड्रोजन परमाणु होते हैं, तो हाइड्रोजन की बाध्यकारी ऊर्जा को 4 गुना, यानी 4 से गुणा किया जाना चाहिए।
- हमारे उदाहरण में, प्रत्येक अणु में एक बंधन होता है, इसलिए बंधन ऊर्जा को केवल 1 से गुणा किया जाता है।
- एच-एच = 436 x 1 = 436 केजे/मोल
- Br-Br \u003d 193 x 1 \u003d 193 kJ / mol
-
टूटे हुए बंधनों की सारी ऊर्जाओं को जोड़ें।समीकरण के बाईं ओर बंधों की संगत संख्या से बाध्यकारी ऊर्जाओं को गुणा करने के बाद, आपको कुल ज्ञात करना होगा।
- आइए हमारे उदाहरण के लिए टूटे हुए बंधों की कुल ऊर्जा ज्ञात करें: H-H + Br-Br = 436 + 193 = 629 kJ/mol।
बाध्यकारी ऊर्जा की गणना के लिए एक समीकरण लिखिए।परिभाषा के अनुसार, बंध ऊर्जा टूटे हुए बंधों का योग घटाकर बनने वाले बंधों का योग है: H = H (टूटे हुए बंधन) - H (बन गए बांड)। H बाध्यकारी ऊर्जा में परिवर्तन को दर्शाता है, जिसे बंधन की थैलीपी भी कहा जाता है, और ∑H रासायनिक प्रतिक्रिया समीकरण के दोनों पक्षों के लिए बाध्यकारी ऊर्जा के योग से मेल खाती है।
रासायनिक समीकरण लिखिए और अलग-अलग तत्वों के बीच सभी बंधों को लेबल कीजिए।यदि प्रतिक्रिया समीकरण को रासायनिक प्रतीकों और संख्याओं के रूप में दिया जाता है, तो इसे फिर से लिखना और परमाणुओं के बीच सभी बंधनों को इंगित करना उपयोगी होता है। इस तरह का एक दृश्य रिकॉर्ड आपको इस प्रतिक्रिया के दौरान टूटे और बनने वाले बंधनों को आसानी से गिनने की अनुमति देगा।
टूटे और बने बंधों को गिनने के नियम जानें।ज्यादातर मामलों में, गणना में बाध्यकारी ऊर्जा के औसत मूल्यों का उपयोग किया जाता है। विशेष अणु के आधार पर एक ही बंधन में थोड़ी अलग ऊर्जा हो सकती है, इसलिए औसत बंधन ऊर्जा आमतौर पर उपयोग की जाती है। .
किसी दिए गए परमाणु के बनने वाले रासायनिक बंधों की संख्या के साथ बाहरी शेल में इलेक्ट्रॉनों की संख्या पर डेटा की तुलना से पता चलता है कि हाइड्रोजन अणु के अध्ययन में सामने आए रासायनिक बंधन गठन के सिद्धांत अन्य परमाणुओं के लिए भी मान्य हैं। ऐसा इसलिए है क्योंकि बंधन प्रकृति में विद्युत है और दो इलेक्ट्रॉनों (प्रत्येक परमाणु से एक) द्वारा बनता है। इसलिए, परमाणुओं की पहली आयनीकरण ऊर्जा (पीईआई) (एक इलेक्ट्रोस्टैटिक मूल वाले) और डायटोमिक अणुओं में उनकी बाध्यकारी ऊर्जा के बीच एक सहसंबंध की उम्मीद की जानी चाहिए।
दूसरे और तीसरे आवर्त के परमाणुओं से बने कई द्विपरमाणुक अणुओं (गैस चरण में) के लिए बाध्यकारी ऊर्जा निर्धारित करने पर प्रायोगिक डेटा तालिका 4.2 और अंजीर में दिखाया गया है। 4.2.1.
तालिका 4.2
|
अणु ए 2 |
बंधन ऊर्जा (केजे/मोल) |
अणु |
बॉन्ड एनर्जी (केजे / एमओएल) |
||
चावल। 4.2-1 तत्व के पीईआई के आधार पर दूसरे और तीसरे आवर्त के तत्वों से अणुओं में बंधन ऊर्जा
ये डेटा (तालिका 4.2, चित्र 4.2-1 देखें) दिखाते हैं कि परमाणुओं के बीच बाध्यकारी ऊर्जा बंधित परमाणुओं के एसईआई से व्यावहारिक रूप से स्वतंत्र है।
क्या यह संभव है कि द्विपरमाणुक अणुओं (जहाँ एक से अधिक इलेक्ट्रॉन हों) में आबंध किसी भिन्न क्रियाविधि के अनुसार बनता है और अतिरिक्तपहले हमारे द्वारा अनदेखी की गई ताकतें?
इन बलों की पहचान के लिए आगे बढ़ने से पहले, आइए इसे समझाने की कोशिश करें आजादीमौजूदा बातचीत के आधार पर।
आइए अतिरिक्त कारकों की जांच करके शुरू करें जो अपेक्षित सहसंबंध की कमी की व्याख्या करते हैं और आजादीडायटोमिक अणुओं में बाध्यकारी ऊर्जा से पीईआई के मापन पर प्रयोगात्मक डेटा।
हम तालिका (4.2) को चार समूहों में विभाजित करते हैं:
समूह अ 40 kJ/mol से कम बाध्यकारी ऊर्जा वाले समान परमाणुओं वाले अणु शामिल हैं। गैस चरण में, ये अणु परमाणुओं में टूट जाते हैं।
ग्रुप बीसमान परमाणुओं से युक्त डायटोमिक अणु शामिल हैं, बाध्यकारी ऊर्जा जिसमें 400 kJ/mol से लेकर 1000 kJ/mol तक है। दरअसल, इन अणुओं में बाध्यकारी ऊर्जा हाइड्रोजन अणु में बाध्यकारी ऊर्जा की तुलना में काफी ऊपर की ओर भिन्न होती है, जो कि 429 kJ/mol है।
समूहसाथ मेंविभिन्न परमाणुओं से युक्त डायटोमिक अणु शामिल हैं, जिनकी बाध्यकारी ऊर्जा 340 kJ/mol से 550 kJ/mol तक भिन्न होती है।
समूहडीसमान परमाणुओं वाले द्विपरमाणुक अणु शामिल हैं, जिनकी बाध्यकारी ऊर्जा 50-350 kJ/mol है।
टेबल 4.4
संचार ऊर्जाअणुओं में
|
समूह अ |
समूह बी |
||
| अणु | बाँधने वाली ऊर्जा | अणु | बाँधने वाली ऊर्जा |
| 2 . बनें | 30 | सी2 | 602 |
| ने 2 | 4 | एन 2 | 941 |
| 7.6 | O2 | 493 | |
| एआर 2 | 7 | पी2 | 477 |
| एस 2 | 421 | ||
|
समूह सी |
समूह डी |
||
| अणु | ऊर्जा | अणु | ऊर्जा |
| लीफ | 572 | बी2 | 274 |
| NaF | 447 | Br2 | 190 |
| LiCl | 480 | Cl2 | 239 |
| सोडियम क्लोराइड | 439 | F2 | 139 |
| ली 2 | 110 | ||
| ना 2 | 72 | ||
स्पष्टीकरण शुरू करने से पहले, आइए उन मुद्दों को स्पष्ट करें जिन्हें हमें कवर करने की आवश्यकता है।
प्रथमप्रश्न:
हाइड्रोजन अणु की तुलना में बहुइलेक्ट्रॉन परमाणुओं के बीच बाध्यकारी ऊर्जा बहुत कम या अधिक क्यों होती है (सारणी 4.2) (सारणी 4.2)एच2)?
हाइड्रोजन अणु में बाध्यकारी ऊर्जा से पॉलीएटोमिक अणुओं में बाध्यकारी ऊर्जा के महत्वपूर्ण विचलन की व्याख्या करने के लिए, बाहरी कोश में इलेक्ट्रॉनों की संख्या सीमित होने के कारण की हमारी समझ को गहरा करना आवश्यक है।
एक इलेक्ट्रॉन का परमाणु से जुड़ाव तब होता है जब ऊर्जा में वृद्धि होती है, या, दूसरे शब्दों में, यदि शुद्धप्रणाली की संभावित ऊर्जा का मूल्य परमाणु + इलेक्ट्रॉनइलेक्ट्रॉन और परमाणु के बीच बंधन के परिणामस्वरूप बढ़ता है। एक इलेक्ट्रॉन के लिए एक परमाणु की आत्मीयता पर डेटा, तालिका 4.3 में दर्शाया गया है, हमें ऊर्जा में लाभ का संख्यात्मक मान देता है जब एक इलेक्ट्रॉन एक परमाणु से जुड़ा होता है।
टेबल 4.3
|
आत्मीयता |
|
आत्मीयता |
जब एक इलेक्ट्रॉन एक परमाणु से जुड़ा होता है, तो नाभिक की ओर आकर्षित इलेक्ट्रॉनों की संख्या में वृद्धि के कारण नाभिक के प्रति इलेक्ट्रॉनों के आकर्षण की कुल ऊर्जा बढ़ जाती है। दूसरी ओर, इलेक्ट्रॉनों की संख्या में वृद्धि के कारण इंटरइलेक्ट्रॉन प्रतिकर्षण की ऊर्जा बढ़ जाती है। अर्थात्, एक परमाणु के साथ एक इलेक्ट्रॉन का लगाव तब होता है, जब इस संबंध के परिणामस्वरूप, आकर्षण की ऊर्जा में लाभ, प्रतिकर्षण की ऊर्जा में वृद्धि के कारण ऊर्जा के नुकसान से अधिक होता है।
जब एक परमाणु में एक इलेक्ट्रॉन जोड़ा जाता है तो ऊर्जा में परिवर्तन की गणना करना हाइड्रोजन 3.4 eV का ऊर्जा लाभ देता है। अर्थात् हाइड्रोजन परमाणु में धनात्मक इलेक्ट्रॉन बंधुता होनी चाहिए। प्रयोग में यही देखा गया है।
संभावित ऊर्जा में परिवर्तन की एक समान गणना जब एक इलेक्ट्रॉन एक परमाणु से जुड़ा होता है हीलियमयह दर्शाता है कि एक इलेक्ट्रॉन के जुड़ने से स्थितिज ऊर्जा में वृद्धि नहीं होती है, बल्कि इसकी कमी होती है। दरअसल, हीलियम परमाणु की आत्मीयता, प्रयोग के अनुसार, शून्य से कम है।
इसलिए, एक इलेक्ट्रॉन को एक परमाणु से जोड़ने या न जोड़ने की संभावना सभी इलेक्ट्रॉनों के नाभिक और पारस्परिक इंटरइलेक्ट्रॉनिक प्रतिकर्षण के आकर्षण की संभावित ऊर्जा के निरपेक्ष मूल्यों में परिवर्तन के अंतर से निर्धारित होती है। यदि यह अंतर शून्य से अधिक है, तो इलेक्ट्रॉन जुड़ जाएगा, और यदि यह शून्य से कम है, तो नहीं।
तालिका 4.3 में दिए गए इलेक्ट्रॉन के लिए परमाणुओं की आत्मीयता के आंकड़े बताते हैं कि पहली, दूसरी और तीसरी अवधि के परमाणुओं के अलावा होना,मिलीग्राम,ने,एआरनाभिक से इलेक्ट्रॉनों के लगाव के दौरान आकर्षण ऊर्जा में वृद्धि प्रतिकर्षण की ऊर्जा में वृद्धि से अधिक होती है।
परमाणुओं के मामले में होना,मिलीग्राम,ने,एआर,नाभिक से इलेक्ट्रॉनों के लगाव के दौरान आकर्षण की ऊर्जा में वृद्धि इंटरइलेक्ट्रॉन प्रतिकर्षण की ऊर्जा में वृद्धि से कम है। इस निष्कर्ष की एक स्वतंत्र पुष्टि तालिका 4.2 (समूह ए) में दी गई दूसरी और तीसरी अवधि के परमाणुओं के लिए पीईआई की जानकारी है।
जब एक रासायनिक बंधन बनता है, तो परमाणुओं के बाहरी इलेक्ट्रॉन कोशों में इलेक्ट्रॉनों की संख्या एक इलेक्ट्रॉन से बढ़ जाती है, और हाइड्रोजन अणु मॉडल की गणना के अनुसार एच 2,बाध्य परमाणुओं के प्रभावी आवेश बदल जाते हैं। बंधे हुए नाभिक के प्रभावी आवेश आवेशित नाभिकों के आकर्षण के कारण और बाध्य परमाणुओं के बाहरी कोशों में इलेक्ट्रॉनों की संख्या में वृद्धि के कारण बदलते हैं।
हाइड्रोजन अणु में, नाभिक के दृष्टिकोण से नाभिक के लिए बाध्यकारी इलेक्ट्रॉनों के आकर्षण बल में 50% की वृद्धि होती है, जो कि 0.5 प्रोटॉन इकाइयों द्वारा बाध्य नाभिक के प्रभावी चार्ज में वृद्धि के बराबर है (अध्याय 3 देखें) .
ऊर्जा लाभ के संदर्भ में, बंधन निर्माण एक तटस्थ परमाणु (मापा गया इलेक्ट्रॉन आत्मीयता) के लिए एक इलेक्ट्रॉन के लगाव और एक परमाणु के लिए एक इलेक्ट्रॉन के लगाव के बीच एक मध्यवर्ती प्रक्रिया की तरह है, जिसका परमाणु चार्ज 1 इकाई बढ़ जाता है।
तालिका 4.3 के अनुसार, लिथियम (PEI - 519 kJ/mol) से बेरिलियम (PEI - 900 kJ/mol) में जाने पर, PEI 400 kJ/mol तक बढ़ जाता है, और जब बेरिलियम से बोरॉन (PEI - 799 kJ/mol) में जाता है ) ऊर्जा लाभ घटकर 100 kJ/mol हो जाता है।
याद रखें कि बोरॉन के बाहरी इलेक्ट्रॉन शेल में 3 इलेक्ट्रॉन होते हैं, और बेरिलियम के बाहरी शेल में 2 इलेक्ट्रॉन होते हैं। अर्थात्, जब एक इलेक्ट्रॉन एक प्रोटॉन इकाई द्वारा परमाणु आवेश में एक साथ वृद्धि के साथ बेरिलियम से जुड़ता है, तो बाध्य इलेक्ट्रॉन बेरिलियम के बाहरी आवरण में प्रवेश करता है, जबकि ऊर्जा लाभ 100 kJ/mol से कम होगा जब एक इलेक्ट्रॉन बाहरी आवरण में प्रवेश करता है। लिथियम का (लिथियम से बेरिलियम में संक्रमण के दौरान)।
अब, तालिका 4.3 में दर्शाए गए नकारात्मक परमाणु-से-इलेक्ट्रॉन आत्मीयता वाले परमाणुओं की बाध्यकारी ऊर्जा में तेज कमी काफी समझ में आती है। हालाँकि, भले ही ने,होना,मिलीग्राम,एआरइलेक्ट्रॉनों को संलग्न नहीं करते, वे अणु बनाते हैं, क्योंकि प्रभावी नाभिकीय आवेश बढ़ता है। इन अणुओं में बाध्यकारी ऊर्जा (समूह .) लेकिन) अन्य अणुओं की तुलना में बहुत कम है।
अब चलिए जवाब दूसराप्रश्न: समूह बी डायटोमिक अणुओं में बाध्यकारी ऊर्जा तालिका 4.2 में क्यों दिखाई गई है। हाइड्रोजन अणु में बाध्यकारी ऊर्जा से 1.5-2 गुना अधिक है?
कार्बन परमाणुओं के बाहरी कोश पर (सी)नाइट्रोजन (एन)और ऑक्सीजन (ओ)क्रमशः 4, 5 और 6 इलेक्ट्रॉन हैं। इन परमाणुओं द्वारा बनने वाले बंधों की संख्या उन अतिरिक्त इलेक्ट्रॉनों की संख्या से सीमित होती है जो बंधन बनने पर बाहरी आवरण में प्रवेश कर सकते हैं। तो कार्बन परमाणु (सी)नाइट्रोजन (एन)और ऑक्सीजन (ओ) क्रमशः 4, 3 और 2 रासायनिक बंध बना सकते हैं। तदनुसार, तालिका 4.4 में दिखाए गए दो परमाणुओं के बीच, एक नहीं, बल्कि कई रासायनिक बंधन बन सकते हैं, जिसका अर्थ है कि एक डायटोमिक अणु में 1 बंधन के गठन की तुलना में ऊर्जा में बहुत अधिक लाभ होता है, जहां बंधित परमाणुओं में 1 इलेक्ट्रॉन होता है। बाहरी खोल में
यदि परमाणु एक रासायनिक बंधन से जुड़े होते हैं, तो ऐसे बंधन को एकल बंधन कहा जाता है। रसायनिक बंधया सामान्य रासायनिक बंधन।जब परमाणु कई रासायनिक बंधों (दोहरे या तिहरे) से जुड़े होते हैं, तो ऐसे बंधन कहलाते हैं एकाधिक बंधन. एकाधिक बंधन, उदाहरण के लिए, नाइट्रोजन अणुओं में (एन 2)और ऑक्सीजन (ओ2)संरचनात्मक सूत्रों द्वारा वर्णित हैं: एन नहींऔर ओ = ओ।
अब समूह पर विचार करें साथ में: अलग-अलग परमाणुओं से बने कुछ डायटोमिक अणुओं में बाध्यकारी ऊर्जा समान परमाणुओं से बने अन्य अणुओं की तुलना में बहुत अधिक क्यों होती है?
आइए अणु को अलग करें सोडियम क्लोराइड. सोडियम और क्लोरीन परमाणु इलेक्ट्रॉन बंधुता में बहुत भिन्न होते हैं। हम बंधन गठन को दो चरणों वाली प्रक्रिया के रूप में प्रस्तुत करते हैं। पहले चरण में, इलेक्ट्रॉनों के लिए परमाणुओं की आत्मीयता के कारण ऊर्जा में लाभ प्राप्त होता है। अर्थात् इस दृष्टि से अणु के निर्माण के दौरान ऊर्जा में होने वाला लाभ Cl2, अणु बनाते समय से अधिक होना चाहिए सोडियम क्लोराइडउनकी इलेक्ट्रॉन आत्मीयता में अंतर से।
हाइड्रोजन अणु (अध्याय 3) की गणना करते समय, बाध्यकारी ऊर्जा (अणुओं को परमाणुओं में अलग करने के लिए आवश्यक ऊर्जा) दो घटकों का योग था:
हाइड्रोजन अणु और दो हाइड्रोजन परमाणुओं की इलेक्ट्रॉनिक ऊर्जा के बीच का अंतर;
पृथक अणुओं को गर्म करने पर खर्च होने वाली अतिरिक्त ऊर्जा।
पहले घटक की गणना करते हुए, हम अणु की ऊर्जा की गणना करते हैं, जो हाइड्रोजन परमाणुओं के नाभिक के इलेक्ट्रॉनों की बाध्यकारी जोड़ी के आकर्षण की ऊर्जा और इंटरइलेक्ट्रॉनिक और इंटरन्यूक्लियर बलों की प्रतिकारक ऊर्जा के योग के बीच अंतर के बराबर है।
इलेक्ट्रॉनों के बंधन युग्मों के लिए नाभिक के आकर्षण की ऊर्जा का अनुमान लगाने के लिए, साथ ही इंटरइलेक्ट्रॉन प्रतिकर्षण की ऊर्जा का अनुमान लगाने के लिए, हमें पहले बाध्य नाभिक के प्रभावी चार्ज के मूल्य का पता लगाना चाहिए।
डायटोमिक अणुओं में आयनीकरण क्षमता और बाध्यकारी ऊर्जा
ट्यूटोरियल
आस्ट्राखान
रासायनिक बंधन: पाठ्यपुस्तक / रयाबुखिन यू। आई। - अस्त्रखान: अस्त्रखान। राज्य तकनीक। अन-टी, 2013. - 40 पी।
इंजीनियरिंग और गैर-रासायनिक विशिष्टताओं के छात्रों के लिए बनाया गया है।
उच्च व्यावसायिक शिक्षा के राज्य शैक्षिक मानकों के अनुरूप है
चित्रण: 15 तस्वीर।, तालिका: 1, ग्रंथ सूची: 6 शीर्षक, ऐप।
विभाग के निर्णय द्वारा मुद्रित "सामान्य, अकार्बनिक और विश्लेषणात्मक रसायन विज्ञान" (प्रोटोकॉल संख्या __ दिनांक _________ 2013)
समीक्षक: कैंड। रसायन विज्ञान, एसोसिएट प्रोफेसर लेबेदेवा ए.पी.
© रयाबुखिन यू.आई., 2013
© एएसटीयू, 2013
परिचय
प्रकृति में, मुक्त परमाणुओं के रूप में रासायनिक तत्व (महान गैसों के अपवाद के साथ - समूह VIIIA के तत्व) व्यावहारिक रूप से नहीं पाए जाते हैं। आमतौर पर, एक रासायनिक तत्व के परमाणु या तो एक दूसरे के साथ या अन्य तत्वों के परमाणुओं के साथ बातचीत करते हैं, क्रमशः सरल या जटिल पदार्थों की उपस्थिति के साथ रासायनिक बंधन बनाते हैं। इसी समय, विभिन्न पदार्थों के अणु एक दूसरे के साथ परस्पर क्रिया करते हैं।
रासायनिक बंधन का सिद्धांत सभी सैद्धांतिक रसायन विज्ञान का आधार है।
रासायनिक बंधन 1 - यह बलों का एक समूह है जो परमाणुओं को एक दूसरे से अधिक स्थिर संरचनाओं - अणुओं या क्रिस्टल में बांधता है।
अणुओं और क्रिस्टल का निर्माण मुख्य रूप से इलेक्ट्रॉनों और परमाणु नाभिकों के बीच कूलम्ब आकर्षण के कारण होता है।
रासायनिक बंधन की प्रकृति को माइक्रोवर्ल्ड को नियंत्रित करने वाले क्वांटम (तरंग) यांत्रिकी के नियमों की खोज के बाद ही समझा गया था। आधुनिक सिद्धांत इस सवाल का जवाब देता है कि रासायनिक बंधन क्यों होता है और इसकी ताकतों की प्रकृति क्या है।
रासायनिक बंधों का बनना एक स्वतःस्फूर्त प्रक्रिया है; अन्यथा, न तो सरल और न ही जटिल पदार्थ मौजूद होंगे। थर्मोडायनामिक दृष्टिकोण से, रासायनिक बंधन के गठन का कारण सिस्टम की ऊर्जा में कमी है।
एक रासायनिक बंधन का निर्माण ऊर्जा की रिहाई के साथ होता है, और इसके टूटने के लिए ऊर्जा के व्यय की आवश्यकता होती है।
एक रासायनिक बंधन की विशेषताएं इसकी ऊर्जा और लंबाई हैं।
रासायनिक बंधन ऊर्जा इसके गठन और इसकी ताकत को चिह्नित करने की प्रक्रिया में जारी ऊर्जा है; बाध्यकारी ऊर्जा केजे में गठित पदार्थ के प्रति तिल में व्यक्त की जाती है (ई अनुसूचित जनजाति। , केजे / एमओएल) 2।
रासायनिक बंधन की ऊर्जा जितनी अधिक होगी, बंधन उतना ही मजबूत होगा। एक द्विपरमाणुक अणु के रासायनिक बंधन की ऊर्जा का अनुमान इसके गठन से पहले की अवस्था से तुलना करके लगाया जाता है। एक ही प्रकार के बंधन वाले बहुपरमाणुक अणुओं के लिए, औसत रासायनिक बंधन ऊर्जा की गणना की जाती है (उदाहरण के लिए, एच 2 ओ या सीएच 4 के लिए)।
औसत रासायनिक बंधन ऊर्जाएक अणु की गठन ऊर्जा को उसके बंधों की संख्या से विभाजित करके निर्धारित किया जाता है।
रासायनिक बंधन लंबाईअणु में परमाणुओं के नाभिकों के बीच की दूरी कहलाती है।
बॉन्ड की लंबाई बॉन्डिंग परमाणुओं के आकार और उनके इलेक्ट्रॉन गोले के ओवरलैप की डिग्री से निर्धारित होती है।
उदाहरण के लिए, हाइड्रोजन फ्लोराइड और हाइड्रोजन आयोडाइड के लिए:

मैंएचएफ< मैंनमस्ते
जुड़े कणों (परमाणुओं या अणुओं) के प्रकार के आधार पर, हैं इंट्रामोल्युलर बांडजिसके माध्यम से अणु बनते हैं, और अंतर-आणविक बंधन,अणुओं से सहयोगियों के गठन या एक अणु में अलग-अलग कार्यात्मक समूहों के परमाणुओं के बंधन के लिए अग्रणी। इस प्रकार के बांड ऊर्जा में तेजी से भिन्न होते हैं: इंट्रामोल्युलर बॉन्ड के लिए, ऊर्जा 100-1000 kJ/mol 1 होती है, और इंटरमॉलिक्युलर बॉन्ड के लिए, यह आमतौर पर 40 kJ/mol से अधिक नहीं होती है।
शिक्षा पर विचार करें इंट्रामोलीक्युलर रसायनिक बंधहाइड्रोजन परमाणुओं की परस्पर क्रिया के उदाहरण पर।
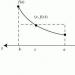
जब दो हाइड्रोजन परमाणु एक-दूसरे के पास पहुंचते हैं, तो उनके इलेक्ट्रॉनों के बीच एंटीपैरलल स्पिन के साथ एक मजबूत विनिमय बातचीत होती है, जिससे एक सामान्य इलेक्ट्रॉन जोड़ी दिखाई देती है। इससे इंटरन्यूक्लियर स्पेस में इलेक्ट्रॉन घनत्व बढ़ जाता है, जो नाभिक, परस्पर क्रिया करने वाले परमाणुओं के आकर्षण में योगदान देता है। नतीजतन, सिस्टम की ऊर्जा कम हो जाती है और सिस्टम अधिक स्थिर हो जाता है - रसायनिक बंध(चित्र .1)।

चावल। 1. हाइड्रोजन परमाणुओं के बीच रासायनिक बंधन के निर्माण का ऊर्जा आरेख
सिस्टम में परमाणुओं के नाभिक के बीच एक निश्चित दूरी पर न्यूनतम ऊर्जा होती है; परमाणुओं के आगे के दृष्टिकोण के साथ, नाभिक के बीच प्रतिकारक बलों में वृद्धि के कारण ऊर्जा बढ़ जाती है।
इस पर निर्भर करते हुए कि आम इलेक्ट्रॉन जोड़ी परमाणुओं के नाभिक के साथ कैसे संपर्क करती है, तीन मुख्य प्रकार के रासायनिक बंधन होते हैं: अंडाकार, आयनिक, धात्विक और हाइड्रोजन बांड।