9885 0
HPLC je tečna kolonska hromatografija, u kojoj se mogu koristiti različiti mehanizmi sorpcije. U suštini, HPLC je moderan oblik klasične tečne kolonske hromatografije. U nastavku su navedene neke od najznačajnijih kvalitativnih karakteristika HPFA:
- velika brzina procesa, što je omogućilo da se smanji trajanje razdvajanja sa nekoliko sati i dana na minute;
- minimalni stepen zamućenja hromatografskih zona, koji omogućava odvajanje jedinjenja koja se neznatno razlikuju u konstantama sorpcije;
- visok stepen mehanizacije i automatizacije odvajanja i obrade informacija, zahvaljujući čemu je kolonska tečna hromatografija dostigla novi nivo ponovljivosti i tačnosti.
Intenzivna proučavanja poslednjih decenija, ogromna količina akumuliranih eksperimentalnih podataka danas omogućavaju da se govori o klasifikaciji varijanti u okviru metode tečne hromatografije visokih performansi. Naravno, u ovom slučaju, klasifikacija prema gore datom mehanizmu sorpcije ostaje važeća.
Uobičajena klasifikacija zasniva se na komparativnom polaritetu mobilne i stacionarne faze. Pravi se razlika između hromatografije normalne i reverzne faze.
Kromatografija normalne faze (NPC) je varijanta HPLC-a kada je mobilna faza manje polarna od stacionarne faze, i postoji razlog za vjerovanje da je glavni faktor koji određuje retenciju interakcija sorbata direktno s površinom ili zapreminom sorbenta. .
Reverzno-fazna hromatografija (RPC) je varijanta HPLC-a kada je mobilna faza polarnija od stacionarne, a zadržavanje se određuje direktnim kontaktom molekula sorbata sa površinom ili zapreminom sorbenta; u ovom slučaju ionizirani sorbati se ne zamjenjuju za jone mobilne faze adsorbirane na površini.
Iono-izmjenjivačka kromatografija - varijanta u kojoj se sorpcija provodi zamjenom sorpiranih iona mobilne faze za jone hromatografiranih tvari; Ligand-izmjenjivačka hromatografija može se odrediti na potpuno isti način.
Kromatografija na dinamički modificiranim sorbentima je varijanta HPLC-a, u kojoj sorbat ne stupa u direktnu interakciju s površinom sorbenta, već ulazi u vezu s molekulima pripovršinskih slojeva eluenta.
Jonska parna hromatografija je varijanta reverzno-fazne hromatografije jonizovanih jedinjenja, u kojoj se mobilnoj fazi dodaje hidrofobni kontrajon, koji kvalitativno menja sorpcione karakteristike sistema.
Ekskluziona hromatografija je metoda za odvajanje spojeva prema njihovoj molekularnoj težini, zasnovana na razlici u brzini difuzije u porama stacionarne faze molekula različitih veličina.
Za HPFA, vrlo važna karakteristika je veličina sorbenata, obično 3-5 µm, sada do 1,8 µm. To omogućava brzo i potpuno odvajanje složenih mješavina supstanci (prosječno vrijeme analize je od 3 do 30 min).
Zadatak odvajanja rješava se pomoću kromatografske kolone, koja je cijev ispunjena sorbentom. Tokom analize, tečnost (eluent) određenog sastava se dovodi kroz hromatografsku kolonu konstantnom brzinom. Tačno izmjerena doza uzorka se ubrizgava u ovaj tok. Komponente uzorka unesene u hromatografsku kolonu, zbog različitog afiniteta prema sorbentu kolone, kreću se duž nje različitim brzinama i do detektora dospevaju uzastopno u različito vreme.
Dakle, hromatografska kolona je odgovorna za selektivnost i efikasnost razdvajanja komponenti. Odabirom različitih tipova kolona možete kontrolisati stepen odvajanja analiziranih supstanci. Jedinjenja se identifikuju po vremenu zadržavanja. Kvantitativno određivanje svake od komponenti se izračunava na osnovu veličine analitičkog signala izmjerenog pomoću detektora spojenog na izlaz hromatografske kolone.
Sorbenti. Formiranje HPLC-a je u velikoj mjeri povezano sa stvaranjem novih generacija sorbenata sa dobrim kinetičkim svojstvima i različitim termodinamičkim svojstvima. Glavni materijal za sorbente u HPLC-u je silika gel. Mehanički je jak i ima značajnu poroznost, što daje veliki kapacitet zamjene za male veličine stupova. Najčešća veličina čestica je 5-10 mikrona. Što je bliži sfernom obliku čestica, manji je otpor protoka, to je veća efikasnost, posebno ako se prosijava vrlo uska frakcija (na primjer, 7 +1 mikrona).
Specifična površina silika gela je 10-600 m/g. Silika gel se može modifikovati raznim hemijskim grupama koje su kalemljene na površinu (C-18, CN, NH2, SO3H), što omogućava korišćenje sorbenata na njegovoj osnovi za odvajanje različitih klasa jedinjenja. Glavni nedostatak silika gela je njegova niska hemijska otpornost pri pH< 2 и рН >9 (silicijum se rastvara u alkalijama i kiselinama). Stoga je trenutno u toku intenzivna potraga za sorbentima na bazi polimera koji su stabilni na pH od 1 do 14, na primjer na bazi polimetil metakrilata, polistirena itd.
Sorbenti za jonoizmenjivačku hromatografiju. Zbog specifičnosti separacije (u kiselom ili alkalnom mediju), glavni materijal je sorbent na polistiren sa divinilbenzenom različitog stepena umrežavanja sa SO3 -H + grupama cijepljenim na njihovu površinu (jako kiseli kationski izmjenjivači) ili -COO- Naf (izmjenjivači kationa sa slabom kiselinom), -H2N + (CH3) 3Cl- (anjonski izmjenjivači jake baze) ili -N+HR2Cl- (anjonski izmjenjivači sa slabom bazom).
Sorbenti za gel-penetrirajuću hromatografiju. Glavni tip je stiren-DVB. Koriste se i makroporozna stakla, metil metakrilat, silika gel. Za ionsku ekskluzijsku hromatografiju koriste se isti sorbenti.
Pumpe. Da bi se osigurao protok mobilne faze (MP) kroz kolonu sa navedenim parametrima, koriste se pumpe visokog pritiska. Najvažnije specifikacije za LC pumpe su: opseg protoka; maksimalni radni pritisak; ponovljivost protoka; opseg pulsiranja dovoda rastvarača.
Po prirodi opskrbe rastvaračem, pumpe mogu biti konstantnog napajanja (protoka) i konstantnog pritiska. U osnovi, u analitičkom radu koristi se režim konstantnog protoka, pri punjenju kolona koristi se režim konstantnog pritiska. Prema principu rada, pumpe se dijele na špric pumpe i klipne pumpe.
špric pumpe. Pumpe ovog tipa karakterizira gotovo potpuno odsustvo pulsiranja u protoku mobilne faze tokom rada. Nedostaci pumpe: a) velika potrošnja vremena i rastvarača za ispiranje pri promeni rastvarača; b) suspenzija odvajanja tokom punjenja pumpe; c) velike dimenzije i težina uz visok protok i pritisak (potreban vam je snažan motor i velika sila klipa sa svojom velikom površinom).
Klipne klipne pumpe. Pumpe ovog tipa osiguravaju konstantan volumetrijski protok mobilne faze dugo vremena. Maksimalni radni pritisak 300-500 atm, brzina protoka 0,01-10 ml/min. Reproducibilnost volumetrijske hrane - 0,5%. Glavni nedostatak je što se rastvarač uvodi u sistem u obliku niza uzastopnih impulsa, tako da dolazi do pulsiranja pritiska i protoka.
To je glavni razlog povećane buke i desenzibilizacije gotovo svih detektora koji se koriste u LC, posebno elektrohemijskih. Načini suzbijanja pulsiranja: korištenjem dvostrukih pumpi ili Bag-lai pumpe s dva klipa, korištenjem prigušnih uređaja i elektroničkih uređaja.
Količina volumetrijske hrane određena je trima parametrima: promjerom klipa (obično 3,13; 5,0; 7,0 mm), njegovom amplitudom (12-18 mm) i frekvencijom (koja ovisi o brzini rotacije motora i mjenjača).
Dozatori. Svrha dozatora je da prenese uzorak pod atmosferskim pritiskom do ulaza u kolonu pri pritiscima do nekoliko atmosfera. Važno je da u dozatoru nema „mrtvih“ zapremina koje ne može da ispere mobilna faza i da se uzorak ne ispere tokom doziranja. U početku su dozatori u LC-u bili slični plinskim dozatorima s membranskom punkcijom. Međutim, membrane ne drže više od 50-100 atm, njihova hemijska otpornost je nedovoljna, njihovi komadići zagađuju filtere kolone i kapilare.
U tečnoj fazi, brzina difuzije je mnogo niža nego u gasnoj fazi. Stoga je moguće dozirati sa zaustavljanjem protoka - uzorak nema vremena da se zamuti u dozatoru. Tokom ubrizgavanja uzorka u dozator, posebna slavina zatvara protok rastvarača. Pritisak na ulazu u kolonu brzo se smanjuje, nakon nekoliko sekundi uzorak se može ubrizgati u dozirnu komoru konvencionalnom mikrošpricom. Zatim se dozator zaključava, protok rastvarača se uključuje i dolazi do odvajanja.
Pritisak koji ovaj ventil drži je do 500-800 atm. Ali kada se protok zaustavi, ravnoteža u koloni se poremeti, što može dovesti do pojave "praznih" dodatnih vrhova.
Loop dozatori su najčešće korišteni. Prilikom punjenja dozatora pod visokim pritiskom postoje ulazi 1,2 i kanal između njih. Ulazi 3-6, kanali između njih i petlje za doziranje su pod atmosferskim pritiskom, što vam omogućava da petlju ispunite štrcaljkom ili pumpom. Kako se dozator rotira, protok mobilne faze tjera uzorak u kolonu. Da bi se smanjila greška, petlja se ispere sa 5-10 puta većom zapreminom uzorka. Ako je uzorak mali, onda se može ubrizgati u petlju mikrošpricom. Volumen petlje je obično 5-50 μl.
NA. Voinov, T.G. Volova
U tečnoj hromatografiji visokih performansi (HPLC), priroda procesa koji se dešavaju u hromatografskoj koloni generalno je identična procesima u gasnoj hromatografiji. Razlika je samo u upotrebi tečnosti kao stacionarne faze. Zbog velike gustine tečnih mobilnih faza i visokog otpora kolona, plinska i tečna hromatografija se uvelike razlikuju u instrumentaciji.
U HPLC, čisti rastvarači ili njihove mješavine se obično koriste kao mobilne faze.
Za stvaranje struje čistog rastvarača (ili mješavine rastvarača), koji se u tečnoj hromatografiji naziva eluent, koriste se pumpe koje su dio hidrauličkog sistema hromatografa.
Adsorpcijska kromatografija se izvodi kao rezultat interakcije tvari s adsorbensima, poput silika gela ili aluminijevog oksida, koji imaju aktivne centre na površini. Razlika u sposobnosti interakcije sa adsorpcijskim centrima različitih molekula uzorka dovodi do njihovog razdvajanja u zone u procesu kretanja sa mobilnom fazom kroz kolonu. Podjela zona komponenti koja se postiže u ovom slučaju ovisi o interakciji i sa rastvaračem i sa adsorbentom.
Silika gel adsorbenti različitih zapremina, površina i prečnika pora nalaze najveću primenu u HPLC. Aluminij oksid i drugi adsorbenti koriste se mnogo rjeđe. Glavni razlog za to:
nedovoljna mehanička čvrstoća, koja ne dozvoljava pakovanje i upotrebu na povišenim pritiscima tipičnim za HPLC;
silika gel u odnosu na aluminijum oksid ima širi raspon poroznosti, površine i prečnika pora; značajno veća katalitička aktivnost aluminijum oksida dovodi do izobličenja rezultata analize usled razgradnje komponenti uzorka ili njihove ireverzibilne hemisorpcije.
HPLC detektori
Tečna hromatografija visokih performansi (HPLC) se koristi za detekciju polarnih neisparljivih supstanci, koje se iz nekog razloga ne mogu pretvoriti u oblik pogodan za gasnu hromatografiju, čak ni u obliku derivata. Takve supstance, posebno, uključuju sulfonske kiseline, boje rastvorljive u vodi i neke pesticide, kao što su derivati fenil-uree.
detektori:
UV - diodni niz detektora. "Matrica" fotodioda (ima ih više od dvije stotine) konstantno registruje signale u UV i vidljivom području spektra, čime se osigurava snimanje UV-B spektra u režimu skeniranja. Ovo omogućava kontinuirano snimanje, uz visoku osjetljivost, neiskrivljenih spektra komponenti koje brzo prolaze kroz posebnu ćeliju.
U poređenju sa detekcijom na jednoj talasnoj dužini, koja ne daje informacije o "čistoći" pika, mogućnost upoređivanja punih spektra niza dioda daje rezultat identifikacije sa mnogo većim stepenom sigurnosti.
Fluorescentni detektor. Velika popularnost fluorescentnih detektora je zbog vrlo visoke selektivnosti i osjetljivosti, te činjenice da mnogi zagađivači okoliša fluoresciraju (na primjer, poliaromatični ugljovodonici).
Elektrohemijski detektor koriste se za detekciju supstanci koje se lako oksidiraju ili redukuju: fenoli, merkaptani, amini, aromatični nitro i halogeni derivati, aldehidi, ketoni, benzidini.
Kromatografsko odvajanje smjese na koloni zbog sporog napredovanja PF traje dugo. Kako bi se ubrzao proces, hromatografija se provodi pod pritiskom. Ova metoda se naziva tečna hromatografija visokih performansi (HPLC).
Modernizacija opreme koja se koristi u klasičnoj tečnoj kolonskoj hromatografiji učinila ju je jednom od perspektivnih i modernih metoda analize. Tečna hromatografija visokih performansi je pogodna metoda za odvajanje, preparativno izolovanje i izvođenje kvalitativne i kvantitativne analize neisparljivih, termolabilnih jedinjenja niske i visoke molekularne težine.
U zavisnosti od vrste sorbenta koji se koristi u ovoj metodi, koriste se 2 varijante hromatografije: na polarnom sorbentu koji koristi nepolarni eluent (opcija direktne faze) i na nepolarnom sorbentu pomoću polarnog eluenta - tzv. reverzno -fazna tečna hromatografija visokih performansi (RPHLC).
Kada eluent pređe u eluent, ravnoteža u RPHLC uslovima se uspostavlja mnogo puta brže nego u uslovima polarnih sorbenata i nevodenih PF. Kao rezultat ovoga, kao i pogodnosti rada sa vodom i vodeno-alkoholnim eluentima, RPHLC je sada stekao veliku popularnost. Većina HPLC analiza se izvodi ovom metodom.
Detektori. Registracija izlaza iz kolone posebne komponente se vrši pomoću detektora. Za registraciju možete koristiti promjenu bilo kojeg analitičkog signala koji dolazi iz mobilne faze i koji se odnosi na prirodu i količinu komponente mješavine. Tečna kromatografija koristi analitičke signale kao što su apsorpcija svjetlosti ili emisija svjetlosti izlazne otopine (fotometrijski i fluorimetrijski detektori), indeks loma (refraktometrijski detektori), potencijal i električna provodljivost (elektrohemijski detektori) itd.
Rekorder snima kontinuirano detektovani signal. Kromatogram je slijed detektorskih signala snimljenih na traci snimača, generiranih kada pojedine komponente smjese izađu iz kolone. U slučaju razdvajanja smjese, pojedinačni pikovi su vidljivi na vanjskom hromatogramu. Položaj pika na kromatogramu se koristi u svrhu identifikacije supstance, visina ili površina pika - u svrhu kvantitativnog određivanja.
Uvod.
Brzi razvoj tečne hromatografije u poslednjih 10 godina uglavnom je rezultat intenzivnog razvoja teoretskih osnova i praktične upotrebe njene visokoefikasne verzije, kao i stvaranja i industrijske proizvodnje potrebnih sorbenata i opreme.
Karakteristična karakteristika tečne hromatografije visokih performansi (HPLC) je upotreba sorbenata veličine zrna od 3-10 µm, koji omogućavaju brz prenos mase uz veoma visoku efikasnost separacije.
Trenutno je HPLC zauzeo prvo mjesto među instrumentalnim metodama u pogledu brzine razvoja, nadmašujući čak i plinsku hromatografiju. Najvažnija prednost HPLC-a u odnosu na plinsku hromatografiju je mogućnost proučavanja gotovo bilo kojeg objekta bez ikakvih ograničenja u pogledu njegovih fizičko-hemijskih svojstava, na primjer, tačke ključanja ili molekularne težine.
Danas je HPLC dobro formirana instrumentalna metoda koja se široko koristi u različitim oblastima nauke i tehnologije. Njegova važnost je posebno velika u važnim oblastima kao što su biohemija, molekularna biologija, kontrola zagađenja životne sredine, kao i u hemijskoj, petrohemijskoj, prehrambenoj i farmaceutskoj industriji.
budući da je potrebno uzeti u obzir niz vrlo specifičnih zahtjeva zbog sljedećih karakteristika metodologije.
a. Kolone za HPLC su ispunjene nosačem sa vrlo malim prečnikom čestica. Kao rezultat, na koloni se stvaraju visoki pritisci pri prostornim brzinama rastvarača potrebnim za brzo odvajanje uzoraka.
b. Detektori koji se koriste u HPLC-u su osetljivi na fluktuacije protoka i pritiska eluenta (šum). Štaviše, kada se koriste detektori koncentracije, potrebna je još veća stabilnost zapreminske brzine eluenta.
in. Proces hromatografskog odvajanja je praćen nizom antagonističkih efekata, na primer, disperzija uzorka u mobilnoj fazi dovodi do mešanja odvojenih komponenti i smanjuje maksimalnu koncentraciju supstance u eluirajućem piku (u detektoru). Disperzija se uočava u svim dijelovima sistema od tačke ubrizgavanja uzorka do detektora.
d) Rastvarači koji djeluju kao mobilna faza često su sposobni da korodiraju opremu. Ovo se prvenstveno odnosi na rastvarače koji se koriste u hromatografiji reverzne faze, što se preferira u biohemijskim HPLC aplikacijama.
Specifičnosti HPLC-a kao instrumentalne tehnike moraju se uzeti u obzir u procesu razvoja, kreiranja i rada ovih sistema. Bilo je potrebno više od deset godina potrage i istraživanja da bi se stvorili komercijalni uzorci hromatografskih sistema i njihovih komponenti koji su dovoljno pouzdani, jednostavni i sigurni za rad sa prihvatljivim omjerom između cijene i tehničkih karakteristika. Nedavni trendovi prema smanjenju jezgri (i dužine i prečnika) tjeraju nas da postavljamo nove zahtjeve za instrumente.
1.1. EFIKASNOSTISELEKTIVNOST
Kromatografija je metoda razdvajanja komponenti mješavine na osnovu razlike u njihovoj ravnotežnoj distribuciji između dvije "nemešljive faze, od kojih je jedna stacionarna, a druga pokretna. Komponente uzorka kreću se kroz kolonu kada su u mobilnoj fazi i ostaju na mjestu kada su veći afinitet komponente za stacionarnu fazu, a manji za mobilnu fazu, to se sporije kreće kroz stup i duže se zadržava u njemu. Zbog razlike u afinitetu komponente mješavine za stacionarne i mobilne prihvatljivo vrijeme smjesu u pojedinačne trake (pikove) komponenti dok se kreću kroz kolonu s mobilnom fazom.
Iz ovih opštih ideja jasno je da je hromatografsko razdvajanje moguće samo ako će komponente uzorka, koje ulaze u kolonu tokom ubrizgavanja uzorka, prvo biti rastvorene u mobilnoj fazi i, drugo, interagovati (zadržati) sa stacionarnom fazom. Ako bilo koja komponenta nije u rastvoru kada se uzorak ubrizgava, biće filtriran i neće učestvovati u hromatografskom procesu. Slično, komponente koje ne stupaju u interakciju sa stacionarnom fazom proći će kroz kolonu s mobilnom fazom bez razdvajanja na komponente.
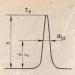
Prihvatimo uslov da su neke dvije komponente rastvorljive u mobilnoj fazi i da stupaju u interakciju sa stacionarnom fazom, odnosno da se hromatografski proces može odvijati bez smetnji. U ovom slučaju, nakon prolaska smjese kroz kolonu, mogu se dobiti hromatogrami oblika a, b ili in(Sl. 1.1). Ovi hromatogrami ilustruju hromatografske separacije koje se razlikuju po efikasnosti (a i b) sa jednakom selektivnošću i selektivnošću (b i u) sa jednakom efikasnošću.
Efikasnost kolone je veća što je pik uži pri istom vremenu zadržavanja. Efikasnost kolone se meri brojem teoretskih ploča (NPP) N:
što je veći ef-

 Rice. 1.2. Parametri kromatografskog pika i izračunavanje broja teoretskih ploča:
Rice. 1.2. Parametri kromatografskog pika i izračunavanje broja teoretskih ploča:
t R - vršno vrijeme zadržavanja; h - visina vrha; Wj/j - širina vrha na polovini njegove visine
Rice. 1.1. Vrsta hromatograma u zavisnosti od efikasnosti i selektivnosti kolone:
a- konvencionalna selektivnost, smanjena efikasnost (manje teorijskih ploča); b - konvencionalna selektivnost i efikasnost; u - konvencionalna efikasnost, povećana selektivnost (veći omjer vremena zadržavanja komponenti)
efikasnost, što je veći FTT, što je manja ekspanzija vršnog opsega prvobitno uskog pojasa dok prolazi kroz kolonu, to je uži vrh na izlazu kolone. NTT karakteriše broj koraka za uspostavljanje ravnoteže između mobilne i stacionarne faze.
Poznavanje broja teoretskih ploča po koloni i dužine stuba L (µm), kao i prosječni prečnik zrna sorbenta dc (µm), lako je dobiti vrijednosti teorijske ekvivalentne visine ploče (HETP), kao i smanjene teorijske ekvivalentne visine ploče (PHETP):
HETT = L/ N
PVETT \u003d B3TT / d c .
Uz vrijednosti NTT, HETP i PVETP, lako se može uporediti efikasnost kolona različitih tipova, različitih dužina, punjenih sorbentima različite prirode i granulacije. Upoređujući NTT dva stuba iste dužine, uporedite njihovu efikasnost. Kada se poredi HETP, kolone se porede sa sorbentima iste veličine zrna, različitih dužina. Konačno, vrijednost PVETT-a omogućava da bilo koje dvije kolone ocijene kvalitet sorbenta, prvo, i kvalitet punjenja kolona, i drugo, bez obzira na dužinu kolona, zrnastost po sorbentima njegove prirode.
Selektivnost kolone igra veliku ulogu u postizanju hromatografskog odvajanja.
Selektivnost kolone zavisi od velikog broja faktora, a veština eksperimentatora je u velikoj meri određena sposobnošću da utiče na selektivnost razdvajanja. Da bi to uradio, hromatograf ima tri veoma važna faktora u svojim rukama: izbor hemijske prirode sorbenta, izbor sastava rastvarača i njegovih modifikatora i razmatranje hemijske strukture i svojstava komponenti za biti odvojeni. Ponekad primjetan učinak na selektivnost ima promjena temperature kolone, koja mijenja koeficijente raspodjele tvari između mobilne i stacionarne faze.
Kada se razmatra razdvajanje dvije komponente u kromatogramu i procjenjuje se, rezolucija je važan parametar. Rs, koji povezuje izlazna vremena i vršne širine obje odvojene komponente
Rezolucija kao parametar koji karakteriše razdvajanje pikova raste kako raste selektivnost, što se odražava povećanjem brojilaca, a efikasnost, koja se odražava smanjenjem vrednosti nazivnika usled smanjenja širine pikova, raste. Stoga je brzi napredak tečne hromatografije doveo do promene koncepta „tečne hromatografije visokog pritiska“ – zamenjena je „tečnom hromatografijom visokih performansi“ (dok je skraćena notacija termina na engleskom jeziku sačuvana HPLC kao najispravnija karakterizacija pravca razvoja moderne tečne hromatografije).
Dakle, ispiranje kolone je smanjeno i efikasnost povećana kada se koriste finiji, ujednačeniji (uski rez) sorbent, gušće i ujednačenije upakovan u kolonu, tanje vezane faze, manje viskozna rastvarača i optimalne brzine protoka.
Međutim, uz razmazivanje trake hromatografske zone tokom odvajanja u koloni, ona se može razmazati i u uređaju za ubrizgavanje uzorka, u kapilare injektor-kolona i kolona-detektor koji spajaju kapilare, u detektorsku ćeliju i u neke pomoćne uređaje ( mikrofilteri za hvatanje mehaničkih čestica iz uzoraka instaliranih nakon injektora, predkolona, reaktorskih zavojnica, itd.) - Zamućenje je veće, što je veći volumen ekstra kolone u odnosu na zadržani volumen vrha. Također je važno gdje se nalazi mrtvi volumen: što je uži hromatografski poziv, mrtvi volumen će dati više zamućenja. Stoga posebnu pažnju treba obratiti na dizajn onog dijela hromatografa gdje je hromatografska zona najuža (injektor i uređaji od injektora do kolone) – ovdje je razmazivanje van kolone najopasnije i utiče na najviše. Iako se smatra da u dobro dizajniranim hromatografima izvore dodatnog razmazivanja izvan kolone treba minimizirati, ipak svaki novi uređaj, svaka izmjena hromatografa, nužno mora završiti ispitivanjem na koloni i poređenjem dobijenog hromatograma sa onaj pasoš. Ako se uoči vršna distorzija, naglo smanjenje efikasnosti, treba pažljivo pregledati kapilare i druge uređaje koji su tek uvedeni u sistem.
Razmazivanje van kolone i njegova pogrešna procjena mogu dovesti do značajnog (preko 50%) gubitka efikasnosti, posebno kada se pokušavaju koristiti relativno stari hromatografi za brzi HPLC, HPLC na mikro kolonama i druge moderne HPLC aplikacije koje zahtijevaju mikroinjektore. , spojne kapilare sa unutrašnjim prečnikom 0,05-0,15 mm minimalne dužine, kolone kapaciteta 10-1000 µl, detektori sa mikrokivetama kapaciteta 0,03-1 µl i sa velikom brzinom, brzi snimači i integratori.
1.2. ZADRŽAVANJE I ČVRSTOĆA RAZTAPALA
Da bi se analiti razdvojili na koloni, kao što je gore navedeno, faktor kapacitivnosti k" mora biti veći od 0, tj. tvari moraju biti zadržane stacionarnom fazom, sorbentom. Međutim, faktor kapacitivnosti ne bi trebao biti prevelik za postizanje prihvatljivog vremena eluiranja. Ako se za datu mešavinu supstanci odabere stacionarna faza, koja ih drži, onda se dalji rad na razvoju postupka analize sastoji u izboru otapala koje bi u idealnom slučaju obezbedilo različito za sve komponente, ali prihvatljivo ne mnogo veliko k". To se postiže promjenom jačine eluiranja rastvarača.
U slučaju adsorpcione hromatografije na silika gelu ili glinici, u pravilu se jačina dvokomponentnog otapala (na primjer, heksana s dodatkom izopropanola) povećava povećanjem sadržaja polarne komponente (izopropanola) u njemu. , ili smanjeni smanjenjem sadržaja izopropanola. Ako sadržaj polarne komponente postane prenizak (manje od 0,1%), treba je zamijeniti slabijom snagom eluiranja. Isto se radi, zamjenjujući ili polarnu ili nepolarnu komponentu drugim, čak i ako dati sistem ne pruža željenu selektivnost u odnosu na komponente mješavine od interesa. Prilikom odabira sistema rastvarača uzimaju se u obzir i rastvorljivosti komponenti smeše i eluotropni niz rastvarača koje su sastavili različiti autori.
Približno na isti način se odabire jačina otapala u slučaju korištenja cijepljenih polarnih faza (nitril, amino, diol, nitro, itd.), uzimajući u obzir moguće kemijske reakcije i isključujući otapala opasna za fazu (npr. , ketoni za amino fazu).
U slučaju hromatografije reverzne faze, jačina rastvarača se povećava povećanjem sadržaja organske komponente (metanol, acetonitril ili THF) u eluentu i smanjuje dodavanjem više vode. Ako se ne može postići željena selektivnost, koristi se druga organska komponenta ili se pokušava promijeniti uz pomoć raznih aditiva (kiseline, reagensi jonski par i sl.).
Kod odvajanja jono-izmjenjivačkom hromatografijom, jačina otapala se mijenja povećanjem ili smanjenjem koncentracije puferske otopine ili promjenom pH, u nekim slučajevima se koristi modifikacija organskim supstancama.
Međutim, posebno u slučaju složenih prirodnih i bioloških mješavina, često nije moguće odabrati jačinu rastvarača na način da se sve komponente uzorka eluiraju u prihvatljivom vremenu. Tada se mora pribjeći gradijentnom eluiranju, odnosno upotrijebiti rastvarač čija se elucijska moć tokom analize mijenja tako da se stalno povećava prema unaprijed određenom programu. Ovom tehnikom moguće je postići eluiranje svih komponenti složenih smjesa u relativno kratkom vremenskom periodu i njihovo razdvajanje na komponente u obliku uskih pikova.
1.3. VELIČINA, PROPUSNOST I EFIKASNOST SORBENTNIH ČESTICA
S obzirom na ispiranje kolone, istakli smo da efikasnost kolone (HETP) zavisi od veličine čestica sorbenta. U velikoj mjeri, brzi razvoj HPLC-a u posljednjih 10-12 godina bio je posljedica, prije svega, razvoja metoda za dobijanje sorbenata s veličinom čestica od 3 do 10 μm i sa uskim frakcijskim sastavom, koji osiguravaju visoku efikasnost sa dobra propusnost, i drugo, razvoj metoda za punjenje kolona ovim sorbentima i, treće, razvoj i serijska proizvodnja tečnih hromatografa sa pumpama za visoke pritiske, injektorima i detektorima sa kivetama male zapremine koji mogu da registruju pikove male zapremine.
Za dobro nabijene kolone sa suspenzijom, teoretska visina ekvivalenta ploče (REHP) može biti 2 bez obzira da li su za pakovanje korištene čestice od 3, 5, 10 ili 20 µm. U ovom slučaju dobićemo, redom, stubove (standardne dužine od 250 mm) sa efikasnošću od 41670, 25000, 12500 i 6250 tona. Čini se prirodnim odabrati najefikasniju kolonu prepunu čestica od 3 µm. Međutim, ova efikasnost dolazi po cenu rada pri veoma visokim pritiscima i relativno sporoj stopi odvajanja, pošto je dostupna pumpa verovatno u stanju da pumpa rastvarač kroz takvu kolonu velikom brzinom u prostoru. Ovdje se suočavamo s pitanjem odnosa između veličine čestica sorbenta, efikasnosti i permeabilnosti kolona.
Ako odavde izrazimo faktor otpora stuba - bezdimenzionalnu vrijednost, dobijamo sljedeću jednačinu:
Faktor otpora za kolone napunjene mikročesticama istog tipa istom metodom se neznatno mijenja i iznosi sljedeće vrijednosti:
Particle View"....Irregular Spherical
formu forme
Suvo pakovanje. . . . . 1000-2000 800-1200
pakovanje suspenzije. . . 700-1500 500-700
Ulazni pritisak u koloni je proporcionalan linearnoj brzini protoka, faktoru otpora kolone, viskoznosti rastvarača i dužini kolone i obrnuto proporcionalan kvadratu prečnika čestica.
Primjenjujući ovu ovisnost za gore navedene kolone sa česticama prečnika 3, 5, 10 i 20 μm i uz pretpostavku konstantne linearne brzine strujanja, faktora otpora kolone i viskoziteta rastvarača, dobijamo omjer ulaznog pritiska od 44:16:4:1 za kolone jednake dužine. Dakle, ako je za sorbent reverzne faze s veličinom čestica od 10 mikrona kada se koriste sistemi otapala metanol - . voda (70:30) je obično na standardnoj koloni pri brzini protoka rastvarača od 1 ml/min, pritisak na ulazu u kolonu je 5 MPa, zatim za čestice od 5 mikrona - 20 MPa i za 3 mikrona - 55 MPa. Kada se koristi silika gel i manje viskozni sistem rastvarača heksan - izopropanol (100:2), vrijednosti će biti znatno niže: 1, 4 i 11 MPa, respektivno. Ako je u slučaju sorbenta obrnute faze vrlo problematično korištenje čestica veličine 3 µm, a moguće je i 5 µm, ali ne na svim uređajima, onda za sorbent normalne faze nema problema s pritiskom. Treba napomenuti da moderni HPLC velike brzine obično koristi veće brzine protoka rastvarača nego u gornjem primjeru, tako da se zahtjevi za pritiskom još više povećavaju.
Međutim, u onim slučajevima kada je za odvajanje potreban određeni broj teoretskih ploča i poželjno je izvršiti analizu brzine, slika se donekle mijenja. Budući da će dužina kolona sa sorbentima veličine zrna od 3, 5, 10 mikrona, sa jednakom efikasnošću, biti 7,5, respektivno; 12,5 i 25 cm, tada će se odnos pritiska na ulazu u kolonu promeniti na 3,3:2:1. Shodno tome, trajanje analize na takvim kolonama jednake efikasnosti će se odnositi na 0,3:0,5:1, odnosno pri pomicanju sa 10 na 5 i 3 μm, trajanje analize će se smanjiti za 2 i 3,3 puta. Ova brža analiza dolazi po cijeni proporcionalno većeg ulaznog tlaka u koloni.
Navedeni podaci važe za one slučajeve kada sorbenti različite granulacije imaju iste krivulje distribucije veličine čestica, kolone su pakirane na isti način i imaju isti faktor otpora kolone. Treba imati na umu da se teškoća dobijanja uskih frakcija sorbenta povećava kako se veličina čestica smanjuje i to. frakcije različitih proizvođača imaju različit frakcijski sastav. Stoga će faktor otpora kolone varirati ovisno o veličini zrna, vrsti sorbenta, načinu pakovanja kolone itd.
KLASIFIKACIJA HPLC METODA PREMA MEHANIZMU SEPARACIJE
Većina odvajanja koje vrši HPLC zasniva se na mešovitom mehanizmu interakcije supstanci sa sorbentom, koji obezbeđuje veće ili manje zadržavanje komponenti u koloni. Mehanizmi razdvajanja u manje-više čistom obliku su prilično rijetki u praksi, na primjer, adsorpcija kada se za odvajanje aromatičnih ugljikovodika koriste apsolutno bezvodni silika gel i bezvodni heksan.
Sa mešovitim mehanizmom zadržavanja za supstance različite strukture i molekularne težine, moguće je proceniti doprinos adsorpcije, distribucije, isključenja i drugih mehanizama zadržavanju. Međutim, za bolje razumijevanje i razumijevanje mehanizama razdvajanja u HPLC-u, preporučljivo je uzeti u obzir separacije u kojima prevladava jedan ili drugi mehanizam u vezi sa određenim tipom hromatografije, na primjer hromatografijom za izmjenu jona.
2.1.1 ADSORPCIJSKA HROMATOGRAFIJA
Odvajanje adsorpcionom hromatografijom vrši se kao rezultat interakcije supstance sa adsorbensima, kao što su silika gel ili aluminijum oksid, koji imaju aktivne centre na površini. Razlika u sposobnosti interakcije sa adsorpcijskim centrima različitih molekula uzorka dovodi do njihovog razdvajanja u zone u procesu kretanja sa mobilnom fazom kroz kolonu. Odvajanje zona komponenti koje se postiže u ovom slučaju zavisi od interakcije i sa rastvaračem i sa adsorbentom.
Sorpcija na površini adsorbenta koji ima hidroksilne grupe zasniva se na specifičnoj interakciji između polarne površine adsorbenta i polarnih (ili polarizabilnih) grupa ili regiona molekula. Takve interakcije uključuju dipol-dipol interakciju između trajnih ili induciranih dipola, formiranje vodonične veze do formiranja n-kompleksa ili kompleksa za prijenos naboja. Moguća i prilično česta u praktičnom radu je manifestacija hemisorpcije, što može dovesti do značajnog povećanja vremena zadržavanja, naglog smanjenja efikasnosti, pojave produkata raspadanja ili ireverzibilne sorpcije supstance.
Izoterme adsorpcije tvari imaju linearan, konveksan ili konkavni oblik. Uz linearnu izotermu adsorpcije, vrh tvari je simetričan i vrijeme zadržavanja ne ovisi o veličini uzorka. Najčešće su izoterme adsorpcije tvari nelinearne i imaju konveksan oblik, što dovodi do neke asimetrije vrha s formiranjem repa.
Silika gel adsorbenti sa različitim zapreminama pora, površinama i prečnikom pora nalaze najveću primenu u HPLC. Aluminij oksid se koristi mnogo rjeđe i, izuzetno rijetko, drugi adsorbenti koji se široko koriste u klasičnoj kolonskoj i tankoslojnoj hromatografiji. Glavni razlog za to je nedovoljna mehanička čvrstoća većine drugih adsorbenata, što ne dozvoljava da se pakuju i koriste na povišenim pritiscima tipičnim za tečnosti visokog pritiska.
Polarne grupe odgovorne za adsorpciju i smještene na površini silika gela i aluminij oksida su slične po svojstvima. Stoga su obično redoslijed eluiranja mješavina supstanci i eluotropni niz rastvarača za njih isti. Međutim, razlika u kemijskoj strukturi silika gela i aluminij oksida ponekad dovodi do razlika u selektivnosti - tada se prednost daje jednom ili drugom adsorbentu koji je prikladniji za ovaj konkretni zadatak. Na primjer, glinica pruža veću selektivnost u odvajanju određenih policikličkih aromatičnih ugljovodonika.
Prednost se obično daje silika gelu u odnosu na glinicu zbog šireg izbora silika gela u smislu poroznosti, površine i prečnika pora, kao i značajno veće katalitičke aktivnosti glinice, što često dovodi do izobličenja rezultata analize. zbog razgradnje komponenti uzorka ili njihove nepovratne hemisorpcije.
2.1.2 Nedostaci adsorpcione hromatografije koji ograničavaju njenu upotrebu
Popularnost adsorpcione hromatografije postepeno je opadala kako se HPLC metoda razvijala, sve više se zamenjuje i nastavlja da je zamenjuju druge opcije, kao što su HPLC reverzne faze i normalne faze na sorbentima vezanih faza. Koji su nedostaci adsorpcione hromatografije doveli do toga?
Prije svega, to je dugo trajanje procesa balansiranja adsorbenata sa rastvaračima koji sadrže vodu u tragovima, teškoća pripreme takvih otapala sa određenim i ponovljivim sadržajem vlage. Ovo rezultira slabom ponovljivošću parametara zadržavanja, rezolucije i selektivnosti. Iz istog razloga, nemoguće je koristiti gradijent elucije – povratak u početno stanje je toliko dug da značajno premašuje dobitak u vremenu zbog upotrebe gradijenta.
Značajni nedostaci adsorbenata, posebno aluminijum oksida, povezani sa čestim preuređivanjem jedinjenja osetljivih na katalizu, njihovom razgradnjom, ireverzibilnom sorpcijom, takođe su dobro poznati i više puta su zabeleženi u literaturi. Nepovratno adsorbirajuće tvari, nakupljajući se u početnom dijelu kolone, mijenjaju prirodu sorbenta, mogu dovesti do povećanja otpora kolone ili čak do njenog potpunog začepljenja. Posljednji nedostatak se može otkloniti korištenjem predkolone, koja na- kako se otpornost i začepljenje povećavaju, zamjenjuje se novim * ili se ponovno puni novim sorbentom. Međutim, ireverzibilna sorpcija, koja se također odvija u ovom slučaju, dovodi do hromatograma u kojem komponente uzorka osjetljive na sorpciju ili katalitičku razgradnju potpuno ili djelimično odsutne.
2.2. DISTRIBUCIJSKA HROMATOGRAFIJA
Particiona hromatografija je varijanta HPLC u kojoj se razdvajanje smeše na komponente vrši zbog razlike u njihovim koeficijentima raspodele između dve nemešljive faze: otapala (mobilna faza) i faze na sorbentu (stacionarna faza). Istorijski, prvi su bili sorbenti ovog tipa, koji su se dobijali nanošenjem tečnih faza (oksidipropionitrila, parafinskog ulja, itd.) na porozne nosače, slično kao što su se pripremali i pripremali sorbenti za gasno-tečnu hromatografiju (GLC). Međutim, odmah su se otkrili nedostaci takvih sorbenata, od kojih je glavni bio relativno brzo ispiranje faze s nosača. Zbog toga se količina faze u koloni postepeno smanjivala, smanjivala su se i vremena zadržavanja, a u početnom dijelu kolone pojavili su se adsorpcijski centri koji nisu pokriveni fazom, što je uzrokovalo formiranje vršnih repova. Ovaj nedostatak je prevaziđen zasićenjem rastvarača podržanom fazom čak i prije nego što je ušao u kolonu. Prenos se takođe smanjio kada su korišćene viskoznije i manje rastvorljive polimerne faze, međutim, u ovom slučaju, zbog teškoće difuzije iz debelih polimernih filmova, efikasnost kolona je značajno smanjena.
Ispostavilo se da je logično tečnu fazu kalemiti na nosač hemijskim vezama na način da njeno uvlačenje postane fizički nemoguće, odnosno pretvoriti nosač i fazu u jedinstvenu cjelinu - u tzv. sorbent.
U budućnosti su napori istraživača bili usmjereni na potragu za reagensima čije bi kalemljenje išlo prilično brzo i potpuno, a nastale veze bile što stabilnije. Ovi reagensi su bili alkilhlorosilani i njihovi derivati, što je omogućilo dobijanje sorbenata u graft-fazi različitih tipova i sa različitim polarnim i nepolarnim grupama na površini pomoću slične tehnologije.
Uspješno korištenje ove druge vrste sorbenata za HPLC doprinijelo je rastu njihove proizvodnje od strane raznih proizvođača. Svaka kompanija proizvodi takve sorbente, po pravilu, na bazi svoje vrste silika gela i po sopstvenoj tehnologiji, što obično predstavlja „know-how” proizvodnje. Kao rezultat toga, veliki broj sorbenata koji su hemijski nazvani potpuno istim (na primjer, silika gel sa cijepljenim oktadecilsilanom) imaju vrlo različite hromatografske karakteristike. To je zbog činjenice da silika gel može imati šire ili uže pore, različitu površinu, poroznost, njegova površina prije cijepljenja može biti hidroksilirana ili ne, mono-, di- ili triklorosilani se mogu cijepiti, uvjeti cijepljenja mogu dati monomerne, polimerne ili sloj mješovite faze, koriste se različite metode uklanjanja rezidualnih reagensa, dodatna deaktivacija silanola i drugih aktivnih grupa može se koristiti, ali i ne mora.
Složenost tehnologije cijepljenja reagensa i pripreme sirovina i materijala, njena višestepena priroda dovode do toga da čak i serije sorbenata dobivene istom tehnologijom od istog proizvođača mogu imati neznatno različite hromatografske karakteristike. Ovo posebno vrijedi za one slučajeve kada se takvi sorbenti koriste za analizu višekomponentnih smjesa koje sadrže tvari koje se značajno razlikuju po broju i položaju funkcionalnih grupa, te po vrsti funkcionalnosti.
S obzirom na navedeno, uvijek treba težiti * da se pri korištenju metode analize koja je opisana u literaturi koristi potpuno isti sorbent i isti radni uvjeti. U ovom slučaju, vjerovatnoća da se djelo ne može reproducirati je minimalna. Ako to nije moguće, a uzima se sorbent druge kompanije sa sličnom vezanom fazom, morate biti spremni na činjenicu da će biti potreban dugotrajan rad na preradi tehnike. Istovremeno, postoji mogućnost (i to treba uzeti u obzir) da se na ovom sorbentu ne može postići potrebna separacija ni nakon dužeg razvoja. Prisutnost u literaturi mnogih opisanih postupaka separacije na dugo proizvedenim starim sorbentima stimulira njihovu daljnju proizvodnju i korištenje iz tog razloga. Međutim, u onim slučajevima kada je potrebno pristupiti razvoju originalnih metoda, posebno u odnosu na tvari sklone razgradnji, hemisorpciji i preuređivanju, preporučljivo je početi raditi na sorbentima koji su nedavno razvijeni i proizvedeni od strane novih , poboljšane verzije tehnologije. Novi sorbenti imaju ujednačeniji frakcijski sastav, ujednačeniju i potpuniju pokrivenost površine vezanom fazom i naprednije završne faze obrade sorbenta.
2.3. HROMATOGRAFIJA IONSKIH IZMJENA
U ionsko-izmjenjivačkoj hromatografiji, razdvajanje komponenti smjese postiže se reverzibilnom interakcijom ionizirajućih supstanci sa jonskim grupama sorbenta. Očuvanje električne neutralnosti sorbenta osigurava prisustvo protujona sposobnih za ionsku izmjenu koji se nalaze u neposrednoj blizini površine. Jon unesenog uzorka, u interakciji sa fiksnim nabojem sorbenta, zamjenjuje se sa protujonom. Supstance koje imaju različite afinitete prema fiksnim nabojima odvajaju se na anjonskim izmjenjivačima ili na kationskim izmjenjivačima. Anionski izmjenjivači imaju pozitivno nabijene grupe na površini i sorbiraju anjone iz mobilne faze.Kationski izmjenjivači, odnosno, sadrže grupe sa -negativnim nabojem koje stupaju u interakciju sa katjonima .
Kao mobilna faza koriste se vodeni rastvori soli kiselina, baza i rastvarača kao što je tečni amonijak, odnosno sistemi rastvarača sa visokom dielektričnom konstantom e i velikom tendencijom jonizacije jedinjenja. Obično rade sa puferskim rastvorima koji omogućavaju podešavanje pH vrijednost.
Tokom hromatografskog odvajanja, joni analita se takmiče sa ionima sadržanim u eluentu, tražeći interakciju sa suprotno naelektrisanim grupama sorbenta. Iz toga slijedi da se hromatografija ionske izmjene može koristiti za odvajanje bilo kojeg spoja koji se može ionizirati na bilo koji način. Moguće je analizirati čak i neutralne molekule šećera u obliku njihovih kompleksa s boratnim ionom:
Šećer + IN 3 2 - \u003d Šećer - IN 3 2 -.
Jono-izmjenjivačka hromatografija je neophodna za odvajanje visoko polarnih supstanci, koje se ne mogu analizirati GLC-om bez konverzije u derivate. Ova jedinjenja uključuju aminokiseline, peptide, šećere.
Jonoizmenjivačka hromatografija ima široku primenu u medicini, biologiji, biohemiji, za kontrolu životne sredine, u analizi sadržaja lekova i njihovih metabolita u krvi i urinu, pesticida u prehrambenim sirovinama, kao i za odvajanje anorganskih jedinjenja, uključujući radioizotope, lantanoide, aktinide itd. Analiza biopolimera (proteina, nukleinskih kiselina, itd.), koja je obično trajala satima ili danima, pomoću jonoizmenjivačke hromatografije vrši se za 20-40 minuta uz bolje odvajanje. Upotreba ionsko-izmjenjivačke hromatografije u biologiji omogućila je direktno promatranje uzoraka u biološkim medijima, smanjujući mogućnost preuređivanja ili izomerizacije, što može dovesti do pogrešnog tumačenja konačnog rezultata. Zanimljivo je koristiti ovu metodu za kontrolu promjena u biološkim tekućinama. Upotreba slabih anionskih izmjenjivača na bazi poroznog silika-gela omogućila je odvajanje peptida. V
Mehanizam jonske razmene može se predstaviti kao sledeće jednačine:
za anionsku izmjenu
X-+R+Y- h ->■ Y-+R+X-.
za kationsku izmjenu |
X++ + R-Y+ h=* Y++R-X+.
U prvom slučaju, ion uzorka X~ se takmiči sa jonom mobilne faze Y~ za ionske centre R+ jonskog izmjenjivača, au drugom slučaju kationi uzorka X+ se takmiče s ionima mobilne faze Y+ za ionske centrira R~.
Naravno, joni uzorka koji slabo stupaju u interakciju sa ionskim izmjenjivačem slabo će se zadržati na koloni tokom ovog takmičenja i prvi će biti isprani iz nje, i obrnuto, jače zadržani joni će biti posljednji koji će eluirati iz kolone. Obično, BTqpH4Hbie interakcije nejonske prirode nastaju zbog adsorpcije ili vodonične veze uzorka sa nejonskim dijelom matrice ili zbog ograničene rastvorljivosti uzorka u mobilnoj fazi. Teško je razlikovati "klasičnu" hromatografiju s ionskom izmjenom u njenom "čistom" obliku, te stoga neki hromatografi polaze od empirijskih, a ne teorijskih obrazaca u hromatografiji s ionskom izmjenom.
Odvajanje specifičnih supstanci prvenstveno zavisi od izbora najpogodnijeg sorbenta i mobilne faze. Kao stacionarne faze u jono-izmjenjivačkoj hromatografiji koriste se jono-izmjenjivačke smole i silika gelovi sa cijepljenim ionogenim grupama.
2.4. HROMATOGRAFIJA VELIČINA
Isključujuća hromatografija je opcija! tečna hromatografija, u kojoj dolazi do razdvajanja zbog raspodjele molekula između otapala unutar pora sorbenta i otapala koji teče " između njegovih čestica.
Za razliku od drugih HPLC opcija, gdje je odvajanje ide zbog različite interakcije komponenata s površinom sorbenta, uloga čvrstog punila u hromatografiji isključenja veličine sastoji se samo u formiranju pora određene veličine, a stacionarna faza je otapalo koje ispunjava ove pore. Stoga je upotreba izraza "sorbent" za ova punila donekle uvjetna.
Osnovna karakteristika metode je mogućnost odvajanja molekula prema njihovoj veličini u rastvoru u rasponu gotovo bilo koje molekulske mase - od 10 2 do 10 8 , što je čini nezamenljivom za proučavanje sintetičkih i biopolimera.
Tradicionalno, proces koji se izvodi u organskim rastvaračima se i dalje često naziva gel permeaciona hromatografija, a u vodenim sistemima gel filtraciona hromatografija. U ovoj knjizi, za obje opcije, usvojen je jedan termin, koji dolazi od engleskog "Size Exclusion" - izuzetak po veličini - i najpotpunije odražava mehanizam procesa.
Detaljna analiza postojećih ideja o vrlo složenoj teoriji procesa ekskluzione hromatografije po veličini izvedena je u monografijama.
Ukupna zapremina rastvarača u koloni Vt (često se naziva ukupnim volumenom kolone, jer Vd ne učestvuje u hromatografskom procesu) je zbir zapremina pokretne i stacionarne faze.
Zadržavanje molekula u okluzivnom stupcu određeno je vjerovatnoćom njihove difuzije u pore i ovisi o odnosu veličina molekula i pora, što je shematski prikazano na Sl. 2.15. Koeficijent distribucije ka, kao iu drugim varijantama kromatografije, to je omjer koncentracija tvari u stacionarnoj i pokretnoj fazi.
Pošto mobilna i stacionarna faza imaju isti sastav, onda kd supstanca, kojoj su obje faze podjednako dostupne, jednaka je jedinici. Ova situacija se ostvaruje za molekule C najmanjih veličina (uključujući molekule rastvarača), koji prodiru u sve pore (vidi sliku 2.15) i stoga se najsporije kreću kroz kolonu. Njihova zadržana zapremina jednaka je ukupnoj zapremini rastvarača Vt-
 Rice. 2.15. Model razdvajanja molekula mjerom u hromatografiji isključenja veličine
Rice. 2.15. Model razdvajanja molekula mjerom u hromatografiji isključenja veličine
Sve molekule veće od veličine pora sorbenta ne mogu ući u njih (potpuno isključenje) i proći kroz kanale između čestica. Oni eluiraju iz kolone sa istim retencijskim volumenom koji je jednak volumenu mobilne faze V 0 - Koeficijent raspodjele za ove molekule je nula.
Molekuli srednje veličine, sposobni da prodru samo u neke od pora, zadržavaju se u koloni u skladu sa svojom veličinom. Koeficijent distribucije ovih molekula varira od nule do jedan i karakteriše udio volumena pora koji je dostupan za molekule date veličine.Njihov zadržani volumen je određen zbirom Y o i dostupnog dijela zapremine pora.
KVALITATIVNA ANALIZA
Kromatograf koji počinje da radi u oblasti tečne hromatografije visokih performansi treba da bude upoznat sa osnovama kvalitativne analize. Kvalitativna analiza se koristi za identifikaciju poznatog proizvoda dobijenog na nov način ili pomiješanog s drugim proizvodima. Neki medicinski hemijski proizvodi i njihovi metaboliti u bioml.terijalima... „. „Upoznavanje sa osnovama kvalitativne“ analize pomoći će da se izbjegne uobičajeno greške, na primjer / razlikovati nečistoće u uzorku od nečistoća u otapalu ili provjeriti čistoću tvari na više od jednog spektrofotometra valne dužine, ali na različitim, itd.
Prije nastavka analize potrebno je utvrditi da li je cijeli uzorak eluiran iz kolone ovim sistemom rastvarača ili ne. Da bi se osiguralo potpuno eluiranje, potrebno je sakupiti svu tekućinu koja teče iz kolone, ispariti rastvarač, izvagati ostatak i pronaći oporavak uzorka.
Identifikacija komponenti u HPLC-u može se izvršiti na tri načina: 1) korišćenje informacija o zadržavanju; 2) istražuje zone dobijene odvajanjem u koloni tečnog hromatografa korišćenjem metoda spektralne ili hemijske analize; 3) direktno povezati analizator spektra na kolonu.
Retencijski volumen se koristi za registraciju pikova u hromatografiji V R ili vrijeme čekanja t R. Obe vrednosti su karakteristika supstance u datom hromatografskom sistemu. Budući da se vrijeme zadržavanja supstance koja se odvaja sastoji od vremena interakcije u koloni i vremena prolaska kroz prazne dijelove cijevi, ono varira od instrumenta do instrumenta. Zgodno je imati supstancu koju ova kolona ne zadržava, uzimajući je kao standard, čije vrijeme zadržavanja i volumen t 0 , V o. Hromatografija supstance i standarda se mora izvesti pod istim uslovima (pritisak i brzina protoka). U identifikaciji po retencijskim podacima, poznate pojedinačne supstance koje mogu biti prisutne u uzorcima se odvajaju u istom hromatografskom sistemu i za njih se dobijaju vrednosti. t R. Upoređujući ove vrijednosti t R s vremenom zadržavanja nepoznatog pika, može se otkriti da se oni ili poklapaju, u kom slučaju pikovi vjerovatno odgovaraju istoj tvari, ili t R poznata supstanca ne odgovara t R nepoznata zona. Tada je još moguće procijeniti vrijednosti t R supstance koje nisu dostupne za direktno merenje njihovog zadržavanja. Hajde da razmotrimo obe opcije.
U prvom slučaju, očigledno, potrebno je preliminarno proučavanje uzorka da bi se pretpostavilo prisustvo specifičnih supstanci u njemu. Kada se radi sa jednostavnim smjesama, lako je odrediti da li se stepen zadržavanja zona uzorka i poznatih supstanci poklapa ili ne, tj. t B su isti ili različiti. U slučaju složenih smjesa, nekoliko supstanci se može eluirati sa sličnim vrijednostima odjednom. t R, a zone koje su stvarno dobijene hromatografskim odvajanjem se preklapaju. Kao rezultat, dobijanje tačnih vrednosti t R za različite zone postaje nemoguće. Pouzdanost identifikacije se povećava sa povećanjem rezolucije, pažljivijom kontrolom uslova razdvajanja, ponovnim merenjem vrednosti t R i usrednjavanje pronađenih vrednosti. U tom slučaju, hromatografsko razdvajanje poznatih i nepoznatih supstanci trebalo bi da se izmjenjuje. Prilikom odvajanja složenih smjesa, vrijednost t R supstance se mogu menjati pod uticajem matrice samog uzorka. Takav efekat je moguć na početku hromatograma i kada se pikovi preklapaju; zonsko zatezanje je takođe moguće, kao što je već pomenuto.
U takvim slučajevima uzorku treba dodati standard u omjeru 1: 1. Ako su tvari identične, vrijednost t R početni materijal se ne mijenja, a na kromatogramu se dobija samo jedan pik. Ako postoji uređaj sa cikličkim hromatografskim sistemom, onda je za pouzdanu identifikaciju poželjno da se smeša prođe kroz kolonu nekoliko puta.
Podaci o stepenu zadržavanja mogu se naći i u literaturi, ali je vrijednost ovih informacija ograničena. Budući da stupci čak i jedne serije daju lošu ponovljivost, književne vrijednosti ne odgovaraju uvijek pravoj vrijednosti. t R na ovoj koloni. Za adsorpcionu hromatografiju, međutim, moguće je predvidjeti t R na osnovu podataka iz literature. Još jedna poteškoća povezana s upotrebom književnih značenja t R, - poteškoće u pronalaženju u stručnoj literaturi, iako bibliografski pregledi objavljeni u Journal of Chromatography imaju ažurirani indeks vrsta supstanci.
U drugom slučaju, kada se vremena zadržavanja poznatih spojeva i zona uzorka ne poklapaju, moguće je predvidjeti vrijeme zadržavanja nepoznate komponente. Predviđanja relativnog zadržavanja zasnovana na podacima o strukturi u 3D hromatografiji su prilično pouzdana. Oni su manje precizni u adsorpciji, particionoj hromatografiji, a posebno kada se radi na hemijski vezanoj fazi. Za ionsku i jonsko-parnu hromatografiju supstanci sa poznatim p Ka moguće su samo približne vrijednosti tR. Uvijek je lakše predvidjeti relativno zadržavanje ili *x vrijednost nego apsolutne vrijednosti. k". Relativne vrijednosti t R lakše procijeniti za srodne spojeve ili derivate, kao što su supstituirane alkil karboksilne kiseline ili derivati benzena.
Kod izokratskog odvajanja homologa ili oligomera, ponekad se opaža sljedeći obrazac:
\ gk" = A + bn,
gdje ALI i AT- konstante za veći broj odabranih uzoraka i za dati hromatografski sistem (na istoj koloni, sa istim mobilnim i stacionarnim fazama); P je broj identičnih strukturnih jedinica u molekuli uzorka.
Uvođenje funkcionalne grupe / u molekulu uzorka će dovesti do promjene k" u prvoj jednačini nekim konstantnim koeficijentom a/ u datom hromatografskom sistemu. Moguće je dobiti grupne konstante a/ za različite supstituentske grupe /, čije će se vrijednosti povećavati sa povećanjem polariteta funkcionalnih grupa u svim vrstama hromatografije, osim obrnute faze, gdje će se vrijednosti konstanti smanjivati sa povećanjem polariteta.
Neke grupne konstante a/ za različite grupe supstituenata / date su u tabeli. 9.1.
U adsorpcijskoj hromatografiji, prva jednadžba nije uvijek primjenjiva, jer vrijedi pod uvjetom da svi izomeri imaju istu vrijednost k", što se ne poštuje uvek. Moguće je, međutim, nacrtati lgfe" istih jedinjenja na jednoj koloni naspram lgfe" istih jedinjenja na drugoj koloni, ili naspram odgovarajućih karakteristika u tankoslojnoj hromatografiji, na primer, lg[(l- RF) IRf].
Kada upoređujete podatke o zadržavanju, možete koristiti vrijednosti faktora kapacitivnosti k", jer na njemu, za razliku od t R ne utiču na brzinu pokretne faze i geometrijske karakteristike stuba.
Odvajanje na kemijski vezanoj fazi slično je razdvajanju particionom hromatografijom sa sličnim fazama, pa se stoga podaci ekstrakcije u ravnoteži mogu koristiti za predviđanje vremena zadržavanja.
U jonoizmenjivačkoj hromatografiji na retenciju utiču tri faktora: stepen ionizacije kiselina i baza, naelektrisanje jonizovane molekule i sposobnost supstance iz vodene mobilne faze koja se koristi u hromatografiji za izmjenu jona da migrira u organsku fazu. . Ovo posljednje ovisi o molekularnoj težini spoja i njegovoj hidrofobnosti. Stoga se jače kiseline ili baze jače zadržavaju u separaciji izmjene anjona ili katjona. Sa smanjenjem RK a pojedinačne kiseline uključene u uzorak, zadržavanje se povećava prilikom odvajanja većeg broja kiselina zbog izmjene anjona, a povećanjem p / C o povećava se zadržavanje baza prilikom njihovog odvajanja zbog kationske izmjene.
Dakle, podudarnost vrijednosti vremena zadržavanja poznate tvari s promatranom omogućuje pretpostaviti njihov identitet. Pouzdanost identifikacije se povećava ako se hromatogrami poznate supstance i nepoznate komponente uporede pod različitim uslovima. Ako se tvari u hromatografiji adsorpcije i reverzne faze ili ionske izmjene i hromatografije isključivanja po veličini ponašaju na isti način, povećava se pouzdanost identifikacije. Ako je pouzdanost identifikacije sa jednakim relativnim zadržavanjem 90%, onda kada se proučava ponašanje istih supstanci u uslovima koji se značajno razlikuju, pouzdanost identifikacije je već 99%.
Vrijedna karakteristika tvari koja se koristi u identifikaciji je omjer signala dobijenih za datu supstancu na dva različita detektora. Nakon napuštanja kolone, analit prvo prolazi kroz prvi detektor, zatim kroz drugi, a signali koji dolaze iz detektora se istovremeno snimaju pomoću multi-pen rekordera ili na dva rekordera. Obično se koristi serijska veza ultraljubičastog detektora (osjetljivijeg, ali selektivnog) sa refraktometrom, ili ultraljubičastog sa fluorescentnim detektorom, ili dva ultraljubičasta detektora koja rade na različitim talasnim dužinama. Relativni odziv, tj. odnos signala refraktometra i signala fotometra, je karakteristika supstance, pod uslovom da oba detektora rade u svom linearnom opsegu; ovo se potvrđuje uvođenjem različitih količina iste supstance. Kvalitativne informacije se mogu dobiti radom na fotometrijskim detektorima opremljenim uređajem za zaustavljanje protoka i koji vam omogućavaju da snimite spektar vrha koji napušta kolonu dok je u protočnoj ćeliji, upoređujući ga sa spektrom poznatog jedinjenja.
Od velikog interesa za identifikaciju su moderni, ali skupi spektrofotometri sa nizom dioda.
Potpuno nepoznata supstanca se ne može identifikovati samo tečnom hromatografijom visokih performansi, potrebne su druge metode.
KVANTITATIVNA ANALIZA
Kvantitativna tečna hromatografija je dobro razvijena analitička metoda koja po preciznosti nije inferiorna od kvantitativne gasne hromatografije i značajno nadmašuje tačnost TLC ili elektroforeze. Nažalost, u HPLC-u ne postoji detektor koji bi imao sličnu osetljivost za jedinjenja različite hemijske strukture ( kao katarometar u Stoga je potrebna kalibracija instrumenta da bi se dobili kvantitativni rezultati.
Kvantitativna analiza se sastoji od sledećih koraka: 1) hromatografsko odvajanje; 2) merenje vršnih površina ili visina; 3) proračun kvantitativnog sastava smeše na osnovu hromatografskih podataka; 4) interpretacija dobijenih rezultata, odnosno statistička obrada. Hajde da razmotrimo sve ove faze.
4.1. HROMATOGRAFSKO ODJELJAVANJE
Tokom uzorkovanja mogu se napraviti greške. Posebno je važno izbjeći greške i uzeti adekvatan reprezentativan uzorak heterogenih čvrstih uzoraka, visoko hlapljivih ili nestabilnih supstanci, poljoprivrednih proizvoda i biomaterijala. Nehomogeni uzorci, kao što su namirnice, temeljito se miješaju i razrežu na četvrtine. Izvođenjem ove operacije uzastopno, postiže se homogenost uzorka.
Greške i gubici supstanci mogu se dozvoliti u fazi ekstrakcije, izolacije, prečišćavanja itd.
Uzorci moraju biti potpuno rastvoreni i njihovi rastvori pripremljeni sa tačnošću od ±0,1%. Poželjno je da se uzorak otopi u mobilnoj fazi, što će isključiti mogućnost njegovog taloženja nakon unošenja u hromatograf. Ako otapanje u mobilnoj fazi nije moguće, onda treba koristiti rastvarač koji se može mešati sa njim i ubrizgati zapremine uzorka (manje od 25 µl) u hromatograf.
Tokom ubrizgavanja uzorka mogu se pojaviti značajne greške zbog frakcioniranja, curenja i vršnog razmazivanja. Razmazivanje vrhova uzrokuje formiranje repova, što dovodi do djelomičnog preklapanja vrhova i, kao posljedicu, do grešaka u detekciji. Uređaji sa ventilom petlje su poželjniji u odnosu na špriceve za ubrizgavanje uzorka u kvantitaciji zbog veće preciznosti i manje zavisnosti od operatera.
Kod hromatografskog odvajanja supstanci mogu nastati i komplikacije koje dovode do izobličenja podataka: kvantitativna analiza. Moguća razgradnja ili transformacija uzorka tokom hromatografskog procesa ili ireverzibilna adsorpcija supstance na ovoj koloni. Važno je osigurati da ove nepoželjne pojave ne postoje i, ako je potrebno, regenerirati stupac ili ga zamijeniti. Preklapanje pikova i zaostatak se takođe mogu smanjiti promenom uslova hromatografije.
Vrhovi koji su lažni ili nejasnog oblika, ili vrhovi čije je vrijeme oslobađanja blizu to, jer možda neće biti dovoljno segregacije. Obično se koriste pikovi sa vrijednošću d" > 0,5. Najveća efikasnost kolone postiže se uvođenjem 10~5 -10~6 g otopljene tvari po 1 g sorbenta. Prilikom unošenja velikih količina uzorka, zavisnost od visina vrha pri opterećenju može se pokazati nelinearnom i potrebna je kvantitativna procjena prema površini vrha.
Greške povezane sa detekcijom ili amplifikacijom dovode do značajnog izobličenja rezultata hromatografskog odvajanja. Svaki detektor karakterizira specifičnost, linearnost i osjetljivost. Posebno je važno provjeriti selektivnost u analizi mikronečistoća. Reakcija UV detektora može se promijeniti na supstance sa sličnim funkcionalnim grupama za faktor 104. Potrebno je kalibrirati odziv detektora za svaki analit. Naravno, supstance koje ne apsorbuju u UV području neće dati signal rekorderu kada se koristi kao detektor fotometra. Kada koristite refraktometar, mogu se pojaviti negativni pikovi. Osim toga, ovaj detektor mora biti termostatiran, što nije potrebno za UV detektor.
Linearnost detektora određuje veličinu ubrizganog uzorka. Mora se imati na umu da brzina protoka kroz kolonu, temperatura kolone i detektora i njegov dizajn utiču na tačnost kvantitativne analize. Greške u prijenosu električnog signala na izlazni uređaj (snimač), integrator ili računar mogu nastati zbog podizanja šuma, nedostatka uzemljenja, fluktuacija napona u mreži itd.
 4.2. MERENJE POVRŠINE ILI VISINE VRHOVA
4.2. MERENJE POVRŠINE ILI VISINE VRHOVA
visina vrha h (Sl. 10.1) nazovite udaljenost od vrha vrha do osnovne linije, ona se mjeri linearno ili se broj podjela na snimaču. Neki elektronski integratori i računari daju informacije o vršnoj visini. Položaj osnovne linije pomaknutih vrhova nalazi se interpolacijom ordinatnih vrijednosti koje odgovaraju početku i kraju vrha (vrh 1 i 3 vidi sl. 10.1). Da bi se poboljšala tačnost, potrebno je imati ravnu, stabilnu osnovnu liniju. U slučaju nerazdvojenih vrhova, osnovna linija se povlači između početka i kraja vrha i ne zamjenjuje se nultom linijom. Budući da visina vrha manje ovisi o utjecaju susjednih vrhova koji se preklapaju, procjena visine vrha je preciznija i skoro uvijek se koristi u analizi tragova.
Područje vrha može se odrediti na različite načine. Hajde da razmotrimo neke od njih.
1. Planimetrijska metoda se sastoji u tome da se vrh prati ručnim planimetrom, koji je uređaj koji mehanički određuje površinu vrha. Metoda je precizna, ali naporna i slabo ponovljiva. Ova metoda se ne preporučuje.
2. Metoda papirne siluete - vrh se izrezuje i vaga. Metoda je dobro ponovljiva, ali naporna, a kromatogram je uništen. Njegova primjena ovisi o homogenosti trake grafikona. Metoda se također ne može široko preporučiti.
4. Metoda triangulacije se sastoji u konstruisanju trougla povlačenjem tangenti na strane vrha. Vrh trougla je viši od vrha vrha. Povećanje površine formirane ovim proširenim vrhom će biti konzistentno kroz hromatogram i neće previše uticati na tačnost. Osim toga, neka površina izgubljena prilikom crtanja tangenti će biti nadoknađena. Osnova trokuta određena je presjekom tangenti sa baznom linijom, a površina je određena umnoškom 7g osnove na visinu. Za određivanje površina asimetričnih vrhova ova metoda je najbolja. Međutim, ponovljivost u konstrukciji tangenta od strane različitih operatera je različita i stoga; nisko.
5. Metoda integratora diska zasnovana je na elektromehaničkom držaču pričvršćenom na diktafon. Olovka pričvršćena na integrator kreće se duž trake na dnu trake brzinom proporcionalnom kretanju olovke diktafona.
Kao i kod ručnih mjerenja, pik bi trebao ostati na skali rekordera, međutim prilagođavanja radi kompenzacije pomaka osnovne linije i nepotpunog odvajanja susjednih vrhova smanjuju pouzdanost i povećavaju vrijeme analize.
Metoda je preciznija od ručnih metoda mjerenja, posebno s asimetričnim vrhovima, i nudi prednost u brzini. Osim toga, obezbjeđuje trajni kvantitativni zapis analize.
6. Metode koje koriste elektronske integratore koji određuju površinu pikova i štampaju informacije o ovoj oblasti i vremenima zadržavanja, mogu uključiti korekciju za pomak osnovne linije i određivanje površine samo djelimično odvojenih pikova. Glavne prednosti su tačnost, brzina, neovisnost djelovanja od rada diktafona. Integratori imaju memoriju i mogu se programirati za specifičnu analizu pomoću prethodno učitanog programa. Prednosti integratora uključuju njegovu sposobnost da koristi faktore korekcije za odziv detektora prilikom ponovnog izračunavanja početnih podataka o površinama pikova, kompenzirajući razliku u osjetljivosti detektora na različite supstance. Takvi sistemi štede vrijeme, poboljšavaju analitičku tačnost i korisni su za rutinsku analitičku analizu.
7. Računari koji mjere vršne površine se široko koriste u tečnoj hromatografiji. Oni štampaju kompletnu poruku, uključujući nazive supstanci, oblasti pikova, vremena zadržavanja, faktore korekcije odziva detektora i sadržaj (u težinskim %) za različite komponente uzorka.

OPĆE FARMAKOPSKO OVLAŠĆENJE
Umjesto čl. GF XI
Tekuća hromatografija visokih performansi (tečna hromatografija visokog pritiska) je metoda kolonske hromatografije u kojoj je mobilna faza tečnost koja se kreće kroz hromatografsku kolonu ispunjenu stacionarnom fazom (sorbentom). Kolone za tečnu hromatografiju visokih performansi karakteriše visok hidraulični otpor na ulazu.
U zavisnosti od mehanizma razdvajanja supstanci, razlikuju se sledeće varijante tečne hromatografije visokih performansi: adsorpciona, particiona, jono-izmjenjivačka, isključujuća, kiralna itd., u skladu sa prirodom glavnih manifestiranih međumolekularnih interakcija. U adsorpcijskoj kromatografiji do razdvajanja tvari dolazi zbog njihove različite sposobnosti da se adsorbiraju i desorbiraju s površine sorbenta s razvijenom površinom, na primjer, silika gela. U particionoj tečnoj hromatografiji visokih performansi, do razdvajanja dolazi zbog razlike u koeficijentima distribucije supstanci koje se odvajaju između stacionarne (po pravilu, hemijski kalemljene na površinu stacionarnog nosača) i mobilne faze.
U zavisnosti od vrste mobilne i stacionarne faze, razlikuje se hromatografija normalne faze i hromatografija obrnute faze. U tečnoj hromatografiji visokih performansi normalne faze, stacionarna faza je polarna (najčešće silika gel ili silika gel sa cijepljenim NH 2 - ili CN grupama, itd.), a mobilna faza je nepolarna (heksan ili mješavine heksan sa polarnijim organskim rastvaračima - hloroformom, alkoholima itd.). Zadržavanje tvari se povećava sa povećanjem polariteta. U hromatografiji normalne faze, moć eluiranja mobilne faze raste sa povećanjem polariteta.
U hromatografiji reverzne faze, stacionarna faza je nepolarna (hidrofobni silika gelovi sa kalemljenim C4, C8, C18 grupama, itd.); mobilna faza je polarna (mješavine vode i polarnih rastvarača: acetonitril, metanol, tetrahidrofuran itd.). Zadržavanje tvari se povećava s povećanjem njihove hidrofobnosti (nepolarnost). Što je veći sadržaj organskog rastvarača, veća je moć eluiranja mobilne faze.
U jonoizmenjivačkoj hromatografiji, molekule supstanci smeše, disocirane u rastvoru na katione i anjone, odvajaju se pri kretanju kroz sorbent (kationski izmenjivač ili anjonski izmenjivač) zbog različite jačine interakcije jona koji se žele. određena ionskim grupama sorbenta.
U hromatografiji bez veličine (sito, gel-penetrirajuća, gel-filtracijska) hromatografija, molekule tvari su razdvojene po veličini zbog njihove različite sposobnosti da prodiru u pore stacionarne faze. U ovom slučaju, najveći molekuli koji mogu prodrijeti u minimalni broj pora stacionarne faze prvi napuštaju kolonu, a tvari male molekularne veličine posljednje napuštaju.
U kiralnoj hromatografiji, optički aktivni spojevi se razdvajaju na pojedinačne enantiomere. Odvajanje se može izvesti na kiralnim stacionarnim fazama ili na akiralnim stacionarnim fazama koristeći kiralne mobilne faze.
Postoje i druge opcije za tečnu hromatografiju visokih performansi.
često se razdvajanje odvija ne jednim, već nekoliko mehanizama istovremeno, ovisno o vrsti pokretne i stacionarne faze, kao i o prirodi spoja koji se utvrđuje.
Područje primjene
Tečna hromatografija visokih performansi uspešno se koristi i za kvalitativnu i za kvantitativnu analizu lekova u testovima "Identitet", "Strane nečistoće", "Rastapanje", "Ujednačenost doziranja", "Kvantitativno određivanje". Treba napomenuti da vam kromatografija omogućava kombiniranje nekoliko testova u jednom uzorku, uključujući "Identitet" i "Kvantitativno određivanje".
Oprema
Za analizu se koriste odgovarajući instrumenti - tečni hromatografi.
Sastav tečnog hromatografa obično uključuje sljedeće glavne komponente:
- jedinica za pripremu mobilne faze, koja uključuje posudu sa mobilnom fazom (ili kontejnere sa pojedinačnim rastvaračima koji su deo mobilne faze) i sistem za otplinjavanje mobilne faze;
— pumpni sistem;
– pokretni mikser faza (po potrebi);
– sistem za ubrizgavanje uzorka (injektor), može biti ručni ili automatski (autosampler);
— hromatografska kolona (može se ugraditi u termostat);
— detektor (jedan ili više sa različitim metodama detekcije);
— sistem upravljanja hromatografom, prikupljanje i obrada podataka.
Pored toga, hromatograf može uključivati: sistem za pripremu uzorka i reaktor pred kolonu, sistem za prebacivanje kolone, reaktor nakon kolone i drugu opremu.
Sistem za pumpanje
Pumpe opskrbljuju mobilnu fazu koloni unaprijed određenom brzinom. Sastav mobilne faze i brzina protoka mogu biti konstantni ili se mijenjati tokom analize. U slučaju konstantnog sastava mobilne faze, proces se naziva izokratskim, au drugom - gradijentom. Moderan pumpni sistem tečnog hromatografa sastoji se od jedne ili više kompjuterski kontrolisanih pumpi. Ovo vam omogućava da promenite sastav mobilne faze prema specifičnom programu tokom gradijenta elucije. Analitičke pumpe za tečnu hromatografiju visokih performansi omogućavaju održavanje brzine protoka mobilne faze u koloni u rasponu od 0,1 do 10 ml/min pri ulaznom pritisku kolone do 40 MPa. Pulsacije pritiska su minimizirane posebnim sistemima prigušivača koji su uključeni u dizajn pumpi. Radni dijelovi pumpi izrađeni su od materijala otpornih na koroziju, što omogućava korištenje agresivnih komponenti u sastavu mobilne faze.
Slavine
U mikseru se formira jedna mobilna faza od pojedinačnih rastvarača dostavljenih pumpama, ako potrebna smeša nije unapred pripremljena. Mešanje komponenti mobilne faze u mešalici može se odvijati i pri niskom pritisku (pre pumpi) i pri visokom pritisku (posle pumpi). Mikser se može koristiti za pripremu mobilne faze i izokratsko eluiranje.
Zapremina miksera može uticati na vreme zadržavanja komponenti u eluciji gradijenta.
Injektori
Injektori mogu biti univerzalni, sa mogućnošću promjene volumena ubrizganog uzorka, ili diskretni za unošenje uzorka samo određene zapremine. Oba tipa injektora mogu biti automatska ("auto-injektori" ili "auto-sampleri"). Injektor uzorka (rastvor) nalazi se direktno ispred hromatografske kolone. Dizajn injektora omogućava promjenu smjera protoka mobilne faze i izvođenje prethodnog ubrizgavanja uzorka u dozirnu petlju određene zapremine (obično od 10 do 100 µl) ili u posebnu varijablu uređaj za doziranje zapremine. Volumen petlje je naznačen na njegovoj oznaci. Dizajn diskretnog injektora, u pravilu, omogućava zamjenu petlje. Moderni automatski injektori mogu imati niz dodatnih funkcija, na primjer, mogu služiti kao stanica za pripremu uzoraka: miješanje i razrjeđivanje uzoraka, te izvođenje reakcije derivatizacije prije kolone.
Kromatografska kolona
Kromatografske kolone su obično cijevi od nehrđajućeg čelika, stakla ili plastike napunjene sorbentom i zatvorene s obje strane filterima s promjerom pora od 2-5 µm. Dužina analitičke kolone može biti u rasponu od 5 do 60 cm ili više, unutrašnji prečnik je od 2 do 10 mm. Kolone sa unutrašnjim prečnikom manjim od 2 mm koriste se u mikrokolona hromatografiji. Postoje i kapilarni stubovi sa unutrašnjim prečnikom od oko 0,3-0,7 mm. Kolone za preparativnu hromatografiju mogu imati unutrašnji prečnik od 50 mm ili više.
Prije analitičke kolone mogu se ugraditi kratke kolone (predkolone) koje obavljaju različite pomoćne funkcije od kojih je glavna zaštita analitičke kolone. Obično se analiza izvodi na sobnoj temperaturi, međutim, kako bi se povećala efikasnost razdvajanja i smanjilo trajanje analize, može se koristiti termostatiranje kolona na temperaturama do 80–100 °C. Mogućnost korištenja povišene temperature tokom separacije ograničena je stabilnošću stacionarne faze, budući da je njeno uništavanje moguće na povišenim temperaturama.
Stacionarna faza (sorbent)
Uobičajeni sorbenti su:
- silika gel, aluminijev oksid, koriste se u hromatografiji normalne faze. Mehanizam zadržavanja u ovom slučaju je obično adsorpcija;
- silika gel, smole ili polimeri s cijepljenim kiselim ili baznim grupama. Obim - jonska izmjena i jonska hromatografija;
- silika gel ili polimeri sa datom distribucijom veličine pora (hromatografija isključivanja veličine);
- hemijski modifikovani sorbenti (bonded phase sorbenti), najčešće pripremljeni na bazi silika gela. Mehanizam zadržavanja je adsorpcija ili distribucija između mobilne i stacionarne faze. Obim zavisi od vrste kalemljenih funkcionalnih grupa. Neke vrste sorbenata mogu se koristiti i u hromatografiji obrnute i normalne faze;
- hemijski modifikovani hiralni sorbenti, na primer, derivati celuloze i amiloze, proteini i peptidi, ciklodekstrini, hitozani koji se koriste za odvajanje enantiomera (hiralna hromatografija).
Sorbenti vezane faze mogu imati različite stepene hemijske modifikacije. Najčešće korištene vezane faze su:
– oktadecil grupe (sorbent oktadecilsilan (ODS) ili C 18);
– oktilne grupe (sorbent oktilsilan ili C 8);
– fenilne grupe (fenilsilan sorbent);
– cijanopropil grupe (CN sorbent);
– aminopropilne grupe (NH 2 sorbent);
– diolne grupe (sorbent diol).
Najčešće se analiza izvodi na nepolarnim vezanim fazama u režimu obrnute faze korištenjem C 18 sorbenta.
Sorbenti vezane faze na bazi silika gela su hemijski stabilni na pH vrednostima od 2,0 do 7,0, osim ako proizvođač nije drugačije odredio. Čestice sorbenta mogu imati sferni ili nepravilan oblik i različitu poroznost. Veličina čestica sorbenta u analitičkoj tečnoj hromatografiji visokih performansi je obično 3-10 µm, u preparativnoj tečnoj hromatografiji visokih performansi je 50 µm ili više. Postoje i monolitne kolone u kojima je sorbent monolit sa prolaznim porama koji ispunjavaju čitav volumen kolone.
Visoku efikasnost odvajanja osigurava velika površina čestica sorbenta (što je posljedica njihove mikroskopske veličine i prisutnosti pora), kao i ujednačenost sastava sorbenta i njegovo gusto i ujednačeno pakovanje.
Detektori
U tečnoj hromatografiji visokih performansi koriste se različite metode detekcije. U opštem slučaju, mobilna faza sa komponentama rastvorenim u njoj, nakon hromatografske kolone, ulazi u detektorsku ćeliju, gde se neprekidno meri jedno ili drugo njeno svojstvo (apsorpcija u ultraljubičastom ili vidljivom delu spektra, fluorescencija, refrakcija indeks, električna provodljivost, itd.). Dobijeni hromatogram je graf zavisnosti nekog fizičkog ili fizičko-hemijskog parametra mobilne faze o vremenu.
Najčešći detektori u tečnoj hromatografiji visokih performansi su spektrofotometrijski. Tokom eluiranja supstanci u posebno dizajniranoj mikroćeliji, optička gustina eluata se meri na unapred odabranoj talasnoj dužini. Širok raspon linearnosti detektora omogućava analizu i nečistoća i glavnih komponenti mješavine na jednom hromatogramu. Spektrofotometrijski detektor omogućava detekciju na bilo kojoj talasnoj dužini unutar svog radnog opsega (obično 190-600 nm). Koriste se i višetalasni detektori, koji omogućavaju detekciju na nekoliko talasnih dužina istovremeno, i detektori diodnog niza, koji omogućavaju istovremeno snimanje optičke gustine u čitavom radnom opsegu talasnih dužina (obično 190–950 nm). Ovo omogućava snimanje spektra apsorpcije komponenti koje prolaze kroz detektorsku ćeliju.
Fluorometrijski detektor se koristi za detekciju fluorescentnih ili nefluorescentnih jedinjenja u obliku njihovih fluorescentnih derivata. Princip rada fluorimetrijskog detektora zasniva se na mjerenju fluorescentne emisije apsorbirane svjetlosti. Apsorpcija se obično vrši u ultraljubičastom području spektra, talasne dužine fluorescentnog zračenja premašuju talasne dužine apsorbovane svetlosti. Fluorometrijski detektori imaju vrlo visoku osjetljivost i selektivnost. Osetljivost fluorescentnih detektora je približno 1000 puta veća od one spektrofotometrijskih. Savremeni fluorescentni detektori omogućavaju ne samo dobijanje hromatograma, već i snimanje spektra ekscitacije i fluorescencije analiziranih jedinjenja.
Da biste odredili jedinjenja koja slabo apsorbuju u ultraljubičastom i vidljivom području spektra (na primjer, ugljikohidrati), koristite refraktometrijski detektori (refraktometri). Nedostaci ovih detektora su njihova niska (u poređenju sa spektrofotometrijskim detektorima) osjetljivost i značajna temperaturna ovisnost intenziteta signala (detektor mora biti termostatiran), kao i nemogućnost korištenja u načinu gradijentnog eluiranja.
Princip rada evaporativni detektori laserskog raspršivanja svjetlosti zasniva se na razlici u pritiscima pare hromatografskih rastvarača koji čine mobilnu fazu i analiziranih supstanci. Mobilna faza na izlazu iz kolone se uvodi u raspršivač, pomiješa se sa dušikom ili CO 2 i u obliku fino dispergovanog aerosola ulazi u zagrijanu cijev isparivača temperature 30-160 °C, u kojoj se mobilna faza isparava. Aerosol neisparljivih čestica analiziranih supstanci raspršuje svjetlosni tok u disperzionoj komori. Po stepenu disperzije svetlosnog toka može se suditi o količini određenog jedinjenja. Detektor je osjetljiviji od refraktometrijskog, njegov signal ne ovisi o optičkim svojstvima uzorka, o vrsti funkcionalnih grupa u analitima, o sastavu mobilne faze i može se koristiti u načinu gradijentnog eluiranja. .
Elektrohemijski detektori (konduktometrijski, amperometrijski, kulometrijski itd.). Amperometrijski detektor se koristi za detekciju elektroaktivnih spojeva koji se mogu oksidirati ili reducirati na površini čvrste elektrode. Analitički signal je veličina struje oksidacije ili redukcije. Detektorska ćelija ima najmanje dvije elektrode - radnu elektrodu i referentnu elektrodu (srebrni klorid ili čelik). Na elektrode se primjenjuje radni potencijal čija vrijednost ovisi o prirodi spojeva koji se određuju. Mjerenja se mogu vršiti i pri konstantnom potencijalu i u impulsnom režimu, kada se profil promjene potencijala radne elektrode postavlja tokom jednog ciklusa snimanja signala. Amperometrijski detektor koristi radne elektrode od karbonskih materijala (najčešće staklastog ugljenika ili grafita), i metala: platine, zlata, bakra, nikla.
Konduktometrijski detektor se koristi za detekciju aniona i kationa u ionskoj hromatografiji. Princip njegovog rada zasniva se na mjerenju električne provodljivosti mobilne faze tokom eluiranja supstance.
Izuzetno informativan je maseni spektrometrijski detektor koji ima visoku osjetljivost i selektivnost. Najnoviji modeli masenih spektrometara za tečnu hromatografiju rade u opsegu mase m/z od 20 do 4000 amu.
Tečna hromatografija visokih performansi također koristi Fourier-IR detektore, radioaktivnost i neke druge.
Sistem prikupljanja i obrade podataka
Savremeni sistem za obradu podataka je personalni računar povezan sa hromatografom sa instaliranim softverom koji omogućava registraciju i obradu hromatograma, kao i kontrolu rada hromatografa i praćenje glavnih parametara hromatografskog sistema.
mobilna faza
Mobilna faza u tečnoj hromatografiji visokih performansi ima dvostruku funkciju: osigurava prijenos desorbiranih molekula duž kolone i reguliše konstante ravnoteže, a samim tim i zadržavanje kao rezultat interakcije sa stacionarnom fazom (ssorbiranom na površini). ) i sa molekulima supstanci koje se odvajaju. Dakle, promenom sastava mobilne faze u tečnoj hromatografiji visokih performansi, može se uticati na vreme zadržavanja jedinjenja, selektivnost i efikasnost njihovog razdvajanja.
Mobilna faza se može sastojati od jednog rastvarača, često dva, ako je potrebno, tri ili više. Sastav mobilne faze je naznačen kao volumni odnos njenih sastavnih rastvarača. U nekim slučajevima može biti naznačen omjer mase, što treba posebno navesti. Kao komponente mobilne faze mogu se koristiti puferske otopine određene pH vrijednosti, razne soli, kiseline i baze i drugi modifikatori.
Normalna fazna hromatografija obično koristi tečne ugljovodonike (heksan, cikloheksan, heptan) i druge relativno nepolarne rastvarače sa malim dodacima polarnih organskih jedinjenja koja kontrolišu elucionu snagu mobilne faze.
U hromatografiji reverzne faze, voda ili vodeno-organske smjese se koriste kao mobilna faza. Organski aditivi su obično polarni organski rastvarači (acetonitril i metanol). Za optimizaciju separacije mogu se koristiti vodene otopine određene pH vrijednosti, posebno puferske otopine, kao i različiti aditivi mobilnoj fazi: fosforna i octena kiselina u separaciji kiselih spojeva; amonijak i alifatski amini u odvajanju baznih spojeva i drugi modifikatori.
Čistoća mobilne faze uvelike utječe na hromatografsku analizu, pa je poželjno koristiti otapala koja su puštena posebno za tečnu hromatografiju (uključujući vodu).
Kada se koristi UV spektrofotometrijski detektor, mobilna faza ne bi trebalo da ima izraženu apsorpciju na talasnoj dužini odabranoj za detekciju. Granica prozirnosti ili optičke gustoće na određenoj talasnoj dužini otapala određenog proizvođača često je naznačena na pakovanju.
Mobilna faza i analizirani rastvori moraju biti bez neotopljenih čestica i mehurića gasa. Voda dobijena u laboratorijskim uslovima, vodeni rastvori, organski rastvarači prethodno pomešani sa vodom, kao i analizirani rastvori moraju biti podvrgnuti finoj filtraciji i degazaciji. U ove svrhe obično se koristi vakuum filtracija kroz membranski filter veličine pora od 0,45 μm, koji je inertan u odnosu na dato otapalo ili otopinu.
Spisak hromatografskih uslova koje treba navesti
Monografija treba da sadrži: puni komercijalni naziv kolone, navodeći proizvođača i kataloški broj, dimenzije kolone (dužina i unutrašnji prečnik), vrstu sorbenta, navodeći veličinu čestica, veličinu pora, temperaturu kolone (ako je potrebna kontrola temperature) , zapreminu ubrizganog uzorka (volumenske petlje), sastav mobilne faze i način njene pripreme, brzinu kretanja mobilne faze, tip detektora i uslove detekcije (ako je potrebno, parametre detektorske ćelije koja se koristi), opis načina gradijenta (ako je korišćeni), uključujući fazu reekvilibracije na početne uslove, vreme hromatografije, detaljan opis metodologije i proračunskih formula, opise pripreme standardnih i test rastvora.
Ako se u autosampleru koristi derivatizacija prije kolone, daju se informacije o programu za automatsko uzorkovanje. U slučaju upotrebe derivatizacije nakon kolone, naznačena je brzina dodavanja reagensa za derivatizaciju, zapremina petlje za miješanje i njena temperatura.
Modificirana tečna hromatografija visokih performansi
Ionska parna hromatografija
Jedna od varijanti tečne hromatografije visokih performansi reverzne faze je ionska parna hromatografija - koja vam omogućava da odredite jonizovana jedinjenja. Da bi se to postiglo, hidrofobna organska jedinjenja sa ionogenim grupama (reagensi jonski par) dodaju se tradicionalnoj reverzno-faznoj tečnoj hromatografiji visoke performanse mobilne faze. Natrijum alkil sulfati se obično koriste za odvajanje baza; tetraalkilamonijum soli (tetrabutilamonijum fosfat, cetiltrimetilamonijum bromid, itd.) se koriste za odvajanje kiselina. U režimu ionskog para, selektivnost razdvajanja nejonskih komponenti bit će ograničena mehanizmom zadržavanja obrnute faze, dok se zadržavanje baza i kiselina značajno povećava, dok se oblik hromatografskih vrhova poboljšava.
Zadržavanje u režimu jonskog para nastaje zbog prilično složenih procesa ravnoteže koji se međusobno nadmeću. S jedne strane, zbog hidrofobnih interakcija i efekta pomicanja polarnog medija mobilne faze, moguća je sorpcija hidrofobnih jona na površini alkil silika gela na način da se nabijene grupe okrenu prema mobilnoj fazi. U ovom slučaju, površina poprima svojstva ionske izmjene, a zadržavanje se pokorava zakonima ionsko-izmjenjivačke hromatografije. S druge strane, moguće je formiranje jonskog para direktno u zapremini eluenta, nakon čega slijedi njegova sorpcija na sorbentu mehanizmom obrnute faze.
Hidrofilna interakcijska hromatografija ( HILIĆ hromatografija)
Hidrofilna interakcijska hromatografija se koristi za odvajanje polarnih jedinjenja koja se slabo zadržavaju u tečnoj hromatografiji visokih performansi reverzne faze. Kao mobilna faza u ovoj varijanti hromatografije koriste se mješavine vode i acetonitrila sa dodatkom soli, kiselina ili baza. Stacionarne faze su, po pravilu, silika gelovi modifikovani polarnim grupama (amino, diol, cijanopropil grupe itd.). Polarnija jedinjenja se drže jače. Moć eluiranja mobilne faze raste sa povećanjem polariteta.
Jonska izmjena i tečna hromatografija visokih performansi
Ionska izmjenjivačka hromatografija se koristi za analizu kako organskih (heterociklične baze, aminokiseline, proteini, itd.) tako i neorganskih (razni kationi i anjoni) spojeva. Odvajanje komponenti analizirane smjese u jonoizmenjivačkoj hromatografiji zasniva se na reverzibilnoj interakciji jona analiziranih supstanci sa jonoizmjenjivačkim grupama sorbenta. Ovi sorbenti su uglavnom ili polimerne smole za izmjenu jona (obično kopolimeri stirena i divinilbenzena sa cijepljenim grupama za izmjenu jona) ili silika gelovi sa cijepljenim grupama za izmjenu jona. Sorbenti sa grupama: -NH 3 +, -R 3 N +, -R 2 HN +, -RH 2 N + itd. koriste se za odvajanje anjona (anjonski izmjenjivači), a sorbenti sa grupama: -SO 3 -, - RSO 3 -, -COOH, -PO 3 - i drugi za odvajanje kationa (katjonski izmjenjivači).
Kao mobilna faza u jono-izmjenjivačkoj hromatografiji koriste se vodeni rastvori kiselina, baza i soli. Obično se puferske otopine koriste za održavanje određenih pH vrijednosti. Također je moguće koristiti male dodatke organskih rastvarača koji se miješaju s vodom - acetonitrila, metanola, etanola, tetrahidrofurana.
Ionska hromatografija - varijanta ionsko-izmjenjivačke hromatografije, u kojoj se konduktometrijski detektor koristi za detekciju analita (jona). Za visoko osjetljivo određivanje promjena u provodljivosti mobilne faze koja prolazi kroz detektor, pozadinska provodljivost mobilne faze mora biti niska.
Postoje dvije glavne varijante jonske hromatografije.
Prva od njih, dvokolona jonska hromatografija, zasniva se na supresiji električne provodljivosti elektrolita mobilne faze pomoću druge kolone za izmjenu jona ili posebnog membranskog supresijskog sistema koji se nalazi između analitičke kolone i detektora. Prilikom prolaska kroz sistem, električna provodljivost mobilne faze se smanjuje.
Druga varijanta jonske hromatografije je ionska hromatografija na jednoj koloni. Ova varijanta koristi mobilnu fazu sa vrlo niskom električnom provodljivošću. Kao elektroliti se široko koriste slabe organske kiseline: benzojeva, salicilna ili izoftalna.
Tečna hromatografija visokih performansi bez veličine
Kromatografija isključenja veličine (gel hromatografija) je posebna verzija tečne hromatografije visokih performansi zasnovana na razdvajanju molekula po njihovoj veličini. Raspodjela molekula između stacionarne i pokretne faze temelji se na veličini molekula i dijelom na njihovom obliku i polaritetu.
Moguća su dva ograničavajuća tipa interakcije molekula sa poroznom stacionarnom fazom. Molekuli veći od maksimalnog promjera pora uopće se ne zadržavaju i prvo se eluiraju, krećući se zajedno s mobilnom fazom. Molekuli čija je veličina manja od minimalnog promjera pora sorbenta slobodno prodiru u pore i posljednji se eluiraju iz kolone. Preostale molekule, koje imaju srednje veličine, djelomično se zadržavaju u porama i tokom eluiranja se razdvajaju na frakcije u skladu sa svojom veličinom i, dijelom, oblikom, prodiru u pore sorbenta, ovisno o veličini i djelimično , u zavisnosti od njihovog oblika. Kao rezultat toga, tvari se eluiraju s različitim vremenima zadržavanja.
Ionska isključena hromatografija
Mehanizam ionsko-ekskluzivne hromatografije zasniva se na efektu, zbog čega se jedinjenja u jonizovanom obliku ne zadržavaju na jonoizmenjivačkom sorbentu, dok se jedinjenja u molekularnom obliku raspoređuju između stacionarne i vodene faze unutar pora. jonoizmenjivačkog sorbenta i mobilne faze koja migrira u prostoru između čestica sorbenta. Razdvajanje se zasniva na elektrostatičkom odbijanju, polarnim i hidrofobnim interakcijama između otopljenih jedinjenja i sorbenta.
Anionske grupe na površini sorbenta djeluju kao polupropusna "membrana" između stacionarne i mobilne faze. Negativno nabijene komponente ne dosežu stacionarnu mobilnu fazu, jer ih odbijaju slično nabijene funkcionalne grupe i eluiraju u "mrtvom" (slobodnom) volumenu kolone. Komponente u molekularnom obliku se ne "odbacuju" sorbentom za kationsku izmjenu i distribuiraju se između stacionarne i mobilne faze. Razlika u stepenu zadržavanja nejonskih komponenti smeše je diktirana kombinacijom polarnih interakcija nejonskih komponenti sa funkcionalnim grupama sorbenta za kationsku izmjenu i hidrofobnih interakcija nejonskih komponenti sa nejonskim komponentama. -polarna sorbentna matrica.
Kiralna hromatografija
Cilj kiralne hromatografije je odvajanje optičkih izomera. Razdvajanje se vrši na kiralnim stacionarnim fazama ili na konvencionalnim akiralnim stacionarnim fazama koristeći kiralne mobilne faze. Kao hiralne stacionarne faze koriste se sorbenti sa modifikovanom površinom, grupe ili supstance koje imaju kiralne centre (hitozani, ciklodekstrini, polisaharidi, proteini itd. (hiralni selektori)). kromatografija normalne ili reverzne faze. Kada se koriste akiralne stacionarne faze da bi se osiguralo razdvajanje enantiomera, mobilnim fazama se dodaju kiralni modifikatori: kiralni metalni kompleksi, neutralni kiralni ligandi, kiralni reagensi ionskog para, itd.
Ultra performans tečna hromatografija
Tečna hromatografija ultra performansi je varijanta tečne hromatografije koja je efikasnija od klasične tečne hromatografije visokih performansi.
Karakteristika tečne hromatografije ultra-performanse je upotreba sorbenata veličine čestica od 1,5 do 2 µm. Kromatografske kolone su tipično duge 50 do 150 mm i prečnika 1 do 4 mm. Volumen ubrizganog uzorka može biti od 1 do 50 µl. Upotreba ovakvih hromatografskih kolona može značajno smanjiti vreme analize i poboljšati efikasnost hromatografskog odvajanja. Međutim, u ovom slučaju, pritisak na kolonu može doseći 80–120 MPa, potrebna frekvencija prikupljanja podataka detektora može se povećati do 40–100 Hz, a volumen van kolone hromatografskog sistema mora biti minimiziran. Oprema za hromatografiju i kolone koje se koriste u tečnoj hromatografiji ultra performansi su posebno prilagođene da zadovolje zahteve ove vrste hromatografije.
Oprema dizajnirana za tečnu hromatografiju ultra performansi može se koristiti i u klasičnoj tečnoj hromatografiji visokih performansi.
(uglavnom intermolekularne) na sučelju. Kao metoda analize, HPLC je deo grupe metoda, koja zbog složenosti objekata koji se proučava uključuje preliminarno razdvajanje početne složene smeše na relativno jednostavne. Dobijene jednostavne smjese se zatim analiziraju konvencionalnim fizičko-hemijskim metodama ili posebnim metodama razvijenim za hromatografiju.
HPLC metoda se široko koristi u oblastima kao što su hemija, petrohemija, biologija, biotehnologija, medicina, prerada hrane, zaštita životne sredine, proizvodnja lekova i mnogim drugim.
Prema mehanizmu razdvajanja analiziranih ili izdvojenih supstanci, HPLC se deli na adsorpcionu, distribucionu, jono-izmjenjivačku, ekskluzijsku, ligand-izmjenjivačku i druge.
Treba imati na umu da se u praktičnom radu razdvajanje često odvija ne jednim, već nekoliko mehanizama istovremeno. Dakle, odvajanje isključenja može biti komplikovano efektima adsorpcije, adsorpcije – distribucije, i obrnuto. Istovremeno, što je veća razlika u supstancama u uzorku u pogledu stepena jonizacije, bazičnosti ili kiselosti, u smislu molekulske težine, polarizabilnosti i drugih parametara, veća je verovatnoća da će drugačiji mehanizam razdvajanja pojavljuju za takve supstance.
HPLC normalne faze
Stacionarna faza je polarnija od mobilne faze, tako da u sastavu eluenta prevladava nepolarno otapalo:
- Heksan:izopropanol = 95:5 (za niskopolarne supstance)
- Hloroform:metanol = 95:5 (za srednje polarne supstance)
- Hloroform:metanol = 80:20 (za visoko polarne supstance)
HPLC reverzne faze
Stacionarna faza je manje polarna od mobilne faze, tako da je voda gotovo uvijek prisutna u eluentu. U ovom slučaju, uvijek je moguće osigurati potpuno otapanje BAS-a u mobilnoj fazi, gotovo uvijek je moguće koristiti UV detekciju, gotovo sve mobilne faze se međusobno miješaju, može se koristiti gradijent elucije, kolona se može brzo vratiti -uravnotežen, kolona se može regenerisati.
Uobičajeni eluenti za HPLC reverzne faze su:
- Acetonitril: voda
- metanol: voda
- Izopropanol: voda
Matrice za HPLC
Matrice koje se koriste u HPLC-u su neorganska jedinjenja kao što su silika (silika gel) ili glinica, ili organski polimeri kao što je polistiren (poprečno povezan sa divinilbenzenom) ili polimetakrilat. Silika gel je, naravno, sada opšteprihvaćen.
Glavne karakteristike matrice:
- Veličina čestica (µm);
- Veličina unutrašnjih pora (Å, nm).
Dobijanje silika gela za HPLC:
- Formiranje mikrosfera polisilicijske kiseline;
- Sušenje čestica silika gela;
- Odvajanje vazduha.
Sorbentne čestice:
- Regularni (sferični): veća otpornost na pritisak, veća cijena;
- Nesferični: niža otpornost na pritisak.
Veličina pora u HPLC je jedan od najvažnijih parametara. Što je veličina pora manja, to je lošija njihova propusnost za molekule eluiranih tvari. I shodno tome, lošiji je sorpcijski kapacitet sorbenata. Što su pore veće, to je, prvo, manja mehanička stabilnost čestica sorbenta, a drugo, manja je površina sorpcije, pa je i efikasnost lošija.
Graftovi stacionarne faze
HPLC normalne faze:
- Stacionarna faza cijepljena propilnitrilom (nitrilom);
- Stacionarna faza sa kalemljenjem propilamina (amina).
HPLC reverzne faze:
- Stacionarna faza sa alkil graftom;
- Stacionarna faza sa alkilsilil graftom.
End-capping - zaštita necijepljenih područja sorbenta dodatnim cijepljenjem sa "malim" molekulima. Hidrofobno zatvaranje (C1, C2): veća selektivnost, lošija kvašenje; hidrofilno zatvaranje (diol): niža selektivnost, veća sposobnost vlaženja.
HPLC detektori
- UV
- diodni niz
- Fluorescentno
- Elektrohemijski
- Refraktometrijski
- masovno selektivno
Linkovi
Wikimedia fondacija. 2010 .
Pogledajte šta je "tečna hromatografija visokih performansi" u drugim rječnicima:
tečna hromatografija visokih performansi- - [A.S. Goldberg. Engleski ruski energetski rječnik. 2006] Teme energija općenito EN tečna hromatografija visokih performansiHPLC … Priručnik tehničkog prevodioca
Termin tečna hromatografija visokih performansi Engleski izraz tečna hromatografija visokih performansi Sinonimi Skraćenice HPLC, HPLC Povezani pojmovi adsorpcija, oligopeptid, proteomika, sorbent, fuleren, endoedra, hromatografija… …
Tekućom hromatografijom, da bi se povećala efikasnost razdvajanja, rastvarač (eluent) pod pritiskom (više od 3x107 Pa) se pumpa kroz kolone ispunjene sorbentom sa česticama malog prečnika (do 1 μm), a perfuziju... ...
Vrsta hromatografije u kojoj tečnost (eluent) služi kao mobilna faza, a ona je stacionarna faza. sorbent, tv. nosač sa tečnošću ili gelom koji se nanosi na njegovu površinu. Izvodi se u koloni ispunjenoj sorbentom (kolona hromatografija), na ravnom ... ... Prirodna nauka. enciklopedijski rječnik
- [κρώμα (υroma) boja] proces koji se zasniva na nejednakoj sposobnosti pojedinačnih komponenti smeše (tečnih ili gasovitih) da ostanu na površini adsorbenta i kada se apsorbuju iz struje nosača i kada ... ... Geološka enciklopedija
- (sa drugog grčkog ... Wikipedia
Pojam hromatografija Engleski termin hromatografija Sinonimi Skraćenice Povezani pojmovi tečna hromatografija visokih performansi, klatrat, laboratorija na čipu, porozimetrija, proteom, proteomika, sorbent, enzim, fuleren, endoedral… … Enciklopedijski rečnik nanotehnologije
Tečna hromatografija zasnovana na dekomp. sposobnost odvojenih jona da razmjenjuju jone sa fiksiranim. joni sorbenta koji nastaju kao rezultat disocijacije ionogenih grupa potonjih. Kationski izmjenjivači se koriste za odvajanje katjona, za ... ... Chemical Encyclopedia
HPLC- tečna hromatografija visokih performansi... Rečnik skraćenica ruskog jezika
Tečna hromatografija visokih performansi (HPLC) je jedna od efikasnih metoda za odvajanje složenih smeša supstanci, koja se široko koristi kako u analitičkoj hemiji tako i u hemijskoj tehnologiji. Osnova hromatografskog odvajanja je učešće ... Wikipedia
Knjige
- Praktična tečna hromatografija visokih performansi, Veronica R. Mayer. Čitaocu predstavljamo 5. izdanje knjige, koje je prošireno savremenim metodama i opremom. U knjizi je mnogo toga poboljšano i dodat je veliki broj referenci. Mesta u tekstu na kojima...