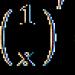Zatim ulazi acetil-SCoA nastao u reakciji PVK dehidrogenaze ciklus trikarboksilne kiseline (TCA ciklus, ciklus limunske kiseline, Krebsov ciklus). Osim piruvata, u ciklus su uključene keto kiseline koje dolaze iz katabolizma aminokiseline ili bilo koje druge tvari.
Ciklus trikarboksilnih kiselina
Ciklus se nastavlja mitohondrijski matriks i predstavlja oksidacija molekule acetil-SCoA u osam uzastopnih reakcija.
U prvoj reakciji se vežu acetil I oksalacetat(oksaloctena kiselina) da nastane citrat(limunska kiselina), tada dolazi do izomerizacije limunske kiseline izocitrat te dvije reakcije dehidrogenacije s popratnim oslobađanjem CO 2 i redukcijom NAD.
U petoj reakciji nastaje GTP, to je reakcija fosforilacija supstrata. Zatim se sekvencijalno događa dehidrogenacija ovisna o FAD-u sukcinat(jantarna kiselina), hidratacija fumarova kiseline do malat(jabučna kiselina), zatim NAD-ovisna dehidrogenacija koja rezultira stvaranjem oksalacetat.
Kao rezultat toga, nakon osam reakcija ciklusa opet nastaje oksalacetat .
Zadnje tri reakcije čine tzv. biokemijski motiv (dehidrogenacija ovisna o FAD-u, hidratacija i dehidrogenacija ovisna o NAD-u, koristi se za uvođenje keto skupine u sukcinatnu strukturu. Ovaj je motiv također prisutan u reakcijama β-oksidacije masnih kiseline. Obrnutim redoslijedom (redukcija, de hidratacija i redukcija) ovaj se motiv opaža u reakcijama sinteze masnih kiselina.
Funkcije TsTK
1. Energija
- generacija atomi vodika za funkcioniranje dišnog lanca i to tri molekule NADH i jednu molekulu FADH2,
- sinteza jedne molekule GTF(ekvivalent ATP-u).
2. Anabolički. U TCC nastaju
- prekursor hema sukcinil-SCoA,
- keto kiseline koje se mogu pretvoriti u aminokiseline - α-ketoglutarat za glutaminsku kiselinu, oksalacetat za asparaginsku kiselinu,
- limunska kiselina, koristi se za sintezu masnih kiselina,
- oksalacetat, koristi se za sintezu glukoze.

Anaboličke reakcije TCA ciklusa
Regulacija ciklusa trikarboksilnih kiselina
Alosterična regulacija
Enzimi koji kataliziraju 1., 3. i 4. reakciju TCA ciklusa osjetljivi su na alosterična regulacija metaboliti:
Regulacija dostupnosti oksaloacetata
Glavni I Osnovni, temeljni Regulator TCA ciklusa je oksaloacetat, odnosno njegova dostupnost. Prisutnost oksaloacetata regrutira acetil-SCoA u TCA ciklus i pokreće proces.
Obično ćelija ima ravnoteža između stvaranja acetil-SCoA (iz glukoze, masnih kiselina ili aminokiselina) i količine oksaloacetata. Izvor oksaloacetata je piruvat, (formiran od glukoze ili alanina), dobiven iz asparaginska kiselina kao rezultat transaminacije ili AMP-IMP ciklusa, a također i iz voćne kiseline samog ciklusa (jantarna, α-ketoglutarna, jabučna, limunska), koji mogu nastati tijekom katabolizma aminokiselina ili nastati iz drugih procesa.

Sinteza oksaloacetata iz piruvata
Regulacija aktivnosti enzima piruvat karboksilaza provedeno uz sudjelovanje acetil-SCoA. Alosteričan je aktivator enzima, a bez njega je piruvat karboksilaza praktički neaktivna. Kada se acetil-SCoA nakupi, enzim počinje djelovati i nastaje oksaloacetat, ali, naravno, samo u prisustvu piruvata.
Također većina aminokiseline tijekom katabolizma mogu se transformirati u metabolite TCA ciklusa, koji zatim prelaze u oksaloacetat, koji također održava aktivnost ciklusa.

Nadopunjavanje bazena metabolita TCA ciklusa iz aminokiselina
Reakcije nadopunjavanja ciklusa novim metabolitima (oksaloacetat, citrat, α-ketoglutarat itd.) nazivaju se anaplerotičan.
Uloga oksalacetata u metabolizmu
Primjer značajnu ulogu oksalacetat služi za aktiviranje sinteze ketonskih tijela i ketoacidoza krvna plazma pri nedovoljna količina oksalacetata u jetri. Ovo stanje se opaža tijekom dekompenzacije dijabetes melitusa ovisnog o inzulinu (dijabetes tipa 1) i tijekom posta. Kod ovih poremećaja u jetri se aktivira proces glukoneogeneze, tj. stvaranje glukoze iz oksalacetata i drugih metabolita, što za posljedicu ima smanjenje količine oksalacetata. Istodobna aktivacija oksidacije masnih kiselina i nakupljanje acetil-SCoA pokreće rezervni put za iskorištavanje acetilne skupine - sinteza ketonska tijela . U tom slučaju dolazi do zakiseljavanja krvi u tijelu ( ketoacidoza) s karakterističnom kliničkom slikom: slabost, glavobolja, pospanost, smanjen tonus mišića, tjelesna temperatura i krvni tlak.

Promjene u brzini reakcija TCA ciklusa i razlozi nakupljanja ketonskih tijela pod određenim uvjetima
Opisana metoda regulacije uz sudjelovanje oksaloacetata ilustracija je prekrasne formulacije " Masti izgaraju u plamenu ugljikohidrata"To implicira da "plamen sagorijevanja" glukoze dovodi do pojave piruvata, a piruvat se pretvara ne samo u acetil-SCoA, već iu oksalacetat. Prisutnost oksaloacetata osigurava uključivanje acetilne skupine nastale iz masne kiseline u obliku acetil-SCoA, u prvoj reakciji TCA ciklusa.
U slučaju velikog "izgaranja" masnih kiselina, koje se opaža u mišićima tijekom fizički rad i u jetri post, brzina ulaska acetil-SCoA u reakciju TCA ciklusa izravno će ovisiti o količini oksaloacetata (ili oksidirane glukoze).
Ako je količina oksalacetata u hepatocit nije dovoljna (nema glukoze ili nije oksidirana u piruvat), tada će acetilna skupina ići na sintezu ketonskih tijela. To se događa kada dugi post I dijabetes melitus tipa 1.
Glavnina kemijska energija ugljik se oslobađa u aerobnim uvjetima uz sudjelovanje kisika. Krebsov ciklus naziva se i ciklus limunske kiseline ili stanično disanje. U dešifriranju pojedinih reakcija ovog procesa sudjelovali su mnogi znanstvenici: A. Szent-Gyorgyi, A. Leninger, H. Krebs, po kojem je ciklus i dobio ime, S. E. Severin i drugi.
Postoji tijesan korelativni odnos između anaerobne i aerobne razgradnje ugljikohidrata. Prije svega, izražava se u prisutnosti pirogrožđane kiseline, koja dovršava anaerobnu razgradnju ugljikohidrata i započinje stanično disanje (Krebsov ciklus). Obje faze kataliziraju isti enzimi. Kemijska energija se oslobađa tijekom fosforilacije i pohranjuje se u obliku makroerga ATP-a. U kemijskim reakcijama sudjeluju isti koenzimi (NAD, NADP) i kationi. Razlike su sljedeće: ako je anaerobna razgradnja ugljikohidrata pretežno lokalizirana u hijaloplazmi, tada se reakcije staničnog disanja odvijaju uglavnom u mitohondrijima.
Pod nekim uvjetima opaža se antagonizam između obje faze. Dakle, u prisutnosti kisika, glikoliza se naglo smanjuje (Pasteurov učinak). Produkti glikolize mogu inhibirati aerobni metabolizam ugljikohidrata (Crabtree efekt).
Krebsov ciklus ima niz kemijske reakcije, uslijed čega se proizvodi razgradnje ugljikohidrata oksidiraju u ugljični dioksid i vodu, a kemijska energija se akumulira u visokoenergetske spojeve. Za to vrijeme nastaje "nosač" - oksaloctena kiselina (OA). Nakon toga dolazi do kondenzacije s "nosačem" aktiviranog ostatka octene kiseline. Pojavljuje se trikarboksilna kiselina – limunska kiselina. Tijekom kemijskih reakcija, ostatak octene kiseline se "okreće" u ciklusu. Od svake molekule pirogrožđane kiseline nastaje osamnaest molekula adenozin trifosfatne kiseline. Na kraju ciklusa oslobađa se “nosač” koji reagira s novim molekulama aktiviranog ostatka octene kiseline.
Krebsov ciklus: reakcije
Ako je konačni proizvod anaerobne razgradnje ugljikohidrata mliječna kiselina, tada se pod utjecajem laktat dehidrogenaze oksidira u pirogrožđanu kiselinu. Dio molekula pirogrožđane kiseline ulazi u sintezu "nosača" alkalne kiseline pod utjecajem enzima piruvat karboksilaze i u prisutnosti iona Mg2 +. Neke od molekula pirogrožđane kiseline izvor su stvaranja "aktivnog acetata" - acetil koenzima A (acetil-CoA). Reakcija se odvija pod utjecajem piruvat dehidrogenaze. Acetil-CoA sadrži oko 5-7% energije. Većina kemijske energije nastaje kao rezultat oksidacije "aktivnog acetata".
Pod utjecajem citrat sintetaze počinje funkcionirati i sam Krebsov ciklus koji dovodi do stvaranja citratne kiseline. Ova kiselina se pod utjecajem akonitat hidrataze dehidrogenira i pretvara u cis-akonitnu kiselinu, koja nakon dodavanja molekule vode postaje izocitrična kiselina. Između tri trikarboksilne kiseline uspostavlja se dinamička ravnoteža.
Izocitrična kiselina se oksidira u oksalojantarnu kiselinu, koja se dekarboksilira i pretvara u alfa-ketoglutarnu kiselinu. Reakciju katalizira enzim izocitrat dehidrogenaza. Alfa-ketoglutarna kiselina se dekarboksilira pod utjecajem enzima 2-okso-(alfa-keto)-glutarat dehidrogenaze, što rezultira stvaranjem sukcinil-CoA koji sadrži visokoenergetsku vezu.
U sljedećoj fazi sukcinil-CoA pod djelovanjem enzima sukcinil-CoA sintetaze prenosi visokoenergetsku vezu na GDP (gvanozin difosfatnu kiselinu). GTP (gvanozin trifosfatna kiselina) pod utjecajem enzima GTP-adenilatne kinaze daje visokoenergetsku vezu na AMP (adenozin monofosfatna kiselina). Krebsov ciklus: formule - GTP + AMP - BDP + ADP.
Pod utjecajem enzima sukcinat dehidrogenaze (SDH) oksidira se u fumarnu kiselinu. Koenzim SDH je flavin adenin dinukleotid. Fumarat se pod utjecajem enzima fumarat hidrataze pretvara u jabučnu kiselinu, koja se zatim oksidira, stvarajući AA. U prisutnosti acetil-CoA u reakcijskom sustavu, alkalna kiselina ponovno se uključuje u ciklus trikarboksilne kiseline.
Dakle, od jedne molekule glukoze nastaje do 38 molekula ATP (dvije uslijed anaerobne glikolize, šest kao rezultat oksidacije dviju molekula NAD·H+H+ koje su nastale tijekom glikolitičke oksidacije i 30 zbog TCA ciklusa) . Učinkovitost TTC-a je 0,5. Ostatak energije se rasipa kao toplina. U ciklusu TCA oksidira se 16-33% laktatne kiseline, a ostatak se koristi za resintezu glikogena.
Ciklus trikarboksilne kiseline prvi je otkrio engleski biokemičar Krebs. On je prvi pretpostavio važnost ovog ciklusa za potpuno izgaranje piruvata, čiji je glavni izvor glikolitička pretvorba ugljikohidrata. Naknadno je pokazano da je ciklus trikarboksilne kiseline "žarište" u kojem konvergiraju gotovo svi metabolički putovi.
Dakle, acetil-CoA nastao kao rezultat oksidativne dekarboksilacije piruvata ulazi u Krebsov ciklus. Ovaj ciklus se sastoji od osam uzastopnih reakcija (slika 91). Ciklus počinje kondenzacijom acetil-CoA s oksaloacetatom i stvaranjem limunske kiseline. ( Kao što će se vidjeti u nastavku, u ciklusu nije sam acetil-CoA taj koji prolazi oksidaciju, već više složena veza- limunska kiselina (trikarboksilna kiselina).)
Tada limunska kiselina (spoj sa šest ugljika), nizom dehidrogenacija (uklanjanje vodika) i dekarboksilacije (eliminacija CO 2), gubi dva atoma ugljika i ponovno se pojavljuje oksaloacetat (spoj s četiri ugljika) u Krebsovom ciklusu, tj. kao rezultat potpune revolucije ciklusa, molekula acetil-CoA izgara do CO 2 i H 2 O, a molekula oksaloacetata se regenerira. Ispod je svih osam sekvencijalnih reakcija (faza) Krebsovog ciklusa.
U prvoj reakciji, koju katalizira enzim citrat sintaza, acetil-CoA se kondenzira s oksaloacetatom. Kao rezultat toga nastaje limunska kiselina:

Očigledno, u ovoj reakciji, citril-CoA vezan za enzim nastaje kao međuprodukt. Potonji se zatim spontano i nepovratno hidrolizira u obliku citrata i HS-CoA.
U drugoj reakciji ciklusa, nastala limunska kiselina prolazi kroz dehidraciju da bi nastala cis-akonitna kiselina, koja, dodavanjem molekule vode, postaje izocitrična kiselina. Ove reverzibilne reakcije hidratacije-dehidracije katalizira enzim akonitat hidrataza:

U trećoj reakciji, koja se čini kao reakcija koja ograničava brzinu Krebsovog ciklusa, izocitratna kiselina se dehidrogenira u prisutnosti NAD-ovisne izocitrat dehidrogenaze:

(Postoje dvije vrste izocitrat dehidrogenaza u tkivima: NAD- i NADP-ovisne. Utvrđeno je da NAD-ovisna izocitrat dehidrogenaza ima ulogu glavnog katalizatora oksidacije izocitrične kiseline u Krebsovom ciklusu.)
Tijekom reakcije izocitrat dehidrogenaze, izocitratna kiselina se dekarboksilira. NAD-ovisna izocitrat dehidrogenaza je alosterički enzim koji zahtijeva ADP kao specifični aktivator. Osim toga, enzim zahtijeva ione Mg 2+ ili Mn 2+ da bi pokazao svoju aktivnost.
U četvrtoj reakciji α-ketoglutarna kiselina se oksidativno dekarboksilira u sukcinil-CoA. Mehanizam ove reakcije sličan je reakciji oksidativne dekarboksilacije piruvata u acetil-CoA. Kompleks α-ketoglutarat dehidrogenaze sličan je po strukturi kompleksu piruvat dehidrogenaze. U oba slučaja u reakciji sudjeluje pet koenzima: TDP, amid lipoične kiseline, HS-CoA, FAD i NAD. Ukupno se ova reakcija može napisati na sljedeći način:

Petu reakciju katalizira enzim sukcinil-CoA sintetaza. Tijekom ove reakcije sukcinil-CoA, uz sudjelovanje GDP-a i anorganskog fosfata, pretvara se u jantarnu kiselinu (sukcinat). Istodobno dolazi do stvaranja visokoenergetske fosfatne veze GTP1 zbog visokoenergetske tioesterske veze sukcinil-CoA:

(Rezultirajući GTP zatim predaje svoju terminalnu fosfatnu skupinu ADP-u, što rezultira stvaranjem ATP-a. Stvaranje visokoenergetskog nukleozid trifosfata tijekom reakcije sukcinil-CoA sintetaze primjer je fosforilacije na razini supstrata.)
U šestoj reakciji sukcinat se dehidrogenira u fumarnu kiselinu. Oksidaciju sukcinata katalizira sukcinat dehidrogenaza u čijoj je molekuli koenzim FAD kovalentno vezan na protein:

U sedmoj reakciji nastala fumarna kiselina se hidratizira pod utjecajem enzima fumarat hidrataze. Produkt ove reakcije je jabučna kiselina (malat). Treba napomenuti da je fumarat hidrataza stereospecifična - tijekom ove reakcije nastaje L-jabučna kiselina:

Konačno, u osmoj reakciji ciklusa trikarboksilne kiseline, pod utjecajem mitohondrijske NAD-ovisne malat dehidrogenaze, L-malat se oksidira u oksaloacetat:

Kao što vidite, u jednom krugu ciklusa, koji se sastoji od osam enzimskih reakcija, dolazi do potpune oksidacije ("izgaranja") jedne molekule acetil-CoA. Za neprekidan rad ciklusa potrebna je konstantna opskrba sustava acetil-CoA, a koenzimi (NAD i FAD), koji su prešli u reducirano stanje, moraju se uvijek iznova oksidirati. Ta se oksidacija događa u sustavu prijenosa elektrona (ili lancu respiratornih enzima) koji se nalazi u mitohondrijima.
Energija koja se oslobađa kao rezultat oksidacije acetil-CoA uglavnom je koncentrirana u visokoenergetskim fosfatnim vezama ATP-a. Od četiri para atoma vodika, tri para se prenose kroz NAD u sustav prijenosa elektrona; u ovom slučaju za svaki par u biološkom oksidacijskom sustavu nastaju tri molekule ATP (u procesu konjugirane oksidativne fosforilacije), dakle ukupno devet molekula ATP. Jedan par atoma ulazi u sustav prijenosa elektrona kroz FAD, što rezultira stvaranjem 2 ATP molekule. Tijekom reakcija Krebsovog ciklusa sintetizira se i 1 molekula GTP-a, što je ekvivalentno 1 molekuli ATP-a. Dakle, oksidacija acetil-CoA u Krebsovom ciklusu proizvodi 12 ATP molekula.

Kao što je već navedeno, 1 molekula NADH 2 (3 molekule ATP) nastaje tijekom oksidativne dekarboksilacije piruvata u acetil-CoA. Budući da razgradnjom jedne molekule glukoze nastaju dvije molekule piruvata, kada se one oksidiraju u 2 molekule acetil-CoA i nakon dva zavoja ciklusa trikarboksilne kiseline, sintetizira se 30 molekula ATP-a (dakle, oksidacija jedne molekule piruvata u CO 2 i H 2 O proizvodi 15 molekula ATP).
Tome treba dodati 2 molekule ATP nastale tijekom aerobne glikolize, te 4 molekule ATP sintetizirane oksidacijom 2 molekule ekstramitohondrijskog NADH 2, koje nastaju oksidacijom 2 molekule gliceraldehid-3-fosfata u reakciji dehidrogenaze. Ukupno nalazimo da kada se 1 molekula glukoze razgradi u tkivima prema jednadžbi: C 6 H 12 0 6 + 60 2 -> 6CO 2 + 6H 2 O, sintetizira se 36 molekula ATP-a, što doprinosi akumulaciji adenozin trifosfat u visokoenergetskim fosfatnim vezama 36 X 34,5 ~ 1240 kJ (ili, prema drugim izvorima, 36 X 38 ~ 1430 kJ) slobodna energija. Drugim riječima, od sve slobodne energije koja se oslobađa tijekom aerobne oksidacije glukoze (oko 2840 kJ), do 50% se akumulira u mitohondrijima u obliku koji se može koristiti za obavljanje različitih fizioloških funkcija. Nema sumnje da je energetski potpuna razgradnja glukoze učinkovitiji proces od glikolize. Treba napomenuti da molekule NADH 2 nastale tijekom pretvorbe gliceraldehid-3-fosfata 2 naknadno, nakon oksidacije, ne proizvode 6 molekula ATP-a, već samo 4. Činjenica je da same molekule ekstramitohondrijskog NADH 2 nisu u stanju prodiru kroz membranu u mitohondrije. Međutim, elektroni koje doniraju mogu se uključiti u mitohondrijski lanac biološke oksidacije korištenjem takozvanog glicerofosfatnog mehanizma prijenosa (Slika 92). Kao što se može vidjeti na slici, citoplazmatski NADH 2 prvo reagira s citoplazmatskim dihidroksiaceton fosfatom da bi se formirao glicerol 3-fosfat. Reakciju katalizira NAD-ovisna citoplazmatska glicerol-3-fosfat dehidrogenaza.
Kratki povijesni podaci
Naš najdraži ciklus je TCA ciklus, odnosno ciklus trikarboksilne kiseline - život na Zemlji i pod Zemljom i u Zemlji... Stanite, općenito ovo je najčudesniji mehanizam - univerzalan je, način je oksidacije produkti razgradnje ugljikohidrata, masti, proteina u stanicama živih organizama, kao rezultat Dobivamo energiju za aktivnosti našeg tijela.
Sam Hans Krebs je otkrio ovaj proces, za koji je dobio Nobelova nagrada!
Rođen je 25. kolovoza 1900. godine u njemačkom gradu Hildesheimu. Primljeno medicinsko obrazovanje Sveučilište u Hamburgu, nastavilo biokemijska istraživanja pod vodstvom Otta Warburga u Berlinu.
Godine 1930. zajedno sa svojim učenikom otkrio je proces neutralizacije amonijaka u tijelu, koji je bio prisutan u mnogim predstavnicima živog svijeta, pa tako i u čovjeku. Ovaj ciklus je ciklus uree, koji je također poznat kao Krebsov ciklus #1.
Kada je Hitler došao na vlast, Hans je emigrirao u Veliku Britaniju, gdje nastavlja studirati znanost na sveučilištima u Cambridgeu i Sheffieldu. Razvijajući istraživanja mađarskog biokemičara Alberta Szent-Györgyija, on je dobio uvid i napravio najpoznatiji Krebsov ciklus br. 2, odnosno “Szent-Györgyö – Krebsov ciklus” - 1937. godine.
Rezultati istraživanja šalju se časopisu Nature, koji odbija objaviti članak. Zatim tekst leti u časopis "Enzymologia" u Nizozemskoj. Krebs je 1953. dobio Nobelovu nagradu za fiziologiju ili medicinu.
Otkriće je bilo iznenađujuće: 1935. godine Szent-Györgyi je otkrio da jantarna, oksaloctena, fumarna i jabučna kiselina (sve 4 kiseline su prirodne kemijske komponente životinjskih stanica) pojačavaju proces oksidacije u prsnom mišiću goluba. Koja je bila isjeckana.
U njemu se metabolički procesi odvijaju najvećom brzinom.
F. Knoop i K. Martius 1937. godine otkrili su da se limunska kiselina pretvara u izocitričnu kiselinu preko međuproizvoda, cis - akonitske kiseline. Osim toga, izocitrična kiselina se može pretvoriti u a-ketoglutarnu kiselinu, a ona u jantarnu kiselinu.
Krebs je primijetio učinak kiselina na apsorpciju O2 od strane prsnog mišića goluba i identificirao aktivirajući učinak na oksidaciju PVC-a i stvaranje acetil-koenzima A. Osim toga, procesi u mišićima bili su inhibirani malonskom kiselinom , koji je sličan jantarnoj kiselini i mogao bi kompetitivno inhibirati enzime čiji je supstrat jantarna kiselina .
Kada je Krebs dodao malonsku kiselinu u reakcijski medij, počelo je nakupljanje a-ketoglutarne, limunske i sukcinske kiseline. Stoga je jasno da kombinirano djelovanje a-ketoglutarne i limunske kiseline dovodi do stvaranja jantarne kiseline.
Hans je ispitao više od 20 drugih tvari, ali one nisu utjecale na oksidaciju. Uspoređujući dobivene podatke, Krebs je dobio ciklus. U samom početku istraživač nije mogao sa sigurnošću reći je li proces započeo s limunskom ili izocitričnom kiselinom, pa ga je nazvao "ciklus trikarboksilne kiseline".
Sada znamo da je prva limunska kiselina, pa je točan naziv citratni ciklus ili ciklus limunske kiseline.
U eukariota se reakcije TCA ciklusa odvijaju u mitohondrijima, dok se svi enzimi za katalizu, osim 1, nalaze u slobodnom stanju u matriksu mitohondrija; iznimka je sukcinat dehidrogenaza, koja je lokalizirana na unutarnjoj membrani mitohondrija i ugrađena je u lipidni dvosloj. U prokariota se reakcije ciklusa odvijaju u citoplazmi.
Upoznajmo sudionike ciklusa:
1) Acetil koenzim A:- acetilna skupina
- koenzim A - koenzim A:
2) ŠTUKA – Oksaloacetat – Oksaloctena kiselina:
čini se da se sastoji od dva dijela: oksalne i octene kiseline.
3-4) Limunska i izocitrična kiselina:
5) a-ketoglutarna kiselina:
6) sukcinil-koenzim A:
7) Jantarna kiselina:
8) Fumarna kiselina:
9) Jabučna kiselina:
Kako nastaju reakcije? Općenito, svi smo navikli na izgled prstena, koji je prikazan ispod na slici. U nastavku je sve opisano korak po korak:
1. Kondenzacija acetil koenzima A i oksaloctene kiseline ➙ limunske kiseline.
Transformacija acetil koenzima A počinje kondenzacijom s oksalooctenom kiselinom, što rezultira stvaranjem limunske kiseline.
Reakcija ne zahtijeva potrošnju ATP-a, budući da se energija za ovaj proces osigurava kao rezultat hidrolize tioeterske veze s acetil koenzimom A, koji je visokoenergetski:
2. Limunska kiselina prelazi kroz cis-akonitnu kiselinu u izocitričnu kiselinu.
Dolazi do izomerizacije limunske kiseline u izocitričnu kiselinu. Pretvorbeni enzim - akonitaza - prvo dehidrira limunsku kiselinu da nastane cis-akonitna kiselina, zatim povezuje vodu s dvostrukom vezom metabolita, stvarajući izocitričnu kiselinu:
3. Izocitrična kiselina se dehidrogenira u α-ketoglutarnu kiselinu i CO2.
Izocitričnu kiselinu oksidira specifična dehidrogenaza, čiji je koenzim NAD.
Istodobno s oksidacijom dolazi do dekarboksilacije izocitrične kiseline. Kao rezultat transformacija nastaje α-ketoglutarna kiselina.
4. Alfa-ketoglutarnu kiselinu dehidrogeniraju ➙ sukcinil-koenzim A i CO2.
Sljedeća faza je oksidativna dekarboksilacija α-ketoglutarne kiseline.
Kataliziran kompleksom α-ketoglutarat dehidrogenaze, koji je po mehanizmu, strukturi i djelovanju sličan kompleksu piruvat dehidrogenaze. Kao rezultat nastaje sukcinil-CoA.
5. Sukcinil koenzim A ➙ jantarna kiselina.
Sukcinil-CoA se hidrolizira u slobodnu jantarnu kiselinu, a oslobođena energija se pohranjuje stvaranjem gvanozin trifosfata. Ova faza je jedina u ciklusu u kojoj se energija izravno oslobađa.
6. Jantarna kiselina je dehidrogenirana ➙ fumarna kiselina.
Dehidrogenaciju jantarne kiseline ubrzava sukcinat dehidrogenaza, čiji je koenzim FAD.
7. Fumarna kiselina je hidratizirana ➙ jabučna kiselina.
Fumarna kiselina, koja nastaje dehidrogenacijom jantarne kiseline, hidratizira se i nastaje jabučna kiselina.
8. Jabučna kiselina se dehidrogenira ➙ Oksalno-octena kiselina – ciklus se zatvara.
Konačni proces je dehidrogenacija jabučne kiseline, koju katalizira malat dehidrogenaza;
Rezultat stadija je metabolit s kojim započinje ciklus trikarboksilne kiseline - oksalno-octena kiselina.
U reakciji 1 sljedećeg ciklusa ući će još jedna količina acetil koenzima A.
Kako zapamtiti ovaj ciklus? Samo!
1) Vrlo figurativan izraz:Cijeli ananas i komad souffléa zapravo su moj današnji ručak, što odgovara - citratu, cis-akonitatu, izocitratu, (alfa-)ketoglutaratu, sukcinil-CoA, sukcinatu, fumaratu, malatu, oksaloacetatu.
2) Još jedna duga pjesma:
ŠTUKA je pojela acetat, ispalo je citrat,
Kroz cisakonitat će postati izocitrat.
Prepustivši vodik NAD-u, gubi CO2,
Alfa-ketoglutarat je izuzetno sretan zbog toga.
Dolazi oksidacija - NAD je ukrao vodik,
TDP, koenzim A uzima CO2.
A energija se jedva pojavila u sukcinilu,
Odmah je rođen ATP, a ono što je ostalo bio je sukcinat.
Sada je došao do FAD-a - treba mu vodik,
Fumarat je popio vodu i pretvorio se u malat.
Zatim je NAD došao do malata, stekao vodik,
ŠTUKA se opet pojavila i tiho sakrila.
3) Izvorna pjesma - ukratko:
ŠTUKA ACETIL LIMONIL,
Ali konj se bojao narcisa,
On je iznad njega ISOLIMON
ALFA - KETOGLUTARAZID.
SUKCINALIZIRAN KOENZIMOM,
JANTAR FUMAROVO,
Spremio JABUKE za zimu,
Ponovno se pretvorio u ŠTUKU.
CIKLUS TRIKARBOKSILNIH KISELINA (KREBSOV CIKLUS)
Ciklus trikarboksilnih kiselina prvi je otkrio engleski biokemičar G. Krebs. Bio je prvi koji je pretpostavio važnost ovog ciklusa za potpuno izgaranje piruvata, čiji je glavni izvor glikolitička transformacija ugljikohidrata. Kasnije se pokazalo da ciklus trikarboksilnih kiselina kiseline je središte u kojem se spajaju gotovo svi metabolički putovi. Tako, Krebsov ciklus– zajednički završni put oksidacija acetil skupine (u obliku acetil-CoA) u koje se pretvara tijekom procesa katabolizam najviše organski molekule, igrajući ulogu „staničnog gorivo»: ugljikohidrata, masne kiseline I aminokiseline.
Nastaje kao rezultat oksidativnog dekarboksilacija piruvat u mitohondrije ulazi acetil-CoA Krebsov ciklus. Ovaj ciklus se događa u matrici mitohondrije a sastoji se od osam uzastopne reakcije(Slika 10.9). Ciklus počinje dodavanjem acetil-CoA oksaloacetatu i stvaranjem limunska kiselina (citrat). Zatim limunska kiselina(spoj sa šest ugljika) po serijama dehidrogenacije(oduzimanje vodik) i dva dekarboksilacije(eliminacija CO 2) gubi dva ugljika atom i opet unutra Krebsov ciklus pretvara u oksaloacetat (spoj s četiri ugljika), tj. kao rezultat pune revolucije ciklusa jedan molekula acetil-CoA izgara do CO 2 i H 2 O, i molekula oksalacetat se regenerira. Pogledajmo svih osam uzastopne reakcije(faze) Krebsov ciklus.
Riža. 10.9.Ciklus trikarboksilnih kiselina (Krebsov ciklus).
Prvi reakcija katalizirano enzim cit-rat sintaza, dok acetil acetil-CoA skupina kondenzira s oksaloacetatom, što rezultira stvaranjem limunska kiselina:

Očigledno, u ovom reakcije kao međuprodukt nastaje udružen s enzim citril-CoA. Zatim potonji spontano i nepovratno hidrolizira u obliku citrat i HS-CoA.
Kao rezultat toga, drugi reakcije formirana limunska kiselina podvrgava se dehidraciji stvarajući cis-akonitic kiseline, koji, dodavanjem molekula voda, Ide na izocitrična kiselina(izocitrat). Katalizira ove reverzibilne reakcije hidratacija–dehidracija enzim akonitat hidrataza (akonitaza). Kao rezultat, dolazi do međusobnog kretanja H i OH molekula citrat:

Treći reakcija, očito ograničava brzinu Krebsov ciklus. Izocitrična kiselina dehidrogenirano u prisutnosti NAD-ovisne izocitrat dehidrogenaze.

Tijekom izocitrat dehidrogenaze reakcije izocitrična kiselina istovremeno dekarboksiliran. NAD-ovisna izocitrat dehidrogenaza je alosterična enzim, koji kao specifičan aktivator potrebno ADF. Osim, enzim pokazati svoje aktivnost treba ioni Mg 2+ ili Mn 2+.
Tijekom četvrtog reakcije dolazi do oksidativne dekarboksilacije α-ketoglutarne kiseline uz nastanak visokoenergetskog spoja sukcinil-CoA. Mehanizam ovoga reakcije slično tome reakcije oksidativni dekarboksilacija piruvata u acetil-CoA, kompleks α-ketoglutarat dehidrogenaze svojom strukturom nalikuje kompleksu piruvat dehidrogenaze. I u jednom i u drugom slučaju u reakcije 5 sudjelovati koenzimi: TPP, amid lipoična kiselina, HS-KoA, FAD i NAD+.

Peti reakcija katalizirano enzim sukcinil-CoA-sintetazoi. Tijekom ovoga reakcije sukcinil-CoA uz sudjelovanje GTP i anorganski fosfat preobraziti se u jantarna kiselina (sukcinat). Istodobno dolazi do stvaranja visokoenergetske fosfatne veze GTP zbog visokoenergetske tioesterske veze sukcinil-CoA:

Kao rezultat toga, šesti reakcije sukcinat dehidrogenira u fumarna kiselina. Oksidacija sukcinat katalizirano sukcinat dehidrogenaza, V molekula koji sa proteinčvrsto (kovalentno) vezani koenzim FAD. Sa svoje strane sukcinat dehidrogenaza snažno povezan s unutarnjim mitohondrijem membrana:

Sedmi reakcija provodi pod utjecajem enzim fumarat hidrataza ( fumaraze). Dobivena fumarna kiselina hidratiziran po proizvodu reakcije je Jabučna kiselina(malat). Treba napomenuti da fumarat hidrataza ima stereospecifičnost(vidi poglavlje 4) – tijekom reakcije Nastaje L-jabučna kiselina:

Konačno, tijekom osmog reakcije ciklus trikarboksilnih kiselina pod utjecajem mitohondrijskog NAD-ovisan malat dehidrogenaza događa se oksidacija L-malat u oksalacetat:

Kao što se može vidjeti, tijekom jedne revolucije ciklusa koji se sastoji od osam enzimskih reakcije, dovršen oksidacija(“sagorijevanje”) jednog molekule acetil-CoA. Za neprekidan rad ciklusa potrebna je konstantna opskrba sustava acetil-CoA i koenzimi(NAD + i FAD), koji su prešli u reducirano stanje, moraju se uvijek iznova oksidirati. Ovaj oksidacija provodi u sustavu transportera elektroni V dišni lanac(V dišnih lanaca enzima), lokaliziran u membrana mitohondrije. Rezultirajući FADH 2 čvrsto je vezan na SDH, pa prenosi atomi vodik preko KoQ-a. Pušten kao rezultat oksidacija energija acetil-CoA uglavnom je koncentrirana u visokoenergetskim fosfatnim vezama ATP. od 4 pare atomi vodik 3 parovi prijenos NADH u transportni sustav elektroni; u isto vrijeme, po svakom par u biološkom sustavu oksidacija 3 se formira molekule ATP(u procesu konjugacije ), dakle ukupno 9 molekule ATP(vidi poglavlje 9). Jedan par atomi iz sukcinat dehidrogenaze-FADH 2 ulazi u transportni sustav elektroni preko KoQ, što je rezultiralo sa samo 2 molekule ATP. Tijekom Krebsov ciklus sintetiziran je i jedan molekula GTP (supstrat fosforilacija), što je ekvivalentno jedan molekula ATP. Pa kad oksidacija jedan molekule acetil-CoA in Krebsov ciklus i sustav oksidativne fosforilacije može formirati 12 molekule ATP.
Ako izračunamo ukupni energetski učinak glikolitičkog cijepanja glukoza i naknadni oksidacija formirana su dva molekule piruvata u CO 2 i H 2 O, tada će se pokazati da je mnogo veći.
Kao što je navedeno, jedan molekula NADH (3 molekule ATP) nastaje tijekom oksidacije dekarboksilacija piruvata u acetil-CoA. Kad se jedan razdvoji molekule glukoza 2 se formira molekule piruvat, a kada oksidacija ima ih do 2 molekule acetil-CoA i sljedeća 2 zavoja ciklus trikarboksilnih kiselina sintetizirano 30 molekule ATP(stoga, oksidacija molekule piruvat u CO 2 i H 2 O daje 15 molekule ATP). Ovoj količini potrebno je dodati 2 molekule ATP, nastale tijekom aerobika glikoliza i 6 molekule ATP, sintetiziran zbog oksidacija 2 molekule ekstramitohondrijski NADH, koji nastaju tijekom oksidacija 2 molekule gliceraldehid-3-fosfat u dehidrogenazi reakcije glikoliza. Stoga se kod cijepanja na tkanine jedan molekule glukoza prema jednadžbi C 6 H 12 O 6 + 6O 2 -> 6CO 2 + 6H 2 O sintetizira se 38 molekule ATP. Nema sumnje da je, energetski, potpuni rascjep glukoza je učinkovitiji proces od anaerobnog glikoliza.
Treba napomenuti da nastali gliceraldehid-3-fosfat 2 molekule NADH naknadno oksidacija možda neće dati 6 molekule ATP, ali samo 4. Činjenica je da su oni sami molekule ekstramitohondrijski NADH ne mogu prodrijeti membrana iznutra mitohondrije. Međutim, ono što daju elektroni mogu se uključiti u mitohondrijski lanac bioloških oksidacija korištenjem tzv. glicerol fosfat shuttle mehanizma (slika 10.10). Citoplazmatski NADH najprije reagira s citoplazmatskim di-hidroksiaceton fosfatom stvarajući glicerol-3-fosfat. Reakcija katalitički

Riža. 10.10. Glicerol fosfat shuttle mehanizam. Objašnjenje u tekstu.
kontrolira NAD-ovisna citoplazmatska glicerol-3-fosfat dehidrogenaza:
Dihidroksiaceton fosfat + NADH + H +<=>Glicerol 3-fosfat + NAD + .
Nastali glicerol-3-fosfat lako prodire u mitohondrije membrana. Iznutra mitohondrije druga (mitohondrijska) glicerol-3-fosfat dehidrogenaza (flavin enzim) ponovno oksidira glicerol-3-fosfat u dihidroksiaceton fosfat:
Glicerol-3-fosfat + FAD<=>Dihidroksiaceton fosfat + FADN 2.
Obnovljen flavoprotein(enzim-FADH 2) uvodi na razini KoQ stečenog njime elektroni u biološki lanac oksidacija i s njim povezano oksidativne fosforilacije, a iz njega izlazi dihidroksiaceton fosfat mitohondrije V citoplazma a opet može stupiti u interakciju s citoplazmatskim NADH + H + . Tako, par elektroni(od jednog molekule citoplazmatski NADH + H +), uveden u dišni lanac koristeći glicerol fosfat shuttle mehanizam, ne daje 3, već 2 ATP.

Riža. 10.11. Malat-aspartatni shuttle sustav za prijenos redukcijskih ekvivalenata iz citosolnog NADH u mitohondrijski matriks. Objašnjenje u tekstu.
Naknadno je pokazano da se uz pomoć ovog mehanizma prijenosa samo u skeletnim mišićima i mozgu odvija prijenos reduciranih ekvivalenata iz citosolnog NADH + H + u mitohondrije.
U Stanice jetra, bubrega i srca, radi složeniji malat-as-partat shuttle sustav. Rad takvog mehanizma shuttle postaje moguć zbog prisutnosti malat dehidrogenaza i as-partat aminotransferaze i u citosolu i u mitohondrije.
Utvrđeno je da su reducirani ekvivalenti iz citosolnog NADH + H + prvi uz sudjelovanje enzim malat dehidrogenaza(Sl. 10.11) prenose se u citosolni oksaloacetat. Kao rezultat toga nastaje malat koji uz pomoć transportnog sustava dikarboksilne kiseline, prolazi kroz unutarnju membrana mitohondrije u matricu. Ovdje se malat oksidira u oksaloacetat, a matriks NAD + se reducira u NADH + H +, koji sada može prenijeti svoje elektroni V dišni lanac enzima, lokaliziran na unutarnjoj membrana mitohondrije. Zauzvrat, dobiveni oksaloacetat u prisutnosti glutamata i enzim ASAT ulazi u reakcija transaminacija. Nastali aspartat i α-ketoglutarat, uz pomoć posebnih transportnih sustava, mogu proći kroz membrana mitohondrije.
Transport u citosolu regenerira oksaloacetat, koji pokreće sljedeći ciklus. Općenito, proces uključuje lako reverzibilan reakcije, odvija se bez utroška energije, njegova "pokretačka sila" je konstantna oporavak NAD + u citosolu gliceraldehid-3-fosfatom, nastalim tijekom katabolizam glukoza.
Dakle, ako mehanizam malat-aspartat funkcionira, onda kao rezultat potpune oksidacija jedan molekule glukoza može se formirati ne 36, već 38 molekule ATP(Tablica 10.1).

U tablici 10.1 reakcije, u kojem se tijekom formiranja visokoenergetskih fosfatnih veza katabolizam glukoza, što ukazuje na učinkovitost procesa u aerobnim i anaerobnim uvjetima
Ministarstvo obrazovanja Ruske Federacije
Samara Državno tehničko sveučilište
Zavod za organsku kemiju
Sažetak na temu:
"CIKLUS TRIKARBOKSILNIH KISELIN (KREBSOV CIKLUS)"
Završio student: III – NTF – 11
Eroshkina N.V.
Provjerio sam.