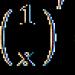Krv ima odlučujuću ulogu u održavanju acidobazne ravnoteže, čija promjena može dovesti do razvoja patoloških stanja ili smrti tijela. Stoga u tijelu postoje posebni sustavi koji sprječavaju promjenu pH vrijednosti krvi i drugih bioloških tekućina pri stvaranju kiselih i alkalnih produkata ili pri velikom unosu vode. Tu ulogu imaju pojedini fiziološki sustavi (dišni, ekskretorni), kao i puferski sustavi. Potonji vrlo brzo (unutar nekoliko sekundi) reagiraju na promjene koncentracija H + i OH - u vodenim sredinama i hitni su regulatori kiselinsko-baznog stanja u tkivima tijela.
Puferski sustavi je mješavina slabe kiseline i njezine topive soli, dviju soli ili proteina koji mogu spriječiti promjene pH vrijednosti vodenog medija. Djelovanje puferskih sustava usmjereno je na vezanje viška H + ili OH - u mediju i održavanje konstantnog pH medija. Kada puferski sustav djeluje, nastaju slabo disocibilne tvari ili voda. Glavni puferski sustavi krvi uključuju bikarbonat, protein (hemoglobin) i fosfat. Dostupni su i acetatni i amonijevi puferski sustavi.
Bikarbonat međuspremnički sustav - snažan i najkontroliraniji sustav krvi i izvanstanične tekućine. Čini oko 10% ukupnog puferskog kapaciteta krvi. Bikarbonatni sustav je konjugirani acidobazni par koji se sastoji od molekule ugljične kiseline H 2 CO 3, koja djeluje kao donor protona, i bikarbonatnog iona HCO 3 -, koji djeluje kao akceptor protona:
SO 2 + N 2 O ↔ N 2 SO 3 ↔ N + + NSO 3 -
Prava koncentracija nedisociranih molekula H 2 CO 3 u krvi je beznačajna i izravno ovisi o koncentraciji otopljenog CO 2. Pri normalnom pH krvi (7,4), koncentracija bikarbonatnih iona HCO 3 - u krvnoj plazmi premašuje koncentraciju CO 2 za približno 20 puta. Bikarbonatni puferski sustav djeluje kao učinkovit regulator u pH području = 7,4. Mehanizam djelovanja ovog sustava je da kada se relativno velike količine kiselih produkata otpuštaju u krv, protoni H + stupaju u interakciju s bikarbonatnim ionima HCO 3 -, što dovodi do stvaranja slabo disocirabilnog H 2 CO 3.
Naknadno smanjenje koncentracije H 2 CO 3 postiže se kao rezultat ubrzanog oslobađanja CO 2 kroz pluća kao rezultat njihove hiperventilacije. Ako se količina baza u krvi poveća, tada one u interakciji sa slabom ugljičnom kiselinom stvaraju bikarbonatne ione i vodu. U tom slučaju ne dolazi do zamjetnih promjena pH vrijednosti. Osim toga, za održavanje normalnog omjera između komponenti puferskog sustava, u ovom slučaju, aktiviraju se fiziološki mehanizmi za regulaciju acidobazne ravnoteže: određena količina CO 2 zadržava se u krvnoj plazmi kao rezultat hipoventilacije pluća. Bikarbonatni sustav je usko povezan sa sustavom hemoglobina.
Sustav fosfatnog pufera je konjugirani acidobazni par koji se sastoji od H 2 PO 4 - iona (donor protona, djeluje kao kiselina) i HPO 4 2- iona (akceptor protona, djeluje kao sol). Fosfatni puferski sustav čini samo 1% puferskog kapaciteta krvi. U drugim tkivima ovaj sustav je jedan od glavnih. Sustav fosfatnog pufera sposoban je utjecati na promjene pH vrijednosti u rasponu od 6,1 do 7,7 i može osigurati određeni kapacitet unutarstanične tekućine čija je pH vrijednost u rasponu od 6,9-7,4. U krvi se maksimalni kapacitet fosfatnog pufera pojavljuje oko vrijednosti 7,2. Organski fosfati također imaju svojstva puferiranja, ali njihova je moć slabija od snage anorganskih fosfatnih pufera.
Proteinski puferski sustav je manje važan za održavanje acidobazne ravnoteže u krvnoj plazmi od drugih puferskih sustava. Proteini tvore puferski sustav zbog prisutnosti acidobaznih skupina u proteinskoj molekuli: protein-H + (kiselina, donor protona) i protein (konjugirana baza, akceptor protona). Proteinski puferski sustav krvne plazme učinkovit je u pH rasponu od 7,2-7,4.
Puferski sustav hemoglobina- najsnažniji puferski sustav krvi, koji čini 75% ukupnog puferskog sustava. Sudjelovanje hemoglobina u regulaciji pH krvi povezano je s njegovom ulogom u prijenosu kisika i ugljičnog dioksida. Kada se zasiti kisikom, hemoglobin postaje jača kiselina (HHbO 2). Hemoglobin, odustajući od kisika, prelazi u vrlo slabu organsku kiselinu (HHb).
Puferski sustav hemoglobina sastoji se od neioniziranog hemoglobina HHb (slaba organska kiselina, donor protona) i kalijeve soli hemoglobina KHb (konjugirana baza, akceptor protona). Puferski sustav oksihemoglobina može se razmatrati na isti način. Hemoglobinski sustav i oksihemoglobinski sustav međusobno su konvertibilni sustavi i postoje kao jedinstvena cjelina. Svojstva puferiranja hemoglobina posljedica su mogućnosti interakcije kiselih spojeva s kalijevom soli hemoglobina:
KHb + H 2 CO 3 => KHCO 3 + HHb.
Time se osigurava održavanje pH krvi unutar fiziološki prihvatljivih vrijednosti, unatoč ulasku velike količine CO 2 i drugih kiselih metaboličkih produkata u vensku krv. Hemoglobin (HHb), ulazeći u kapilare pluća, pretvara se u oksihemoglobin (HHbO 2), što dovodi do određenog zakiseljavanja krvi, istiskivanja dijela H 2 CO 3 iz bikarbonata i smanjenja alkalne rezerve krvi.
Respiratorna funkcija krvi. Važna funkcija krvi je njezina sposobnost prijenosa kisika do tkiva i CO 2 od tkiva do pluća. Tvar koja obavlja ovu funkciju je hemoglobin. Hemoglobin je sposoban apsorbirati O2 pri relativno visokom sadržaju u atmosferskom zraku i lako ga otpustiti kada se parcijalni tlak O2 smanji:
Nb + O 2 ↔ NbO.
Stoga je u plućnim kapilarama krv zasićena O 2, dok se u kapilarama tkiva, gdje se njezin parcijalni tlak naglo smanjuje, opaža obrnuti proces - krv otpušta kisik u tkiva.
CO 2 koji nastaje u tkivima tijekom oksidativnih procesa mora se eliminirati iz organizma. Ovu izmjenu plinova osigurava nekoliko tjelesnih sustava.
Najveću važnost imaju vanjsko, ili plućno, disanje, koje osigurava usmjerenu difuziju plinova kroz alveolokapilarne pregrade u plućima i izmjenu plinova između vanjskog zraka i krvi; respiratorna funkcija krvi, ovisna o sposobnosti otapanja plazme i sposobnosti hemoglobina da reverzibilno veže kisik i ugljikov dioksid; transportna funkcija kardiovaskularnog sustava (protok krvi), osiguravajući prijenos krvnih plinova iz pluća u tkiva i natrag; funkcija enzimskih sustava koja osigurava izmjenu plinova između krvi i stanica tkiva, tj. disanje tkiva.
Difuzija krvnih plinova događa se kroz staničnu membranu duž koncentracijskog gradijenta. Zbog ovog procesa dolazi do izravnavanja u alveolama pluća na kraju udaha. parcijalni pritisci razni plinovi u alveolarnom zraku i krvi. Izmjena s atmosferskim zrakom tijekom naknadnog izdisaja i udisaja opet dovodi do razlika u koncentraciji plinova u alveolarnom zraku iu krvi, zbog čega kisik difundira u krv, a ugljični dioksid iz krvi.
Najveći dio O 2 i CO 2 prenosi se u obliku njihove veze s hemoglobinom u obliku molekula HbO 2 i HbCO 2 . Maksimalna količina kisika koju veže krv kada je hemoglobin potpuno zasićen kisikom naziva se kisikov kapacitet krvi. Normalno se njegova vrijednost kreće od 16,0-24,0 vol.% i ovisi o sadržaju hemoglobina u krvi, čiji 1 g može vezati 1,34 ml kisika (Hüfnerov broj).
Vezanje kisika za hemoglobin je reverzibilan proces koji ovisi o napetosti kisika u krvi, kao io drugim čimbenicima, posebice o pH krvi.
CO 2 stvoren u tkivima prelazi u krv krvnih kapilara, zatim difundira u eritrocit, gdje se pod utjecajem karboanhidraze pretvara u ugljičnu kiselinu, koja disocira na H + i HCO 3 -. HCO 3 - djelomično difundira u krvnu plazmu, stvarajući natrijev bikarbonat. Kada krv uđe u pluća (poput HCO 3 - iona sadržanih u crvenim krvnim stanicama), ona stvara CO 2, koji difundira u alveole.
Oko 80% ukupne količine CO 2 prenosi se iz tkiva u pluća u obliku bikarbonata, 10% u obliku slobodno otopljenog ugljičnog dioksida i 10% u obliku karboksihemoglobina. Karboksihemoglobin disocira u plućnim kapilarama na hemoglobin i slobodni CO 2 koji se uklanja izdahnutim zrakom. Oslobađanje CO 2 iz veze s hemoglobinom olakšava se transformacijom potonjeg u oksihemoglobin, koji je, s izraženim kiselim svojstvima, sposoban pretvoriti bikarbonate u ugljičnu kiselinu, koja disocira u molekule vode i CO 2.
Hipoksemija se razvija kada nema dovoljnog zasićenja krvi kisikom. , što je popraćeno razvojem hipoksije, tj. nedovoljna opskrba tkiva kisikom. Teški oblici hipoksemije mogu izazvati potpuni prekid dostave kisika u tkiva, a zatim se razvija anoksija, u tim slučajevima dolazi do gubitka svijesti, što može rezultirati smrću.
Patologija izmjene plinova povezana s poremećenim transportom plinova između pluća i tjelesnih stanica opaža se kada se plinski kapacitet krvi smanjuje zbog nedostatka ili kvalitativnih promjena hemoglobina, a manifestira se u obliku anemične hipoksije. Kod anemije se kisikov kapacitet krvi smanjuje proporcionalno padu koncentracije hemoglobina. Smanjenje koncentracije hemoglobina tijekom anemije također ograničava transport ugljičnog dioksida iz tkiva u pluća u obliku karboksihemoglobina.
Poremećaj transporta kisika u krvi također se javlja kod patologije hemoglobina, na primjer, s anemijom srpastih stanica, s inaktivacijom dijela molekula hemoglobina zbog njegove pretvorbe u methemoglobin, na primjer, s trovanjem nitratima (methemoglobinemija) ili u karboksihemoglobin ( trovanje CO).
Poremećaji u izmjeni plinova zbog smanjenja volumetrijske brzine protoka krvi u kapilarama javljaju se kod zatajenja srca, vaskularne insuficijencije (uključujući kolaps, šok), lokalnih poremećaja - kod vazospazma itd. U uvjetima stagnacije krvi koncentracija snižene povećava se hemoglobin. Kod srčanog zatajenja ova je pojava posebno izražena u kapilarama udaljenih dijelova tijela od srca, gdje je krvotok najsporiji, što se klinički očituje akrocijanozom.
Primarni poremećaj izmjene plinova na staničnoj razini opaža se uglavnom kada je izložen otrovima koji blokiraju respiratorne enzime. Kao rezultat toga, stanice gube sposobnost korištenja kisika i razvija se teška hipoksija tkiva, što dovodi do strukturne dezorganizacije subcelularnih i staničnih elemenata, sve do nekroze. Kršenje staničnog disanja može biti uzrokovano nedostatkom vitamina, na primjer, nedostatkom vitamina B2, PP, koji su koenzimi respiratornih enzima.
Puferski sustavi su spojevi koji se suprotstavljaju naglim promjenama koncentracije H + iona. Svaki puferski sustav je kiselo-bazni par: slaba baza (anion, A –) i slaba kiselina (H-anion, H-A). Minimiziraju pomake u broju H + iona zbog njihovog vezanja na anion i uključivanja u slabo disocirajući spoj - slabu kiselinu. Stoga se ukupni broj H + iona ne mijenja tako značajno koliko bi mogao biti.
Postoje tri puferska sustava tjelesnih tekućina - bikarbonat, fosfat, protein(uključujući hemoglobin).Djeluju trenutno i nakon nekoliko minuta učinak im je maksimalan.
Sustav fosfatnog pufera
Fosfatni puferski sustav čini oko 2% ukupnog puferskog kapaciteta krvi i do 50% puferskog kapaciteta urina. Tvore ga hidrogenfosfat (HPO 4 2–) i dihidrogenfosfat (H 2 PO 4 –). Dihidrogenfosfat slabo disocira i ponaša se kao slaba kiselina; hidrogenfosfat ima alkalna svojstva. Normalno, omjer HPO 4 2– prema H 2 PO 4 – je 4:1.
Kada kiseline (H + ioni) stupaju u interakciju s disupstituiranim fosfatom (HPO 4 2‑), nastaje dihidrogen fosfat (H 2 PO 4 –):
Uklanjanje H+ iona fosfatnim puferom
Zbog toga se koncentracija H + iona smanjuje.
Kada baze uđu u krv (višak OH – ‑ grupa), one se neutraliziraju H + ionima koji ulaze u plazmu iz H 2 PO 4 – :

Uklanjanje alkalnih ekvivalenata fosfatnim puferom
Uloga fosfatnog pufera posebno je velika u unutarstaničnom prostoru i u lumenu bubrežnih tubula. Acidobazna reakcija urin ovisi samo o sadržaju dihidrogenfosfata (H2 PO4 –), jer natrijev bikarbonat se reapsorbira u bubrežnim tubulima.
Bikarbonatni puferski sustav
Ovaj sustav je najsnažniji i čini 65% ukupne snage puferiranja krvi. Sastoji se od bikarbonatnog iona (HCO 3 –) i ugljične kiseline (H 2 CO 3). Normalno, omjer HCO 3 - prema H 2 CO 3 je 20 : 1.
Kada ioni H + (tj. kiselina) uđu u krv, ioni natrijevog bikarbonata stupaju u interakciju s njim i nastaje ugljična kiselina:

Kada bikarbonatni sustav radi, koncentracija vodikovih iona se smanjuje, jer Ugljična kiselina je vrlo slaba kiselina i ne disocira lako. Istovremeno u krvi ne događa se paralelno značajno povećanje koncentracije HCO 3 – .
Ako tvari s alkalnim svojstvima uđu u krv, one reagiraju s ugljičnom kiselinom i stvaraju bikarbonatne ione:

Rad bikarbonatnog pufera neraskidivo je povezan s dišnim sustavom (s ventilacijom). U plućnim arteriolama uz smanjenje koncentracije CO 2 u plazmi i zbog prisutnosti enzima u eritrocitima karboanhidraza ugljična kiselina brzo se razgrađuje u CO 2 koji se uklanja s izdahnutim zrakom:
H 2 CO 3 → H 2 O + CO 2
Osim u eritrocitima, značajna aktivnost karboanhidraze zabilježena je u epitelu bubrežnih tubula, stanicama želučane sluznice, korteksu nadbubrežne žlijezde i stanicama jetre, u malim količinama - u središnjem živčani sustav, gušterača i drugi organi.
Proteinski puferski sustav
Proteini plazme su prvenstveno bjelanjak, igraju ulogu pufera zbog svojih amfoternih svojstava. Njihov doprinos puferiranju krvne plazme je oko 5%.
U kisela sredina disocijacija COOH skupina radikala aminokiselina (u asparaginskoj i glutaminskoj kiselini) je potisnuta, a NH 2 skupine (u argininu i lizinu) vežu višak H +. U tom slučaju protein postaje pozitivno nabijen.
U alkalni okolišu, povećava se disocijacija COOH‑skupina, H+ ioni koji ulaze u plazmu vežu višak OH‑iona i pH se održava. Proteini u ovom slučaju djeluju kao kiseline i negativno su nabijeni.

Promjena naboja proteinskih puferskih skupina pri različitim pH vrijednostima
Puferski sustav hemoglobina
Ima veliku snagu u krvi hemoglobinski pufer, čini do 28% ukupnog puferskog kapaciteta krvi. Kao kiselo dio pufera je oksigenirani hemoglobin H‑HbO2. Ima izražena kisela svojstva i 80 puta lakše otpušta vodikove ione nego reducirani H‑Hb, koji djeluje kao baza. Hemoglobinski pufer može se smatrati dijelom proteinskog pufera, ali njegova je značajka raditi u bliskom kontaktu s bikarbonatnim sustavom.
Promjena kiselosti hemoglobina događa se u tkivima i plućima, a uzrokovana je vezanjem H + odnosno O 2 . Izravni mehanizam djelovanja pufera je dodavanje ili donacija H + iona ostatak histidina u globinskom dijelu molekule (Bohrov efekt).
U tkivima je kiseliji pH normalno rezultat nakupljanja mineralnih (ugljične, sumporne, klorovodične) i organskih kiselina (mliječne). Kada se pH nadoknadi ovim puferom, H + ioni se vežu za nadolazeći oksihemoglobin (HbO 2) i pretvaraju ga u H‑HbO 2. To trenutačno uzrokuje oslobađanje kisika od oksihemoglobina (Bohrov učinak) i on se pretvara u smanjeni H-Hb.
HbO 2 + H + → → H-Hb + O 2
Zbog toga se smanjuje količina kiselina, prvenstveno H 2 CO 3, stvaraju se HCO 3 ioni i alkalizira tkivni prostor.
U plućima, nakon uklanjanja CO 2 (ugljične kiseline), krv se alkalizira. U ovom slučaju, adicijom O 2 na deoksihemoglobin H-Hb nastaje kiselina jača od ugljične kiseline. Donira svoje H + ione mediju, sprječavajući povećanje pH:
H-Hb + O 2 → → HbO 2 + H +
Rad hemoglobinskog pufera smatra se neodvojivo od bikarbonatnog pufera:

Fosfatni puferski sustav čini oko 1-2% ukupnog puferskog kapaciteta krvi i do 50% puferskog kapaciteta urina.
Tvori ga natrijev dihidrogenfosfat (NaH2PO4) i natrijev hidrogenfosfat (Na2HPO4).
Prvi spoj slabo disocira i ponaša se kao slaba kiselina, drugi ima alkalna svojstva.
Normalno, omjer HPO42– prema H2PO4– je 4:1.
Kada kiseline (vodikovi ioni) reagiraju s disupstituiranim natrijevim fosfatom (Na2HPO4), natrij se istiskuje i nastaje natrijeva sol dihidrogen fosfata (H2PO4–). Kao rezultat toga, zbog vezanja kiseline unesene u sustav, koncentracija vodikovih iona značajno se smanjuje.
HPO42– + H-anion > H2PO4– + anion–
Kada dođu baze, višak OH– skupina se neutralizira H+ prisutnim u mediju, a potrošnja H+ iona nadoknađuje se povećanjem disocijacije NaH2PO4.
H2PO4– + Kation-OH > Kation+ + HPO42– + H2O
Fosfatni pufer je od primarne važnosti za regulaciju pH intersticijske tekućine i urina.
U urinu, njegova uloga je očuvanje natrijevog bikarbonata zbog dodatnog iona vodika (u usporedbi s NaHCO3) u izlučenom NaH2PO4:
Na2HPO4 + N2SO3 > NaH2PO4 + NaNSO3
Kiselinsko-bazna reakcija urina ovisi samo o sadržaju dihidrogenfosfata, jer natrijev bikarbonat se reapsorbira u bubrežnim tubulima.
Proteinski puferski sustav
Puferski kapacitet ovog sustava je 5% ukupnog puferskog kapaciteta krvi.
Proteini plazme, prvenstveno albumin, imaju ulogu pufera zbog svojih amfoternih svojstava.
U kiseloj sredini, disocijacija COOH skupina je potisnuta, a NH2 skupine vežu višak H+, te protein postaje pozitivno nabijen.
U alkalna sredina Povećava se disocijacija karboksilnih skupina, nastali H+ veže višak OH– iona i pH se održava, proteini djeluju kao kiseline i negativno su nabijeni.
Puferski sustav hemoglobina
Najveću snagu ima hemoglobinski pufer, koji se može smatrati dijelom proteinskog pufera. Čini do 30% ukupnog puferskog kapaciteta krvi.
U puferskom sustavu hemoglobina značajnu ulogu igra histidin, koji se nalazi u proteinima u velikim količinama.
Izoelektrična točka histidina je 7,6, što hemoglobinu omogućuje lako prihvaćanje i lako otpuštanje vodikovih iona pri najmanjoj promjeni fiziološkog pH krvi (normalno 7,35-7,45).
Ovaj međuspremnik predstavlja nekoliko podsustava:

Par NNb/NNbO2 je glavni u radu pufera hemoglobina.
Spoj HHbO2 je jača kiselina u usporedbi s ugljičnom kiselinom, HHb je slabija kiselina od ugljične kiseline. Utvrđeno je da HHbO2 otpušta ione vodika 80 puta lakše nego HHb.
Dodatak vodikovih iona histidinskom ostatku deoksihemoglobina izgleda ovako:

Rad pufera hemoglobina neraskidivo je povezan s dišnim sustavom (na pitanje važnosti pranayame! - ALG)
U plućima, nakon uklanjanja CO2 (ugljične kiseline), krv se alkalizira.
U tom slučaju adicijom O2 na deoksihemoglobin H-Hb nastaje HHbO2 kiselina, koja je jača od ugljične kiseline. Otpušta svoje H+ ione u medij, sprječavajući povećanje pH:
N-Hb + O2 > > NbO2 + N+
U tkivnim kapilarama stalan dotok kiselina (uključujući ugljičnu kiselinu) iz stanica dovodi do disocijacije oksihemoglobina HbO2 (Bohrov učinak) i vezanja H+ iona u obliku H-Hb:
NbO2+ N+ > > N-Hb + O2
Dugoročna stabilizacija pH pomaka
Riječ je o takozvanoj fiziološkoj kompenzaciji acidobazne neravnoteže koja se prvenstveno događa zbog rada dišnog sustava i bubrega, a manjim dijelom zbog jetre i koštanog sustava.
Dišni sustav
Plućna ventilacija osigurava uklanjanje ugljične kiseline nastale tijekom rada bikarbonatnog puferskog sustava. Po brzini reakcije na promjene pH, ovo je drugi sustav nakon puferskih sustava.
Dodatna ventilacija pluća dovodi do uklanjanja CO2, a time i H2CO3, te povećava pH krvi, čime se kompenzira zakiseljavanje međustanične tekućine i krvne plazme produktima metabolizma, prvenstveno organskim kiselinama.
Pomaci u vrijednostima pO2 nisu jako značajni za promjene u plućnoj ventilaciji. Samo smanjenje pO2 na 8 kPa u arterijskoj krvi (norma je 11,04-14,36 kPa ili 83-108 mm Hg) dovodi do povećanja aktivnosti respiratornog centra.
Značajniji faktor za aktiviranje dišnog sustava je koncentracija H+ iona.
Akumulacija H+ iona u krvi unutar 1-2 minute uzrokuje maksimalnu (za određenu koncentraciju) stimulaciju respiratornog centra, povećavajući njegovu aktivnost do 4-5 puta, što dovodi do smanjenja pCO2 na 10-15 mm Hg. .
I obrnuto, smanjenje kiselosti krvi smanjuje aktivnost respiratornog centra za 50-75%, dok se pCO2 može povećati na 60 mm Hg i više.
Kost
Ovo je sustav koji najsporije reagira. Mehanizam njegovog sudjelovanja u regulaciji pH krvi je sposobnost izmjene Ca2+ i Na+ iona s krvnom plazmom u zamjenu za H+ protone. Dolazi do otapanja hidroksiapatitnih kalcijevih soli koštanog matriksa, otpuštanja iona Ca2+ i vezivanja iona HPO42– s H+ pri čemu nastaje dihidrogen fosfat koji se izlučuje mokraćom.
Paralelno sa smanjenjem pH (zakiseljavanje) ioni H+ ulaze u osteocite, a istječu ioni kalija.
Jetra
Značajnu, ali pasivnu ulogu u regulaciji kiselinsko-baznog stanja krvi preuzima jetra, u kojoj se odvija metabolizam organskih kiselina niske molekularne težine (mliječna kiselina, itd.). Osim toga, kiseli i alkalni ekvivalenti izlučuju se u žuč.
Bubrezi
Razvoj bubrežnog odgovora na promjenu acidobaznog stanja događa se unutar nekoliko sati.
Regulacija koncentracije H+ iona provodi se posredno, protokom Na+ iona koji se kreće duž koncentracijskog gradijenta, te preraspodjelom protoka K+ i H+ iona koji napuštaju epitelne stanice (luče se) u zamjenu za Na+ ione.
Također, kako bi se osigurala električna neutralnost unutarstanične i izvanstanične tekućine tijekom reapsorpcije Na+ iona, pojačana je reapsorpcija Cl– iona, ali ih nema dovoljno, pa je potrebno pojačati reapsorpciju i dodatnu sintezu HCO3. – ioni (i tu soda igra svoju ulogu – natrijev bikarbonat NaHCO3 Opskrbimo li tijelo dodatnim ionima HCO3 preko sode, značajno smanjujemo opterećenje bubrega i pomažemo im u radu – ALG)
U bubrezima se aktivno odvijaju tri procesa povezana s uklanjanjem kiselih ekvivalenata. Zahvaljujući ovim procesima, pH urina može se smanjiti na 4,5-5,2:
1. Reapsorpcija bikarbonatnih iona HCO3–.
2. Acidogeneza – uklanjanje H+ iona titrirajućim kiselinama (uglavnom u sastavu dihidrogenfosfata NaH2PO4).
3. Amoniogeneza – uklanjanje H+ iona u sastavu amonijevih iona NH4+.
Reapsorpcija bikarbonatnih iona
U proksimalnim tubulima ioni Na+ migriraju u citosol epitelnih stanica zahvaljujući koncentracijskom gradijentu koji se stvara na bazolateralnoj membrani tijekom djelovanja enzima Na+,K+ ATPaze.
U zamjenu za ione Na+, epitelne stanice tubula aktivno izlučuju vodikove ione u tubularnu tekućinu.
HCO3– ioni u primarnom urinu i izlučeni H+ ioni tvore ugljičnu kiselinu H2CO3.
U glikokaliksu epitelnih stanica enzim karboanhidraza katalizira razgradnju ugljične kiseline na CO2 i vodu.
Kao rezultat toga, između lumena tubula i citosola nastaje gradijent koncentracije ugljičnog dioksida, a CO2 difundira u stanice.
Unutarstanična karboanhidraza koristi ulazni CO2 i stvara ugljičnu kiselinu koja disocira.
HCO3– ioni se transportiraju u krv, H+ – ioni se izlučuju u urin u zamjenu za Na+ ione. Dakle, volumen reapsorpcije HCO3– u potpunosti odgovara izlučivanju H+ iona.

Proces reapsorpcije bikarbonatnih iona
Reapsorpcija 90% filtriranog HCO3– događa se u proksimalnim tubulima.
Preostala količina karbonatnog iona reapsorbira se u Henleovoj petlji i distalnim tubulima. Ukupno se više od 99% filtriranih bikarbonata reapsorbira u bubrežnim tubulima.
(Iz gore navedenog postaje očito da dodatni prihod u bikarbonatni ionski sustav zbog unosa natrijeve bikarbone – sode – smanjuje opterećenje ove strane bubrega. Što je više slobodnih bikarbonatnih iona u sustavu, to je tijelo manje ovisno o procesu njihove reapsorpcije. Sukladno tome, bubrezi nisu jako opterećeni po tom pitanju, zbog čega na kraju imamo urin s alkalnijom reakcijom! Poznato je da je kod novorođenčadi indeks urina blizu 8...ALG)
Acidogeneza
Tijekom procesa acidogeneze dnevno se putem mokraće izlučuje 10-30 mmol kiselina, koje se nazivaju titracijske kiseline.
Fosfati, kao jedna od tih kiselina, igraju ulogu puferskog sustava u urinu.
Uloga ovog sustava je izlučivanje kiselih ekvivalenata bez gubitka bikarbonatnih iona zbog dodatnog vodikovog iona u izlučenom NaH2PO4 (u usporedbi s NaHCO3):
Na2HPO4 + N2SO3 > NaH2PO4 + NaNSO3
Nakon što se natrijev bikarbonat reapsorbira u bubrežnim tubulima, kiselost urina ovisi samo o vezanju H+ iona na HPO42– i sadržaju dihidrogen fosfata.

Proces acidogeneze u bubrežnim tubulima
Iako je u krvi omjer HPO42– : H2PO4– 4:1, u glomerularnom filtratu mijenja se na 1:9.
To se događa jer se manje nabijeni H2PO4– bolje filtrira u glomerulima.
Vezanje iona H+ s ionima HPO42– kroz cijeli tubul dovodi do povećanja količine H2PO4–.
U distalnim tubulima omjer može doseći 1:50.
Amoniogeneza
Amoniogeneza se odvija u cijelom bubrežnom tubulu, ali je aktivnija u distalnim dijelovima - distalnim tubulima i sabirnim kanalima korteksa i medule. Glutamin i glutaminska kiselina, ulazeći u tubularne stanice, brzo se deaminiraju pomoću enzima glutaminaze i glutamat dehidrogenaze da nastane amonijak.
Budući da je hidrofoban spoj, amonijak difundira u lumen tubula i prihvaća H+ ione da bi formirao amonijev ion.
Izvor H+ iona u primarnom urinu u proksimalnom tubulu je Na+, H+ antiport. U distalnim dijelovima, za razliku od proksimalnih, dolazi do izlučivanja H+ iona uz sudjelovanje H+-ATPaze, lokalizirane na apikalnoj membrani interkalarnih stanica.

Acidobazna ravnoteža.
Acidobazna ravnoteža je omjer koncentracija vodikovih (H +) i hidroksilnih (OH -) iona u tjelesnim tekućinama.
Konstantnost pH unutarnje okoline tijela posljedica je kombiniranog djelovanja puferskih sustava i niza fizioloških mehanizama.
1. Puferski sustavi krvi i tkiva:
Bikarbonat: NaHCO3 + H2CO3
Fosfat: NaHPO 4c + NaHPO 4k
Protein: protein-Na + + protein-H +
Hemoglobin: HbK+HbH +
2. Fiziološka kontrola:
Respiratorna funkcija pluća
Izlučujuća funkcija bubrega
ASR odražava stanični metabolizam, funkciju transporta plinova u krvi, vanjsko disanje i metabolizam vode i soli.
Normalno, pH krvi se kreće od 7,37 do 7,44, s prosječnom pH vrijednošću od 7,4.
Puferski sustavi održavaju konstantan pH kada se dovode kiseli i bazni (OH -) proizvodi. Puferski učinak objašnjava se vezanjem slobodnih H + i OH - iona komponentama pufera i njihovom pretvorbom u nedisocirani oblik slabe kiseline ili vode.
Puferski sustavi tijela sastoje se od slabih kiselina i njihovih soli s jakim bazama.
Kako bi se uklonio pH pomak, potrebna su različita vremena:
Puferski sustavi – 30 sek
Kontrola disanja – 1 – 3 min
Ekskretorna funkcija bubrega – 10 – 20 sati.
Puferski sustavi ispravljaju samo pH pomake. Fiziološki mehanizmi također obnavljaju puferski kapacitet.
Bikarbonatni puferski sustav.
Bikarbonatni pufer čini oko 10% ukupnog puferskog kapaciteta krvi.
Bikarbonatni pufer sastoji se od ugljične kiseline, koja djeluje kao donor protona, i bikarbonatnog iona, koji djeluje kao akceptor protona.
H 2 CO 3 je slaba kiselina, teško se disocira
H2CO3H++
NaHCO 3 - sol slabe kiseline i jake baze potpuno disocira:
NaNSO3Na++
Mehanizam puferskog djelovanja
1. Kada kiseli produkti uđu u krv, ioni vodika komuniciraju s ionima bikarbonata i nastaje slabo disocirajuća ugljična kiselina:
H + + NaHCO 3 Na + + H 2 CO 3
Omjer H 2 CO 3 / NaHCO 3 se uspostavlja, pH se ne mijenja (koncentracija NaHCO 3 lagano opada).
Pluća osiguravaju uklanjanje ugljičnog dioksida.
2. Kada baze uđu u krv iz tkiva, OH - ioni stupaju u interakciju sa slabom ugljičnom kiselinom (OH - ioni stupaju u interakciju s H + iz pufera, tvoreći H 2 O)
H 2 CO 3 + OH - H 2 O +
pH ostaje isti i raste. Višak pojačava disocijaciju H 2 CO 3, potrošnja H + se nadopunjuje povećanjem disocijacije H 2 CO 3.
Pri normalnom pH krvi, koncentracija bikarbonatnih iona u krvnoj plazmi premašuje koncentraciju ugljičnog dioksida za oko 20 puta:
![]()
Sustav fosfatnog pufera
Komponente međuspremnika:
Na 2 HPO 4c – sol – disupstituirani fosfat
NaH 2 PO 4k – slaba kiselina – monosupstituirani fosfat
Omjer ![]()
Sustav fosfatnog pufera čini 1% puferskog kapaciteta krvi.
Mehanizam djelovanja pufera.
1. Kada kiseli metabolički produkti uđu u krv, H + ioni se vežu na disupstituirani fosfatni ion, formira se kiseli monosupstituirani ion, čiji višak uklanjaju bubrezi u urinu:
Fosfatni pufer djeluje kada se pH mijenja u rasponu od 6,1 do 7,7. U krvi se maksimalni kapacitet fosfatnog pufera pojavljuje na 7,2.
Sustav fosfatnog pufera igra značajnu ulogu u regulaciji ASR unutar stanica, posebno u bubrežnim tubulima. To je zbog veće koncentracije fosfata u stanicama u usporedbi s izvanstaničnom tekućinom (oko 8% ukupnog puferskog kapaciteta). Fosfatni pufer sastoji se od dvije komponente: alkalne - (Na 2 HPO 4) i kisele - (NaH 2 PO 4).
Bubrežni tubularni epitel sadrži puferske komponente u maksimalnoj koncentraciji, što osigurava njegovu veliku snagu. U krvi, fosfatni pufer pomaže u održavanju ("regeneraciji") bikarbonatnog puferskog sustava. S povećanjem razine kiselina u krvnoj plazmi (koja sadrži i bikarbonatne i fosfatne pufere), koncentracija H 2 CO 3 raste, a sadržaj NaHCO 3 opada:
H 2 CO 3 + Na 2 HPO 4 NaHCO 3 + NaH 2 PO 4
Kao rezultat, višak ugljične kiseline se eliminira, a razina NaHCO 3 raste.
Proteinski puferski sustav
Proteinski puferski sustav je glavni unutarstanični pufer. Čini otprilike tri četvrtine puferskog kapaciteta unutarstanične tekućine.
Komponente proteinskog pufera su slabo disocirajući protein sa kisela svojstva(protein-COOH) i soli jake baze (protein-COONa). Kako se razina kiselina povećava, one stupaju u interakciju s proteinskom soli i stvaraju neutralnu sol i slabu kiselinu. Kada se koncentracija baza poveća, dolazi do njihove reakcije s proteinom s kiselim svojstvima. Kao rezultat, umjesto jake baze nastaje slabo bazična sol.
Puferski sustav hemoglobina
Puferski sustav hemoglobina, najkapacitetniji pufer krvi, čini više od polovice njegovog ukupnog puferskog kapaciteta. Hemoglobinski pufer sastoji se od kisele komponente - oksigenirani Hb - HbO 2 i bazične komponente - neoksigenirane. HbO 2 disocira oko 80 puta jače otpuštanjem H + u okoliš od Hb. Sukladno tome, veže više kationa, uglavnom K +.
Glavna uloga puferskog sustava hemoglobina je njegovo sudjelovanje u transportu CO 2 iz tkiva u pluća.
U kapilarama sistemske cirkulacije HbO 2 ispušta kisik. U crvenim krvnim stanicama CO 2 stupa u interakciju s H 2 O i nastaje H 2 CO 3 . Ova kiselina disocira u HCO 3 – i H +, koji se spaja s Hb. HCO 3 – anioni izlaze iz eritrocita u krvnu plazmu, a ekvivalentna količina Cl – aniona ulazi u eritrocite. Ioni Na + preostali u krvnoj plazmi stupaju u interakciju s HCO 3 - i time obnavljaju njezinu alkalnu rezervu.
U kapilarama pluća, u uvjetima niskog pCO 2 i visokog pO 2, Hb dodaje kisik da nastane HbO 2. Karbaminska veza se prekida, oslobađajući CO 2 . U isto vrijeme, HCO 3 – iz krvne plazme ulazi u eritrocite (u zamjenu za Cl – ione) i stupa u interakciju s H +, odcijepljenim od Hb u trenutku njegove oksigenacije. Nastali H 2 CO 3 pod utjecajem karboanhidraze se cijepa na CO 2 i H 2 O. CO 2 difundira u alveole i izlučuje se iz organizma.
Karbonati kostiju
Karbonati kostiju funkcioniraju kao depo za puferske sustave tijela. Kosti sadrže veliki broj soli ugljične kiseline: karbonati kalcija, natrija, kalija itd. S akutnim povećanjem sadržaja kiseline (na primjer, kod akutnog srčanog, respiratornog ili bubrežnog zatajenja, šoka, kome i drugih stanja), kosti mogu osigurati do 30–40% kapaciteta međuspremnika. Oslobađanje kalcijevog karbonata u krvnu plazmu pomaže u učinkovitoj neutralizaciji viška H +. U uvjetima kroničnog opterećenja kiselim spojevima (na primjer, kod kroničnog zatajenja srca, jetre, bubrega, dišnog sustava), kosti mogu osigurati do 50% puferskog kapaciteta tjelesnih bioloških tekućina.
FIZIOLOŠKI MEHANIZMI
Uz moćno i brzo djelovanje kemijski sustavi mehanizmi organa funkcioniraju u tijelu kako bi kompenzirali i eliminirali pomake u CBS-u. Za njihovu provedbu i postizanje željenog učinka potrebno je više vremena - od nekoliko minuta do nekoliko sati. Najučinkovitiji fiziološki mehanizmi za regulaciju CBS-a uključuju procese koji se odvijaju u plućima, bubrezima, jetri i gastrointestinalnom traktu.
Pluća
Pluća eliminiraju ili smanjuju pomake u respiratornom traktu promjenom volumena alveolarne ventilacije. Ovo je prilično pokretljiv mehanizam - unutar 1-2 minute nakon promjene volumena alveolarne ventilacije, pomaci u CBS-u se kompenziraju ili eliminiraju.
Razlog promjene volumena disanja je izravna ili refleksna promjena ekscitabilnosti neurona dišnog centra.
Smanjenje pH u tjelesnim tekućinama(krvna plazma, CSF) je specifični refleksni podražaj za povećanje učestalosti i dubine dišnih pokreta. Kao rezultat toga, pluća oslobađaju višak CO 2 (nastao tijekom disocijacije ugljične kiseline). Zbog toga se smanjuje sadržaj H + (HCO 3 – + H + = H 2 CO 3 ® H 2 O + CO 2) u krvnoj plazmi i drugim tjelesnim tekućinama.
Povećanje pH u tjelesnim tekućinama smanjuje ekscitabilnost inspiracijskih neurona respiratornog centra. To dovodi do smanjenja alveolarne ventilacije i uklanjanja CO 2 iz tijela, tj. do hiperkapnije. U tom smislu, u tekućim medijima tijela, povećava se razina ugljične kiseline, koja se disocira s stvaranjem H +, a pH se smanjuje.
Posljedično, sustav vanjskog disanja može vrlo brzo (u roku od nekoliko minuta) eliminirati ili smanjiti pH pomake i spriječiti razvoj acidoze ili alkaloze: udvostručenje plućne ventilacije povećava pH krvi za oko 0,2; smanjenje ventilacije od 25% može smanjiti pH za 0,3-0,4.
Bubrezi
Glavni mehanizmi za smanjenje ili uklanjanje promjena u brzini metabolizma u krvi koje ostvaruju nefroni bubrega uključuju acidogenezu, amoniogenezu, izlučivanje fosfata i mehanizam izmjene K+, Na+.
Acidogeneza. Ovaj proces ovisan o energiji, koji se odvija u epitelu distalnog nefrona i sabirnih kanalića, izlučuje H + u lumen tubula u zamjenu za reapsorbirani Na + (Sl. 14-1).
LAYOUT Umetni datoteku " PF Slika 14 01 Reapsorpcija HCO3‑ u stanicama proksimalnog dijela »
Riža.14–1 .Reapsorpcija HCO 3‑ u stanicama proksimalnog dijela.
CA - karboanhidraza.
LAYOUT Umetni datoteku " PF Slika 14 02 Reapsorpcija HCO3‑ u stanicama proksimalnog dijela »

Riža.14–2 .Izlučivanje H+ stanicama tubula i sabirnih kanalića.
CA - karboanhidraza.
Količina izlučenog H + je ekvivalentna količini koja ulazi u krv s nehlapljivim kiselinama i H 2 CO 3. Na + reapsorbiran iz lumena tubula u krvnu plazmu uključen je u regeneraciju bikarbonatnog puferskog sustava plazme (Sl. 13–2).
Amoniogeneza, kao i acidogeneza, ostvaruje se epitelom nefronskih tubula i sabirnih kanalića. Amoniogeneza se odvija oksidativnom deaminacijom aminokiselina, pretežno (oko 2/3) glutamina, a manjim dijelom alanina, asparagina, leucina i histidina. Amonijak nastao tijekom ovog procesa difundira u lumen tubula. Tamo se NH 3 + veže za H + ion i formira amonijev ion (NH 4 +). Ioni NH 4 + zamjenjuju Na + u solima i oslobađaju se uglavnom u obliku NH 4 Cl i (NH 4) 2 SO 4. U tom slučaju, ekvivalentna količina natrijevog bikarbonata ulazi u krv, osiguravajući regeneraciju bikarbonatnog puferskog sustava.
Izlučivanje fosfata provodi epitel distalnih tubula uz sudjelovanje fosfatnog puferskog sustava:
Na 2 HPO 4 + H 2 CO 3 NaH 2 PO 4 + NaHCO 3
Nastali natrijev bikarbonat se reapsorbira u krv i održava bikarbonatni pufer, a NaH 2 PO 4 izlučuje se iz tijela mokraćom.
Dakle, izlučivanje H + tubularnim epitelom tijekom provedbe tri gore opisana mehanizma (acidogeneza, amoniogeneza, izlučivanje fosfata) povezano je s stvaranjem bikarbonata i njegovim ulaskom u krvnu plazmu. Time se osigurava stalno održavanje jednog od najvažnijih, obimnijih i mobilnih puferskih sustava - hidrokarbonatnog - i, kao rezultat toga, učinkovito uklanjanje ili smanjenje pomaka u CBS-u koji su opasni za tijelo.
K + ,Na + -mehanizam izmjene, ostvaren u distalnim dijelovima nefrona i početnim dijelovima sabirnih kanala, osigurava izmjenu Na + u primarnom urinu za K +, koji se u njega izlučuje epitelnim stanicama. Reapsorbirani Na+ u tjelesnim tekućinama sudjeluje u regeneraciji bikarbonatnog puferskog sustava. K + ,Na + -izmjenu kontrolira aldosteron. Osim toga, aldosteron regulira (povećava) volumen sekrecije i izlučivanja H +.
Stoga se bubrežni mehanizmi uklanjanja ili smanjenja pomaka u CBS-u provode izlučivanjem H + i obnavljanjem rezerve bikarbonatnog puferskog sustava u tjelesnim tekućinama.
Jetra
Jetra ima značajnu ulogu u kompenzaciji promjena u CBS-u. S jedne strane, u njemu djeluju zajednički unutarstanični i izvanstanični puferski sustavi (hidrokarbonatni, proteinski, itd.), S druge strane, u hepatocitima se odvijaju različite metaboličke reakcije koje su izravno povezane s uklanjanjem poremećaja CBS-a.
Sinteza proteina u krvi, uključen u proteinski puferski sustav. Svi albumini nastaju u jetri, kao i fibrinogen, protrombin, prokonvertin, proakcelerin, heparin, niz globulina i enzima.
Stvaranje amonijaka sposoban neutralizirati kiseline kako u samim hepatocitima tako iu krvnoj plazmi i međustaničnoj tekućini.
Sinteza glukoze od neugljikohidratnih tvari - aminokiseline, glicerol, laktat, piruvat. Uključivanje ovih organskih nehlapljivih kiselina tijekom stvaranja glukoze osigurava smanjenje njihovog sadržaja u stanicama i biološkim tekućinama. Tako se UA, koju mnogi organi i tkiva ne mogu metabolizirati, približno 80% transformira u hepatocitima u H 2 O i CO 2, a preostala količina se resintetizira u glukozu. Tako se laktat pretvara u neutralne proizvode.
Uklanjanje nehlapljivih kiselina iz tijela- glukuronska i sumporna kiselina za detoksikaciju produkata metabolizma i ksenobiotika.
Izlučivanje u crijevo kisele i bazične tvari sa žuči.
Želudac i crijeva
Želudac je uključen u prigušivanje pomaka ASR-a, uglavnom promjenom sekrecije klorovodične kiseline: kada tjelesne tekućine postanu alkalizirane, ovaj proces je inhibiran, a kada su zakiseljene, pojačava se. Crijeva pomažu smanjiti ili eliminirati promjene u hormonima bogatim kiselinom na:
lučenje crijevnog soka, koji sadrži velike količine bikarbonata. U isto vrijeme, H + ulazi u krvnu plazmu.
Promjene u količini apsorbirane tekućine. To pomaže normalizirati ravnotežu vode i elektrolita u stanicama, izvanstaničnim i drugim biološkim tekućinama i, kao rezultat, normalizirati pH.
Reapsorpcija komponenti puferskih sustava(Na +, K +, Ca 2+, Cl –, HCO 3 –).
Povezane informacije.