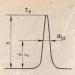
Oksidacija glukoze u CO 2 i H 2 O (aerobno raspadanje). Aerobna razgradnja glukoze može se izraziti ukupnom jednadžbom:
C 6 H 12 O 6 + 6 O 2 > 6 CO 2 + H 2 O + 2820 kJ / mol.
Ovaj proces uključuje nekoliko faza (Slika 7-33).
Aerobna glikoliza - proces oksidacije glukoze s stvaranjem dviju molekula piruvata;
Opći put katabolizma, uključujući pretvorbu piruvata u acetil-CoA i njegovu daljnju oksidaciju u citratnom ciklusu;
CPE za kisik, zajedno s reakcijama dehidrogenacije koje se javljaju u procesu razgradnje glukoze.
U određenim situacijama, opskrba tkiva kisikom možda neće zadovoljiti njihove potrebe. Na primjer, u početnim fazama intenzivnog rada mišića pod stresom, otkucaji srca možda neće doseći željenu frekvenciju, a potreba mišića za kisikom za aerobnu razgradnju glukoze je velika. U takvim slučajevima se aktivira proces koji teče bez kisika i završava stvaranjem laktata iz pirogrožđane kiseline. Taj se proces naziva anaerobna razgradnja ili anaerobna glikoliza. Anaerobna razgradnja glukoze energetski je neučinkovita, ali upravo taj proces može postati jedini izvor energije za mišićnu stanicu u opisanoj situaciji. U budućnosti, kada je opskrba mišića kisikom dovoljna kao rezultat prijelaza srca na ubrzani ritam, anaerobno raspadanje prelazi u aerobno. Putevi katabolizma glukoze i njihov energetski učinak prikazani su na sl. 7-34 (prikaz, stručni).
B. Aerobna glikoliza
Aerobna glikoliza je proces oksidacije glukoze u pirogrožđanu kiselinu u prisutnosti kisika. Svi enzimi koji kataliziraju reakcije ovog procesa lokalizirani su u citosolu stanice.
1. Faze aerobne glikolize
U aerobnoj glikolizi mogu se razlikovati 2 stupnja.
Pripremna faza tijekom koje se glukoza fosforilira i dijeli na dvije molekule fosfotrioze. Ova serija reakcija odvija se pomoću 2 ATP molekule.
Faza povezana sa sintezom ATP-a. Kao rezultat ove serije reakcija, fosfotrioze se pretvaraju u piruvat. Energija koja se oslobađa u ovoj fazi koristi se za sintezu 10 molova ATP-a.
2. Reakcije aerobne glikolize
Pretvorba glukoza-6-fosfata u 2 molekule gliceraldehid-3-fosfata
Glukoza-6-fosfat, nastao kao rezultat fosforilacije glukoze potpomognute ATP-om, tijekom sljedeće reakcije pretvara se u fruktozo-6-fosfat. Ova reverzibilna reakcija izomerizacije odvija se pod djelovanjem enzima glukoza fosfat izomeraze.
Nakon toga slijedi još jedna reakcija fosforilacije koja koristi fosfatni ostatak i energiju ATP-a. Tijekom ove reakcije, katalizirane fosfofruktokinazom, fruktoza-6-fosfat se pretvara u fruktoza-1,6-bisfosfat. Ova je reakcija, kao i heksokinaza, praktički nepovratna i, štoviše, najsporija je od svih reakcija glikolize. Reakcija koju katalizira fosfofruktokinaza određuje brzinu svih glikoliza, stoga je regulacijom aktivnosti fosfofruktokinaze moguće promijeniti brzinu katabolizma glukoze.

Fruktoza-1,6-bisfosfat se dalje cijepa na 2 trioza fosfata: gliceraldehid-3-fosfat i dihidroksiaceton fosfat. Reakciju katalizira enzim fruktoza bisfosfat aldolaza, ili jednostavno aldolaza. Ovaj enzim katalizira i reakcije aldola cijepanja i kondenzacije aldola, t.j. reverzibilna reakcija. Produkti reakcije cijepanja aldola su izomeri. U kasnijim reakcijama glikolize koristi se samo gliceraldehid-3-fosfat, pa se dihidroksiaceton fosfat uz sudjelovanje enzima trioza fosfat izomeraze pretvara u gliceraldehid-3-fosfat (slika 7-35).
U opisanom nizu reakcija, fosforilacija se događa dva puta pomoću ATP-a. Međutim, potrošnja dvije molekule ATP-a (po molekuli glukoze) tada će biti nadoknađena sintezom više ATP-a.
Pretvorba gliceraldehid-3-fosfata u piruvat
Ovaj dio aerobne glikolize uključuje reakcije povezane sa sintezom ATP-a. Najsloženija reakcija u ovoj seriji reakcija je pretvorba gliceraldehid-3-fosfata u 1,3-bisfosfoglicerat. Ova transformacija je prva oksidacijska reakcija tijekom glikolize. Reakcija je katalizirana gliceraldehid-3-fosfat dehidrogenaza, koji je enzim ovisan o NAD. Značaj ove reakcije nije samo u tome što nastaje reduciran koenzim čija je oksidacija u respiratornom lancu povezana sa sintezom ATP-a, već i u činjenici da je slobodna energija oksidacije koncentrirana u makroergijskom veza produkta reakcije. Gliceraldehid-3-fosfat dehidrogenaza sadrži cisteinski ostatak u aktivnom centru, čija sulfhidrilna skupina izravno je uključena u katalizu. Oksidacija gliceraldehid-3-fosfata dovodi do redukcije NAD i stvaranja visokoenergetske anhidridne veze u 1,3-bisfosfogliceratu na poziciji 1 uz sudjelovanje H3PO4. U sljedećoj reakciji, visokoenergetski fosfat se prenosi na ADP sa stvaranje ATP-a. Enzim koji katalizira ovu transformaciju nazvan je prema fosfoglicerat kinazi reverzne reakcije (kinaze su nazvane prema supstratu koji je na istoj strani reakcijske jednadžbe s ATP-om). Ova serija reakcija prikazana je na sl. 7-36 (prikaz, stručni).

Nastanak ATP-a na ovaj način nije povezan s respiratornim lancem, a naziva se fosforilacija supstrata ADP-a. Formirani 3-fosfoglicerat više ne sadrži makroergijsku vezu. U sljedećim reakcijama dolazi do intramolekularnih preuređivanja, čije se značenje svodi na to da niskoenergetski fosfoester prelazi u spoj koji sadrži visokoenergetski fosfat. Intramolekularne transformacije sastoje se u prijenosu fosfatnog ostatka s položaja 3 u fosfogliceratu na položaj 2. Zatim se molekula vode odcijepi od nastalog 2-fosfoglicerata uz sudjelovanje enzima enolaze. Naziv enzima za dehidraciju dolazi od obrnute reakcije. Kao rezultat reakcije nastaje supstituirani enol - fosfoenolpiruvat. Nastali fosfoenolpiruvat je makroergijski spoj čija se fosfatna skupina u sljedećoj reakciji prenosi na ADP uz sudjelovanje piruvat kinaze (enzim je također nazvan po obrnutoj reakciji u kojoj se fosforilira piruvat, iako takva reakcija ne uzima mjesto u ovom obliku).
Pretvorba fosfoenolpiruvata u piruvat je ireverzibilna reakcija. Ovo je druga reakcija fosforilacije supstrata tijekom glikolize. Rezultirajući enolni oblik piruvata zatim se neenzimski transformira u termodinamički stabilniji keto oblik. Opisani niz reakcija prikazan je na sl. 7-37 (prikaz, stručni).
Riža. 7-37 (prikaz, stručni). Pretvorba 3-fosfoglicerata u piruvat.
Shema 10 reakcija do kojih dolazi tijekom aerobne glikolize i daljnje oksidacije piruvata prikazana je na sl. 7-33 (prikaz, stručni).
Oksidacija citoplazmatskog NADH u mitohondrijskom respiratornom lancu. Shuttle sustavi
NADH, nastao tijekom oksidacije gliceraldehid-3-fosfata u aerobnoj glikolizi, oksidira se prijenosom atoma vodika u mitohondrijski respiratorni lanac. Međutim, citosolni NADH nije u stanju prenijeti vodik u respiratorni lanac jer je mitohondrijska membrana nepropusna za njega. Prijenos vodika kroz membranu događa se uz pomoć posebnih sustava zvanih "shuttle". U tim sustavima vodik se transportira kroz membranu uz sudjelovanje parova supstrata vezanih odgovarajućim dehidrogenazama, t.j. s obje strane mitohondrijske membrane je specifična dehidrogenaza. Poznata su 2 shuttle sustava. U prvom od ovih sustava, vodik se prenosi iz NADH u citosolu na dihidroksiaceton fosfat pomoću enzima glicerol-3-fosfat dehidrogenaze (enzim ovisan o NAD, nazvan po obrnutoj reakciji). Glicerol-3-fosfat koji nastaje tijekom ove reakcije dalje oksidira enzim unutarnje mitohondrijske membrane – glicerol-3-fosfat dehidrogenaza (FAD-ovisni enzim). Zatim protoni i elektroni iz FADH 2 prelaze do ubikinona i dalje duž CPE (slika 7-38).
Glicerol fosfatni shuttle sustav radi u bijelim mišićnim stanicama i hepatocitima. Međutim, mitohondrijska glicerol-3-fosfat dehidrogenaza je odsutna u stanicama srčanog mišića. Drugi shuttle sustav, koji uključuje malatnu, citosolnu i mitohondrijsku malatnu dehidrogenazu, univerzalniji je. U citoplazmi NADH reducira oksaloacetat u malat (slika 7-39, reakcija 1), koji uz sudjelovanje nosača prelazi u mitohondrije, gdje se oksidira u oksaloacetat pomoću NAD-ovisne malat dehidrogenaze (reakcija 2) . NAD smanjen tijekom ove reakcije donira vodik mitohondrijskom CPE. Međutim, oksaloacetat nastao iz malata ne može sam izaći iz mitohondrija u citosol, budući da je mitohondrijska membrana za njega nepropusna. Stoga se oksaloacetat pretvara u aspartat, koji se transportira u citosol, gdje se ponovno pretvara u oksaloacetat. Pretvorba oksaloacetata u aspartat i obrnuto povezana je s dodatkom i eliminacijom amino skupine (reakcije transaminacije, vidi dio 9). Ovaj shuttle sustav naziva se malat-aspartat sustav (slika 7-39). Rezultat njezina rada je regeneracija citoplazmatskog NAD + iz NADH.
Oba shuttle sustava značajno se razlikuju u količini sintetiziranog ATP-a. U prvom sustavu omjer P/O je 2, budući da se vodik uvodi u CPE na razini KoQ. Drugi sustav je energetski učinkovitiji jer prenosi vodik do CPE preko mitohondrijske NAD+, a omjer P/O je blizu 3.
4. ATP ravnoteža tijekom aerobne glikolize i razgradnje glukoze na CO2 i H2O
Oslobađanje ATP-a tijekom aerobne glikolize
Za stvaranje fruktozo-1,6-bisfosfata iz jedne molekule glukoze potrebne su 2 molekule ATP (reakcije 1 i 3 na slici 7-33). Reakcije povezane sa sintezom ATP-a nastaju nakon razgradnje glukoze na 2 molekule fosfotrioze, t.j. u drugom koraku glikolize. U ovoj fazi se događaju 2 reakcije fosforilacije supstrata i sintetiziraju se 2 molekule ATP (reakcije 7 i 10). Osim toga, jedna molekula gliceraldehid-3-fosfata je dehidrogenirana (reakcija 6), a NADH prenosi vodik u mitohondrijski CPE, gdje se oksidativnom fosforilacijom sintetiziraju 3 molekule ATP-a. U ovom slučaju, količina ATP-a (3 ili 2) ovisi o vrsti shuttle sustava. Stoga je oksidacija jedne molekule gliceraldehid-3-fosfata u piruvat povezana sa sintezom 5 ATP molekula. S obzirom da se iz glukoze formiraju 2 molekule fosfotrioze, dobivenu vrijednost treba pomnožiti s 2, a zatim oduzeti 2 molekule ATP-a potrošene u prvoj fazi. Dakle, prinos ATP-a tijekom aerobne glikolize je (5×2) - 2 = 8 ATP.
Izlaz ATP-a tijekom aerobne razgradnje glukoze do krajnjih proizvoda
Kao rezultat glikolize nastaje piruvat, koji se dalje oksidira u CO 2 i H 2 O u OPC opisanom u odjeljku 6. Sada je moguće procijeniti energetsku učinkovitost glikolize i OPC, koji zajedno čine proces aerobnog razgradnja glukoze do krajnjih proizvoda (tablice 7-4) .
Dakle, prinos ATP-a tijekom oksidacije 1 mola glukoze u CO 2 i H 2 O iznosi 38 mola ATP-a.

U procesu aerobne razgradnje glukoze dolazi do 6 reakcija dehidrogenacije. Jedan od njih se javlja u glikolizi, a 5 u OPC (vidi odjeljak 6). Supstrati za specifične NAD-ovisne dehidrogenaze: gliceraldehid-3-fosfat, zhiruvat, izocitrat, β-ketoglutarat, malat. Jedna reakcija dehidrogenacije u citratnom ciklusu pod djelovanjem sukcinat dehidrogenaze odvija se uz sudjelovanje koenzima FAD. Ukupna količina ATP-a sintetiziranog oksidativnom fosforilacijom iznosi 17 mola ATP-a po 1 molu gliceraldehid fosfata. Tome se mora dodati 3 mola ATP-a sintetiziranog fosforilacijom supstrata (dvije reakcije u glikolizi i jedna u citratnom ciklusu).

Riža. 7-38 (prikaz, stručni). Glicerofosfatni shuttle sustav. 1 - gliceraldehid-3-fosfat dehidrogenaza; 2 - glicerol-3-fosfat dehidrogenaza (citosolni enzim, nazvan po obrnutoj reakciji); 3 - glicerol-3-fosfat dehidrogenaza (mitohondrijski flavin enzim).
Tablica 7-4. Faze aerobne razgradnje glukoze
S obzirom da se glukoza razlaže na 2 fosfotrioze i da je stehiometrijski koeficijent daljnjih transformacija 2, dobivenu vrijednost treba pomnožiti s 2, a od rezultata treba oduzeti 2 mola ATP-a upotrijebljenog u prvoj fazi glikolize.
U prvoj fazi, glukoza se dijeli na 2 trioze:

Tako se u prvoj fazi glikolize 2 molekule ATP-a troše na aktivaciju glukoze i nastaju 2 molekule 3-fosfogliceraldehida.
U drugom stupnju 2 molekule 3-fosfogliceraldehida se oksidiraju u dvije molekule mliječne kiseline.


Značaj reakcije laktat dehidrogenaze (LDH) je oksidacija NADH 2 u NAD u uvjetima bez kisika i omogućavanje dehidrogenazne reakcije 3-fosfogliceraldehida.

Ukupna jednadžba za glikolizu je:
glukoza + 2ADP + 2H 3 PO 4 → 2 laktat + 2ATP + 2H 2 O
Glikoliza se odvija u citosolu. Njegovu regulaciju provode ključni enzimi - fosfofruktokinaza, piruvat kinaza. Ove enzime aktiviraju ADP i NAD, a inhibiraju ATP i NADH 2 .
Energetska učinkovitost anaerobne glikolize svodi se na razliku između broja potrošenih i formiranih ATP molekula. U reakciji heksokinaze i fosfofruktokinazne reakcije troše se 2 molekule ATP-a po molekuli glukoze. U reakciji glicerokinaze i reakcije piruvat kinaze nastaju 2 ATP molekule po molekuli trioze (1/2 glukoze). Za molekulu glukoze (2 trioze) nastaju 4 molekule ATP-a. Ukupni bilans: 4 ATP - 2 ATP = 2 ATP. 2 ATP molekule nakupljaju u sebi ≈ 20 kcal, što je oko 3% energije potpune oksidacije glukoze (686 kcal).
Unatoč relativno niskoj energetskoj učinkovitosti anaerobne glikolize, ona ima važnu biološki značaj, što je to jedini način generiranja energije u uvjetima bez kisika. U uvjetima nedostatka kisika osigurava izvođenje intenzivnog rada mišića u početnom razdoblju tjelesne aktivnosti.
U fetalnim tkivima anaerobna glikoliza je vrlo aktivna u uvjetima nedostatka kisika. Ostaje aktivan tijekom novorođenčadi, postupno prelazi u aerobnu oksidaciju.
Daljnja konverzija mliječne kiseline
- Uz intenzivnu opskrbu kisikom u aerobnim uvjetima, mliječna kiselina se pretvara u PVC i preko acetil CoA uključuje se u Krebsov ciklus, osiguravajući energiju.
- Mliječna kiselina se transportira iz mišića u jetru, gdje se koristi za sintezu glukoze – ciklus R. Corey.
Corey ciklus

- Pri visokim koncentracijama mliječne kiseline u tkivima, kako bi se spriječilo zakiseljavanje (acidoza), može se izlučiti putem bubrega i žlijezda znojnica.
Aerobna oksidacija glukoze
Aerobna oksidacija glukoze uključuje 3 faze:
Faza 1 javlja se u citosolu, a to je stvaranje pirogrožđane kiseline:
Glukoza → 2 PVC + 2 ATP + 2 NADH 2;
Druga faza odvija se u mitohondrijima:
2 PVC → 2 acetil - CoA + 2 NADH 2;
Faza 3 odvija se unutar mitohondrija:
2 acetil - CoA → 2 TCA.
Zbog činjenice da se u citosolu u prvoj fazi formiraju 2 molekule NADH 2, koje se mogu oksidirati samo u mitohondrijskom respiratornom lancu, neophodan je prijenos vodika iz NADH 2 citosola u intramitohondrijske lance za prijenos elektrona. Mitohondriji su nepropusni za NADH 2, pa postoje posebni shuttle mehanizmi za prijenos vodika iz citosola u mitohondrije. Njihova bit se ogleda u dijagramu, gdje je X oksidirani oblik nosača vodika, a XH 2 njegov reducirani oblik:

Ovisno o tome koje tvari sudjeluju u prijenosu vodika kroz mitohondrijsku membranu, razlikuje se nekoliko mehanizama shuttle.
Glicerofosfatni shuttle mehanizam, u kojem dolazi do gubitka dvije ATP molekule, tk. umjesto dvije molekule NADH 2 (potencijalno 6 ATP molekula) nastaju 2 FADH 2 molekule (zapravo 4 ATP molekule).
Mali shuttle mehanizam djeluje na uklanjanju vodika iz mitohondrijske matrice:
![]()
Energetska učinkovitost aerobne oksidacije.
- glukoza → 2 PVC + 2 ATP + 2 NADH 2 (→ 8 ATP).
- 2 PVC → 2 acetil CoA + 2 NADH 2 (→ 6 ATP).
- 2 acetil CoA → 2 TCA (12*2 = 24 ATP).
Ukupno je moguće formiranje 38 molekula ATP-a od kojih je potrebno oduzeti 2 molekule ATP-a izgubljene u mehanizmu glicerofosfatnog shuttlea. Tako se formira 36 ATP.
36 ATP (oko 360 kcal) je od 686 kcal. 50-60% je energetska učinkovitost aerobne oksidacije glukoze, koja je dvadeset puta veća od učinkovitosti anaerobne oksidacije glukoze. Stoga se u tkivima, kada kisik uđe, blokira se anaerobni put, a ta se pojava naziva Pasteurov efekt. Kod novorođenčadi aerobni put počinje se aktivirati u prva 2-3 mjeseca života.
6.5. 2. Biosinteza glukoze (glukoneogeneza)
Glukoneogeneza je put za sintezu glukoze u tijelu iz neugljikohidratnih tvari, koja je u stanju održavati razinu glukoze dugo vremena u nedostatku ugljikohidrata u prehrani. Početne tvari za njega su mliječna kiselina, PVC, aminokiseline, glicerin. Glukoneogeneza je najaktivnija u jetri i bubrezima. Taj je proces intracelularno lokaliziran dijelom u citosolu, dijelom u mitohondrijima. Općenito, glukoneogeneza je proces obrnut od glikolize.

Glikoliza ima tri nepovratna koraka katalizirana enzimima:
piruvat kinaza;
fosfofruktokinaza;
heksokinaza.
Stoga, u glukoneogeneza umjesto ovih enzima, postoje specifični enzimi koji "zaobilaze" ove nepovratne korake:
- piruvat karboksilaza i karboksikinaza ("bypass" piruvat kinaza);
- fruktoza-6-fosfataza ("zaobilazi" fosfofruktokinazu);
- glukoza-6-fosfataza ("zaobilazi" heksokinazu).

Glukoza-6-fosfat se pretvara u glukozu djelovanjem glukoza-6-fosfataze, koja se oslobađa iz hepatocita u krv.
Ključni enzimi za glukoneogenezu su piruvat karboksilaze i fruktoza-1,6-difosfataza. ATP im je aktivator (za sintezu jedne molekule glukoze potrebno je 6 molekula ATP-a).
Dakle, visoka koncentracija ATP-a u stanicama aktivira glukoneogenezu koja zahtijeva energiju, a ujedno inhibira glikolizu (u fazi fosfofruktokinaze), što dovodi do stvaranja ATP-a. Ovaj položaj ilustrira donji grafikon.

vitamin H
Vitamin H (biotin, antiseboreični vitamin) je uključen u glukoneogenezu, koji kemijske prirode je heterocikl koji sadrži sumpor s ostacima valerinske kiseline. Široko je rasprostranjen u životinjskim i biljnim proizvodima (jetra, žumanjak). Dnevna potreba za njim je 0,2 mg. Avitaminoza se očituje dermatitisom, oštećenjem noktiju, povećanjem ili smanjenjem stvaranja sebuma (seboreja). Biološka uloga vitamin H:
- sudjeluje u reakcijama karboksilacije;
- sudjeluje u reakcijama transkarboksilacije;
- sudjeluje u izmjeni purinskih baza, nekih aminokiselina.
Glukoneogeneza je aktivna posljednjih mjeseci intrauterini razvoj. Nakon rođenja djeteta, aktivnost procesa se povećava, počevši od trećeg mjeseca života.
Razgradnja ugljikohidrata u aerobnim uvjetima može se odvijati na izravan (apotomski ili pentozni) način i neizravan (dihotomni) način.
Dihotomna (grč. dicha - na dva dijela, tome-presjek) oksidacija ugljikohidrata odvija se prema jednadžbi:
C6H12O6 + 6O2 \u003d 6 CO2 + b H2O + 686 kcal
Ovaj put je glavni u stvaranju energije. Prve faze ovog puta podudaraju se s anaerobnom oksidacijom glukoze. Divergencija putova počinje u fazi stvaranja pirogrožđane kiseline, koja se u životinjskim tkivima dekarboksilira oksidativnim putem. Glikoliza je slijed enzimskih reakcija koje dovode do pretvorbe glukoze u piruvat uz istovremeno stvaranje ATP-a. U aerobnim uvjetima piruvat prodire u mitohondrije, gdje se potpuno oksidira do CO2 i H2O. Ako je sadržaj kisika nedovoljan, kao što može biti slučaj u mišićima koji se aktivno kontrahiraju, piruvat se pretvara u laktat. Anaerobna glikoliza je složen enzimski proces razgradnje glukoze koji se događa u ljudskim i životinjskim tkivima bez potrošnje kisika. Krajnji produkt glikolize je mliječna kiselina. Tijekom glikolize nastaje ATP. Ukupna jednadžba za glikolizu može se predstaviti na sljedeći način:
U anaerobnim uvjetima, glikoliza je jedini proces u životinjskom tijelu koji opskrbljuje energiju. Zahvaljujući glikolizi, ljudski i životinjski organizam može obavljati niz fizioloških funkcija tijekom određenog razdoblja u uvjetima nedostatka kisika. Kada se glikoliza dogodi u prisutnosti kisika, govorimo o aerobnoj glikolizi. Prva enzimska reakcija glikolize je fosforilacija, t.j. prijenos ortofosfatnog ostatka na glukozu na račun ATP-a. Reakciju katalizira enzim heksokinaza:
Druga reakcija glikolize je pretvorba glukoza-6-fosfata enzima glukoza-6-fosfat izomeraze u fruktozo-6-fosfat:
Treću reakciju katalizira enzim fosfofruktokinaza; rezultirajući fruktozo-6-fosfat ponovno fosforilira druga ATP molekula:
Četvrtu reakciju glikolize katalizira enzim aldolaza. Pod utjecajem ovog enzima fruktoza-1,6-bisfosfat se cijepa na dvije fosfotrioze:
Peta reakcija je reakcija izomerizacije trioza fosfata. Katalizuje enzim trioza fosfat izomeraza:
Formiranje gliceraldehid-3-fosfata, takoreći, dovršava prvu fazu glikolize. Druga faza je najteža i najvažnija. Uključuje redoks reakciju (reakciju glikolitičke oksidoredukcije) povezanu s fosforilacijom supstrata, tijekom koje nastaje ATP. Kao rezultat šeste reakcije, gliceraldehid-3-fosfat u prisutnosti enzima gliceraldehidrofosfat dehidrogenaze, koenzima NAD i anorganskog fosfata prolazi kroz svojevrsnu oksidaciju s stvaranjem 1,3-bisfosfoglicerinske kiseline i reduciranog oblika NAD ( NADH). Ova reakcija je blokirana jodom ili bromoacetatom, te se odvija u nekoliko faza:
Sedmu reakciju katalizira fosfoglicerat kinaza, s prijenosom energetski bogatog fosfatnog ostatka (fosfatna skupina na poziciji 1) na ADP uz stvaranje ATP-a i 3-fosfoglicerinske kiseline (3-fosfoglicerat):
Osma reakcija je popraćena intramolekularnim prijenosom preostale fosfatne skupine, a 3-fosfoglicerinska kiselina se pretvara u 2-fosfoglicerinsku kiselinu (2-fosfoglicerat).
Devetu reakciju katalizira enzim enolaza, dok 2-fosfoglicerinska kiselina, kao rezultat eliminacije molekule vode, prelazi u fosfoenolpirogrožđanu kiselinu (fosfoenolpiruvat), a fosfatna veza u položaju 2 postaje visokoergična:
Desetu reakciju karakterizira pucanje visokoenergetske veze i prijenos fosfatnog ostatka s fosfoenolpiruvata u ADP (fosforilacija supstrata). Katalizira enzim piruvat kinaza:
Kao rezultat jedanaeste reakcije dolazi do redukcije pirogrožđane kiseline i stvaranja mliječne kiseline. Reakcija se odvija uz sudjelovanje enzima laktat dehidrogenaze i koenzima NADH, nastalih u šestoj reakciji:
Biološki značaj procesa glikolize prvenstveno je u stvaranju energetski bogatih spojeva fosfora. U prvim fazama glikolize troše se 2 molekule ATP (reakcije heksokinaze i fosfofruktokinaze). Na sljedećim nastaju 4 ATP molekule (reakcije fosfoglicerat kinaze i piruvat kinaze). Dakle, energetska učinkovitost glikolize u anaerobnim uvjetima iznosi 2 ATP molekule po molekuli glukoze.
-
Aerobna oksidacija ugljikohidrati. Propadanje ugljikohidrati u aerobni uvjeti mogu ići izravnim (apotomskim ili pentoznim) putem i neizravnim (dihotomnim) putem. -
Aerobna oksidacija ugljikohidrati. Propadanje ugljikohidrati u aerobni uvjeti mogu ići izravnim (apotomijski ili pentozni) način i. -
Glikoliza je najjednostavniji oblik biol. mehanizam za pohranu energije ugljikohidrati u ATP-u.
S energetski povoljnijim aerobni oksidacija od jedne molekule glukoze... -
Oksidativno fosforilacija bi se pravilnije nazvala fosforilacijom u respiratornom lancu.
Aerobna oksidacija ugljikohidrati. -
- PHA može s tvorbom ući u reakcije glukoneogeneze ugljikohidrati- Glukoza ili glikogen.
Aktivacija FA događa se u citoplazmi, a b- oksidacija- u mitohondrijima. -
U procesu disanja ugljikohidrati, masti i proteini prolaze kroz više faza oksidacija, što dovodi do obnove glavnih dobavljača VE za respiratorne flavine... -
Glikoneogeneza – obrazovanje ugljikohidrati(glukoza ili glikogen) iz tvari neugljikohidratnog podrijetla.
Oksidativno faza: 2 reakcije oksidacija heksoza fosfat bez kisika. -
Glavni ugljikohidrata mlijeko – laktoza – prisutna u mlijeku svih vrsta sisavaca.
Oksidacija piruvat u acetil-CoA nastaje uz sudjelovanje brojnih enzima i koenzima ... -
Prilikom izgaranja 1 g ugljikohidrati Nastaje 4 kcal. To je manje od masti (9 kcal).
G. Ugljikohidrati kao izvor energije imaju sposobnost oksidirati u tijelu kao aerobni, pa... -
U srži suvremene ideje o razgradnji masnih kiselina u tkivima leži teorija - oksidacija
Put raspada GBF-a ugljikohidrati daje energiju za sintezu.
Pronađene slične stranice:10
Aerobna oksidacija ugljikohidrata glavni je način stvaranja energije za tijelo. Neizravno - dihotomno i izravno - apotomsko.
Izravni put za razgradnju glukoze je pentozni ciklus- dovodi do stvaranja pentoza i nakupljanja NADPH 2 . Pentozni ciklus karakterizira uzastopna eliminacija svakog od njegovih 6 ugljikovih atoma iz molekula glukoze uz stvaranje 1 molekule ugljičnog dioksida i vode tijekom jednog ciklusa. Razgradnja cijele molekule glukoze događa se unutar 6 ciklusa koji se ponavljaju.
Važnost pentozofosfatnog ciklusa oksidacije ugljikohidrata u metabolizmu je velika:
1. Opskrbljuje smanjeni NADP, neophodan za biosintezu masnih kiselina, kolesterola itd. Zbog pentoznog ciklusa, tjelesna potreba za NADPH 2 pokrivena je za 50%.
2. Opskrba pentoza fosfata za sintezu nukleinske kiseline i mnogi koenzimi.
Reakcije pentoznog ciklusa odvijaju se u citoplazmi stanice.
U nizu patoloških stanja povećava se udio pentoznog puta oksidacije glukoze.
neizravan način- razgradnju glukoze do ugljičnog dioksida i vode uz stvaranje 36 molekula ATP-a.
1. Razgradnja glukoze ili glikogena u pirogrožđanu kiselinu
2. Pretvorba pirogrožđane kiseline u acetil-CoA
Oksidacija acetil-CoA u Krebsovom ciklusu u ugljični dioksid i vodu
C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O + 686 kcal
U slučaju aerobne pretvorbe, pirogrožđana kiselina podliježe oksidativnoj dekarboksilaciji da nastane acetil-CoA, koji se zatim oksidira u ugljični dioksid i vodu.
Oksidaciju piruvata u acetil-CoA katalizira sustav piruvat dehidrogenaze i odvija se u nekoliko faza. Ukupna reakcija:
Piruvat + NADH + HS-CoA acetil-CoA + NADH 2 + CO 2 reakcija je gotovo nepovratna
Potpuna oksidacija acetil-CoA događa se u ciklusu trikarboksilne kiseline ili Krebsovom ciklusu. Taj se proces odvija u mitohondrijima.
Ciklus se sastoji od 8 uzastopnih reakcija:
U ovom ciklusu, molekula koja sadrži 2 atoma ugljika (octena kiselina u obliku acetil-CoA) reagira s molekulom oksalooctene kiseline, što rezultira spojem sa 6 atoma ugljika – limunskom kiselinom. U procesu dehidrogenacije, dekarboksilacije i pripremne reakcije, limunska kiselina se ponovno pretvara u oksalooctenu kiselinu, koja se lako spaja s drugom molekulom acetil-CoA.
1) acetil-CoA + oksaloacetat (PIEC) limunska kiselina
citrat sintaza
2) limunska kiselina izocitna kiselina
akonitat hidrataze
3) izocitritna kiselina + PREKO-ketoglutarna kiselina + NADH 2 + CO 2
izocitrat dehidrogenaza
4) -ketoglutarna kiselina + HS-CoA + NADsukcinil SCoA + NADH 2 + CO 2
5) sukcinil-CoA + GDP + jantarna kiselina + GTP + HS-CoA
sukcinil CoA sintetaza
6) jantarna kiselina + FADfumarna kiselina + FADH 2
sukcinat dehidrogenaza
7) fumarna kiselina + H 2 O L jabučna kiselina
fumarat hidrataze
8) malat + NADoksaloacetat + NADH 2
malat dehidrogenaza
Ukupno, kada se molekula glukoze razgradi u tkivima, sintetizira se 36 ATP molekula. Bez sumnje, ovo je energetski učinkovitiji proces od glikolize.
Krebsov ciklus je uobičajeni konačni put kojim se dovršava metabolizam ugljikohidrata, masnih kiselina i aminokiselina. Sve te tvari uključene su u Krebsov ciklus u jednoj ili drugoj fazi. Tada dolazi do biološke oksidacije ili disanja tkiva, glavna značajka a to je da se odvija postupno, kroz brojne enzimske faze. Taj se proces događa u mitohondrijima, staničnim organelama koje sadrže veliki broj enzima. Proces uključuje dehidrogenaze ovisne o piridinu, dehidrogenaze ovisne o flavinu, citokrome, koenzim Q - ubikinon, proteine koji sadrže ne-hem željezo.
Intenzitet disanja kontrolira se omjerom ATP/ADP. Što je taj omjer manji, to je disanje intenzivnije, osiguravajući proizvodnju ATP-a.
Također, ciklus limunske kiseline je glavni izvor ugljičnog dioksida u stanici za reakcije karboksilacije, koje započinju sintezu masnih kiselina i glukoneogenezu. Isti ugljični dioksid opskrbljuje ugljikom ureu i neke jedinice purinskih i pirimidinskih prstenova.
Odnos između procesa metabolizma ugljikohidrata i dušika također se ostvaruje kroz međuprodukte ciklusa limunske kiseline.
Postoji nekoliko puteva kojima se intermedijari ciklusa limunske kiseline ugrađuju u proces lipogeneze. Cijepanjem citrata dolazi do stvaranja acetil-CoA, koji igra ulogu prekursora u biosintezi masnih kiselina.
Izocitrat i malat osiguravaju stvaranje NADP-a, koji se troši u kasnijim koracima oporavka sinteze masti.
Uloga ključni faktor, koji određuje pretvorbu NADH igra stanje adenin nukleotida. Visok sadržaj ADP i nizak ATP ukazuje na nisku rezervu energije. Istovremeno, NADH sudjeluje u reakcijama dišnog lanca, pospješujući procese oksidativne fosforilacije povezane sa pohranom energije. Obrnuti fenomen se opaža kod niskog sadržaja ADP-a i visokog ATP-a. Ograničavajući sustav prijenosa elektrona, oni potiču korištenje NADH u drugim redukcijskim reakcijama kao što su sinteza glutamata i glukoneogeneza.
Dah. Aerobna oksidacija ugljikohidrata događa se u prisutnosti atmosferskog kisika, zbog čega se često naziva disanjem.
Za razliku od glikolize (glikogenolize), gdje provinska kiselina služi kao konačni akceptor atoma vodika i elektrona, kisik igra ulogu takvog akceptora tijekom disanja. U prvom slučaju nastaje mliječna kiselina kao konačni proizvod, u kojem ukupno oksidacijsko stanje ugljika ostaje isto kao i glukoza, u drugom slučaju nastaje ugljični dioksid – puno jednostavniji spoj u kojem je jedini ugljikov atom potpuno je oksidiran. U isto vrijeme, disanje i glikoliza imaju mnogo zajedničkih karika.
Disanje je, kao i glikoliza, praćeno stvaranjem fosfatnih estera glukoze i fruktoze, fosfotrioza-dioksiaceton fosfata i gliceraldehid-3-fosfata, kao i međuprodukta kao što je 1,3-difosfosfosfosfosfosfosfosfat, 3-difosfosfosfosfat. i pirogrožđane kiseline. Mnoge reakcije glikolize i disanja kataliziraju isti enzimi. Drugim riječima, tijekom disanja, pretvaranje glukoze u mliječnu kiselinu prolazi kroz sve iste korake kao u glikolizi. Međutim, u ovom slučaju, atomi vodika odcijepljeni od gliceraldehid-3-fosfata ne reduciraju pirogrožđanu kiselinu, već se prenose na kisik, prolazeći kroz složeni sustav enzima respiratornog lanca.
Mliječna kiselina nastala u procesu glikolize, kao što je već spomenuto, još uvijek sadrži prilično značajnu zalihu (oko 93%) potencijalne energije. No, unatoč tome, prvi živi organizmi koji su vadili energiju u anaerobnim uvjetima pustili su je u okoliš.
Dolaskom kisika u Zemljinu atmosferu, živi organizmi razvili su nove, naprednije oksidacijske mehanizme, zbog čega se količina oslobođene energije pokazala mnogo veća nego tijekom glikolize, budući da je krajnji produkt disanja CO2, čiji je atom ugljika potpuno oksidiran. Uz to, priroda je stvorila nove mehanizme za dodatnu oksidaciju krajnjeg produkta glikolize koji se izlučuje u okoliš. Drugim riječima, čini se da je stvorio nadgradnju nad glikolizom za oksidaciju konačnog proizvoda u aerobnim uvjetima, dok je zadržao mnoge od svojih faza kao i prije.
Disanjem se ne stvara mliječna kiselina. Stoga je pirogrožđana kiselina uobičajeni supstrat, odnosno središnja karika gdje se završava glikoliza i počinje disanje (ili se putevi glikolize i disanja – anaerobna i aerobna oksidacija glukoze) razilaze.
Zadržavši prethodne faze glikolize, stanice ljudskog tijela i viših životinja zadržale su sposobnost oksidacije glukoze u anaerobnim uvjetima, zbog čega su, uz nedostatak kisika, sposobne primati energiju na ovaj način. Međutim, istovremeno se u anaerobnim uvjetima stvara mliječna kiselina, koja ima prilično veliku zalihu energije, ne ispušta se u okoliš, već se nakuplja u mišićima. Iz mišića se krvotokom prenosi u jetru, gdje se ponovno pretvara u glukozu. Kada u stanicu uđe dovoljna količina kisika, dio mliječne kiseline dalje se oksidira u CO 2 i H 2 O.
Transformacija mliječne kiseline. Mliječna kiselina nastala tijekom anaerobne oksidacije glukoze oksidira se u CO 2 i H 2 O na sljedeći način. Prvo, pod djelovanjem enzima laktat dehidrogenaza,čiji je koenzim NAD, oksidira se u pirogrožđanu kiselinu:
na koji se onda utječe piruvat dekarboksilaza, koji je složen polienzimski kompleks, podvrgava se oksidativnoj dekarboksilaciji s stvaranjem aktivnog oblika octene kiseline - acetil-CoA:

gdje je TPP tiamin pirofosfat; LA - lipoična kiselina; HSKOA - koenzim A.
U slučaju kada su tkiva dobro opskrbljena kisikom, pirogrožđana kiselina se odmah podvrgava oksidativnoj dekarboksilaciji, a da se ne reducira u mliječnu kiselinu. Reducirani koenzim NAD H + H + , nastao tijekom oksidacije gliceraldehid-3-fosfata, prenosi vodik putem enzima aerobnog metabolizma (tj. respiratornog lanca) do kisika, tvoreći vodu.
Pretvorba pirogrožđane kiseline u acetil-CoA je pripremna, odnosno prijelazna faza, zbog koje se ugljikohidrati kroz pirogrožđanu kiselinu, a zatim kroz acetil-CoA, uključuju u novu fazu - oksidaciju kisika. Drugim riječima, ovaj proces je veza između glikolize i samog disanja. Međutim, već kao rezultat oksidativne dekarboksilacije pirogrožđane kiseline u acetil-CoA oslobađa se oko 9% ukupne energije oksidacije glukoze, t.j. više nego kod glikolize u cjelini, gdje se oslobađa samo 5-7% energije. S obzirom na 5-7 % energije glikolize i 9% energije oksidativne dekarboksilacije pirogrožđane kiseline, tada se oslobađa ukupno 14-16% energije akumulirane u ugljikohidratima. Stoga preostalih 84-86 % energija se pohranjuje u molekuli octene kiseline.
Ciklus trikarboksilne kiseline (Krebsov ciklus) je novi, napredniji mehanizam za oksidaciju ugljikohidrata, razvijen u živim organizmima s pojavom kisika na Zemlji. Uz pomoć ovog mehanizma dolazi do daljnje pretvorbe octene kiseline u obliku acetil-CoA u CO 2 i H 2 O u aerobnim uvjetima uz oslobađanje energije.
Zbog činjenice da su prvi supstrati u procesu oksidacije octene kiseline trikarboksilne kiseline, a hipotezu o mehanizmu te oksidacije iznio je X. A. Krebs, proces je nazvan ciklus trikarboksilne kiseline, odnosno Krebsov ciklus.
Prva reakcija ciklusa je reakcija kondenzacije acetil-CoA s oksalooctenom kiselinom, koju katalizira enzim citrat sintaza. Kao rezultat, nastaje aktivni oblik limunske kiseline, citril-KoA:

Hidroliziran, citril-CoA se pretvara u limunsku kiselinu:

Potonji pod djelovanjem enzima akonitat hidrataze prelazi u cis-akonitnu kiselinu, koja se dodavanjem vode pretvara u izocitnu kiselinu:

Izocitritna kiselina se dalje oksidira odvajanjem dvaju vodikova atoma, pretvarajući se u oksalojantarnu kiselinu. Ovom reakcijom započinje uklanjanje CO 2 i prva oksidacija acetil-CoA u trikarboksilnom ciklusu. Oksalno-jantarna kiselina, dekarboksilirana, prelazi u α-ketoglutarnu kiselinu. Dehidrogenaciju izocitrične i dekarboksilaciju oksalno-jantarne kiseline katalizira enzim izocitrat dehidrogenaza uz sudjelovanje koenzima NAD +:

Sljedeći korak u ciklusu trikarboksilne kiseline je oksidativna dekarboksilacija α-ketoglutarne kiseline, što rezultira stvaranjem jantarne kiseline. Ovaj proces se odvija u dvije faze. Prvo, α-ketoglutarna kiselina podvrgava se oksidativnoj dekarboksilaciji da nastane aktivni oblik jantarne kiseline - sukcinil-CoA - i CO 2 . Ova reakcija podsjeća na reakciju pretvorbe pirogrožđane kiseline u acetil-CoA, a također je katalizira složeni polienzimski kompleks - α -ketoglutarat dehidrogenaza. Kao rezultat ove reakcije dolazi do druge eliminacije ugljičnog dioksida i dehidrogenacije octene kiseline koja je ušla u ciklus:

Rezultirajući aktivni oblik jantarne kiseline, sukcinil-CoA, za razliku od acetil-CoA, je visokoenergetski tio-eterski spoj, u kojem se akumulira energija oksidacije α-ketoglutarne kiseline.
U sljedećoj fazi, ova energija se koristi za stvaranje GTP (gvanozin trifosforne kiseline) iz GDP-a i anorganske fosforne kiseline i pohranjuje se u fosfatnim vezama ovog spoja. Reakciju katalizira enzim sukciniltiokinaza:

GTP nastao kao rezultat ove reakcije stupa u interakciju s ADP-om, što rezultira stvaranjem ATP-a:
GTP + ADP BDP + ATP.
Sinteza ATP-a u kombinaciji s oksidacijom supstrata još je jedan primjer fosforilacije supstrata.
U daljnjem tijeku ciklusa trikarboksilne kiseline događaju se još dvije dehidrogenacije. Jantarna kiselina pod djelovanjem sukcinat dehidrogenaza uz sudjelovanje koenzima FAD + odcjepljuje dva atoma vodika i pretvara se u fumarnu kiselinu, a FAD + se reducira u FAD H 2. Tada fumarna kiselina pričvršćivanjem molekule vode tvori jabučnu kiselinu (malat) koja uz pomoć malat dehidrogenaza a koenzim NAD + ponovno prolazi kroz dehidrogenaciju. U tom slučaju nastaje oksalo-octena kiselina, t.j. supstrat s kojeg je započeo ciklus trikarboksilne kiseline:

Regenerirana oksalooctena kiselina može ponovno reagirati s novom molekulom acetil-CoA, a proces će započeti istim redoslijedom.
Opća shema ciklus trikarboksilne kiseline može se predstaviti na sljedeći način:
Ciklus trikarboksilne kiseline

(kutije prikazuju krajnje produkte oksidacije acetil-CoA).
Iz gornjeg dijagrama proizlazi da je glavna funkcija Krebsovog ciklusa dehidrogenacija octene kiseline. Ako uravnotežimo enzimsku dehidrogenaciju jednog ciklusa, lako možemo izračunati da se kao rezultat reakcija formira osam atoma vodika: šest atoma se koristi za smanjenje NAD +, a dva - za smanjenje FAD + sukcinat hidrogenaze.
Ukupna reakcija ovog ciklusa opisana je sljedećom jednadžbom:
CH3COOH + 2H2O → 2CO2 + 8H,
iz čega proizlazi da četiri atoma vodika pripadaju vodi. Posljedično, preostala četiri nastala su tijekom dehidrogenacije octene kiseline, t.j. ovo je sav vodik koji je bio u sastavu njegove molekule. Istodobno su dva ugljikova atoma otpuštena u obliku ugljičnog monoksida (IV) dva puta (jednom tijekom dekarboksilacije oksalno-jantarne kiseline, drugi - tijekom dekarboksilacije α-ketoglutarne kiseline), t.j. točno onoliko koliko su ušli u ciklus u obliku acetalne skupine.
Iz gornje jednadžbe također proizlazi da u ciklus ne sudjeluju ni kisik, ni ATP, ni anorganska fosforna kiselina. Svi ovi metaboliti međusobno djeluju u respiratornom lancu, što uključuje anorgansku fosfornu kiselinu, atome vodika i kisik koji se odvajaju tijekom dehidrogenacije, a ATP nastaje kao rezultat oksidativne fosforilacije. Energija za ovaj proces oslobađa se kao rezultat redoks reakcija tijekom prijenosa atoma vodika i elektrona iz reduciranih oblika NAD H 2 i FAD H 2 na kisik.
Proces oksidativne fosforilacije detaljno je opisan u pogl. 22. Podsjećamo samo da za svaki par elektrona (par vodikovih atoma) u respiratornom lancu nastaju tri ATP molekule oksidativnom fosforilacijom (jedna tijekom prijenosa atoma vodika s NAD H + H + na FAD, druga - tijekom prijenosa para elektrona iz citokroma b na citokrom S a treći - od citokroma a 3 na atom kisika). Dakle, svaki oksidativni stupanj u pretvorbi glukoze u CO 2 i H 2 O, povezan s NAD, prati stvaranje tri molekule ATP-a, povezane s FAD-om – stvaranje dvije molekule ATP-a.
Energetska ravnoteža oksidacije ugljikohidrata. Najprije sumiramo energetsku ravnotežu zbog dehidrogenacije octene kiseline u Krebsovom ciklusu. Kao što smo već utvrdili, u ovom ciklusu događaju se četiri dehidrogenacije, što je rezultiralo stvaranjem tri reducirana oblika NAD, jedne FAD, a jedna molekula ATP je sintetizirana fosforilacijom supstrata:
Dakle, šest puta više ATP se sintetizira u Krebsovom ciklusu nego u glikolizi. Ako uzmemo u obzir još dvije reducirane NAD molekule nastale oksidacijom mliječne i pirogrožđane kiseline, onda će to iznositi još 6 molekula ATP-a, a ukupno - 18. Budući da se glukoza razlaže na dvije fosfotrioze, količina ATP-a se povećava za 2 puta i bit će 36 molekula.
Dodajući tome 2 ATP molekule nastale tijekom glikolize, dobivamo ukupnu ravnotežu energije akumulirane u makroergijskim vezama ATP-a tijekom oksidacije glukoze u CO 2 i H 2 O: 36 + 2 = 38.
Utvrđeno je da potpunu oksidaciju 1 mol glukoze u CO 2 i H 2 O prati oslobađanje 2872 kJ. 38 ATP molekula akumulira 1270-1560 kJ, t.j. približno 50% ukupne energije koja se oslobađa tijekom procesa oksidacije. Dakle, preostalih 50 % energija se u tijelu raspršuje u obliku topline kako bi se održala odgovarajuća temperatura.
Od razmatranih faza oksidacije glukoze, aerobna faza je od iznimne važnosti. Ako tijekom anaerobne oksidacije, t.j. prilikom stvaranja mliječne kiseline oslobađa se samo 197 kJ energije, od čega 40 % akumulira se u makroergijskim vezama dvije ATP molekule, tada se u aerobnoj fazi oslobađa 2872 - 197 = 2675 kJ, što je oko 93% ukupne energije. Dakle, tijelo prima glavninu energije kroz disanje.
Apotomijski način oksidacija glukoze. Uz Krebsov ciklus u mnogim stanicama, postoji još jedan način razgradnje glukoze, tzv apotomski, ili pentoza fosfat. Eksperimentalno je utvrđeno da se u aerobnim uvjetima u eritrocitima, jetri i bubrezima glukoza može oksidirati u 6-monofosfoglukonsku kiselinu, a fruktoza-1,6-difosfat pri tom ne nastaje. Kao rezultat ove oksidacije glukoze nastaje značajna količina pentoza. Ovaj put je otkrio sovjetski biokemičar V. A. Engelhardt, a njegove pojedinačne faze proučavali su O. Warburg, F. Dickens, I. D. Golovatsky i dr. Pentozofosfatni put nije glavni put za oksidaciju glukoze. Njegova glavna svrha je opskrba stanica smanjenim oblicima NADP-a, potrebnim za biosintezu masnih kiselina, kolesterola, purinskih i pirimidinskih baza, steroida itd. Druga funkcija ovog puta je da opskrbljuje pentoze, uglavnom D-ribozu, za sinteza nukleinskih kiselina.
Put pentoza fosfata za razgradnju glukoze može se sažeti sljedećom jednadžbom:
Glukoza-6-monofosfat + 2 NADP + → Riboza-5-monofosfat + CO 2 + 2 NADP H + H + + 2H +.
Pentoze koje se ne koriste za biosintezu nukleinskih kiselina i nukleotida troše se na biosintezu drugih spojeva i regeneraciju glukoze.
biosinteza ugljikohidrata
Postoje dva glavna načina biosinteze ugljikohidrata iz relativno nekompliciranih metabolita. Jedna od njih je redukcija ugljičnog dioksida u glukozu. Ovaj proces, karakterističan za zelene biljke i tzv fotosinteza, provodi se zbog energije sunčeve svjetlosti uz pomoć klorofila prema sljedećoj jednadžbi:
CO 2 + 2H 2 O 1 / 6C 6 H 12 O 6 + O 2 + H 2 O.
Hvateći sunčeve zrake i pretvarajući njihovu energiju u energiju ugljikohidrata, zelene biljke osiguravaju očuvanje i razvoj života na Zemlji. To je, prema K. A. Timiryazevu, kozmička uloga zelenih biljaka kao posrednika između sunca i cijelog života na Zemlji.
Nedavno je rad grupe znanstvenika s Instituta za biokemiju. A. V. Palladin iz Akademije znanosti Ukrajinske SSR pod vodstvom akademika M. F. Gulyja pokazao je da su tkiva viših životinja također sposobna fiksirati ugljični dioksid, iako se mehanizam fiksiranja razlikuje od mehanizma fotosintetskih stanica. Sastoji se od izgradnje ugljičnog kostura ugljičnim monoksidom (IV) takvih supstrata kao što su keto kiseline, masne kiseline, aminokiseline itd.
U jetri, bubrezima i skeletnim mišićima ljudi i viših životinja postoji još jedan put za biosintezu ugljikohidrata tzv. glukoneogeneza. To je sinteza glukoze iz pirogrožđane ili mliječne kiseline, kao i iz takozvanih glikogenih aminokiselina, masti i drugih prekursora, koji se tijekom metabolizma mogu pretvoriti u pirogrožđanu kiselinu ili metabolite ciklusa trikarboksilne kiseline.
Glukoneogeneza je obrnuti put od glikolize. Međutim, postoje tri koraka na ovom putu koji se ne mogu energetski iskoristiti u pretvorbi pirogrožđane kiseline u glukozu. Ova tri koraka glikolize zamijenjena su "bypass" reakcijama s manjim unosom energije.
Prva bypass reakcija je pretvorba pirogrožđane kiseline u fosfoenolpirogrožđanu kiselinu. Budući da se razgradnja glukoze događa u mitohondrijima, a sinteza u citoplazmi, u prvoj fazi mitohondrijska pirogrožđana kiselina se prvo pretvara u oksalooctenu kiselinu. Ovu transformaciju katalizira enzim piruvat karboksilaza, aktivirani acetil-CoA uz sudjelovanje ATP-a. Rezultirajuća oksalo-octena kiselina se zatim reducira uz sudjelovanje NAD H + H + u jabučnu kiselinu:
Pirogrožđana kiselina + CO 2 Oksalooctena kiselina  Jabučna kiselina.
Jabučna kiselina.
Jabučna kiselina difundira u citoplazmu, oksidira se citoplazmatskom malat dehidrogenazom uz stvaranje citoplazmatske oksalooctene kiseline iz koje nastaje fosfoenolpirogrožđana kiselina. Ova reakcija je katalizirana fosfoenolpiruvat karboksikinaza. Donator fosforne kiseline je GTP:
Jabučna kiselina  Oksaloctena kiselina Fosfoenolpirogrožđana kiselina.
Oksaloctena kiselina Fosfoenolpirogrožđana kiselina.
Nakon toga slijedi cijeli niz obrnutih reakcija, koje završavaju stvaranjem fruktoza-1,6-difosfata. Pretvorba fruktozo-1,6-difosfata u fruktozo-6-fosfat druga je ireverzibilna reakcija glikolize. Stoga ga ne katalizira fosfofruktokinaza, već fruktoza difosfataza. Ovaj enzim katalizira ireverzibilnu hidrolizu 1-fosfatne skupine:
Fruktoza-1,6-difosfat + H 2 O → Fruktoza-6-fosfat + H 3 RO 4.
U sljedećem (reverzibilnom) stupnju biosinteze glukoze, fruktoza-6-fosfat se pretvara u glukoza-6-fosfat pod djelovanjem fosfogluko-izomeraze glikoliza.
Razgradnja glukoza-6-fosfata u glukozu je treća ireverzibilna reakcija koja se ne provodi preokretom heksokinazom. Slobodnu glukozu proizvodi glukoza-6-fosfataza, katalizira reakciju hidrolize:
Glukoza-6-fosfat + H 2 O → Glukoza + H 3 PO 4.
U većini stanica glukoza-6-fosfat, nastao tijekom glikogenolize, koristi se kao prekursor za biosintezu oligo- i polisaharida. Spoj igra važnu ulogu u biosintezi ovih složenih šećera uridin fosfoglukoza, koji djeluje kao srednji transporter glukoze.
Tijekom biosinteze glikogena, na primjer, glukoza-6-fosfat, pretvarajući se u glukozu-1-fosfat pod djelovanjem fosfoglukomutaze, stupa u interakciju s uridin trifosfornom kiselinom (UTP) - spojem sličnim ATP-u, koji umjesto adenina uključuje dušik. baza uracil. Kao rezultat ove interakcije, glukoza-I-fosfat uridiltransferaza nastaje uridil difosfoglukoza:
Glukoza-1-fosfat + UTP UDP-glukoza + Fn.
U završnoj fazi biosinteze glikogena u reakciji koju katalizira glikogen sintetaza, ostatak glukoze iz UDP-glukoze se prenosi na terminalni ostatak glukoze lanca amilaze uz stvaranje 1,4-glikozidne veze (vidi Poglavlje 16). Grananje glikogena kroz stvaranje 1,6 veza je završeno amil-1,4-1,6-transglukozidaza.
Biosinteza glikogena ne provodi se samo iz glukoza-6-fosfata, nastalog glukoneogenezom. Kao što je gore navedeno, dio glukoze nakon apsorpcije također se koristi za njegovu biosintezu. Sinteza glikogena, kao proces stvaranja pokretne rezerve ugljikohidrata u tijelu, od velike je biološke važnosti. Vodeća uloga u tome pripada jetri. Zahvaljujući sintezi i taloženju glikogena u jetri, održava se stalna koncentracija glukoze u krvi i drugim tkivima, te se sprječava njezin gubitak u mokraći prilikom jela, posebice ugljikohidrata. Osim toga, taloženje glikogena u jetri pridonosi postupnom korištenju ugljikohidrata, ovisno o stanju organizma.
Korištenju glukoze za sintezu glikogena prethodi stvaranje glukozno-fosfornih estera. Prvo nastaje glukoza-so-6-monofosfat. Izvor energije i donor fosfata je ATP. Ovu reakciju katalizira heksokinaza. Pod djelovanjem enzima fosfoglukomutaze, glukoza-6-monofosfat se pretvara u glukoza-1-monofosfat:

Daljnja pretvorba glukoza-1-monofosfata u glikogen odvija se na način koji nam je već poznat.
Poglavlje 24
Lipidi su velika skupina organskih spojeva. Svi se razlikuju po svom kemijski sastav i strukturu, ali imaju jedno zajedničko svojstvo za njih - netopivost u vodi. Budući da enzimi koji djeluju na ove organski spojevi, topiv u vodi, cijepanje i apsorpcija lipida u probavnom kanalu karakteriziraju neke značajke. Prisutnost lipida različite strukture uzrokuje različite načine njihova cijepanja i sinteze.
Zadržimo se na metabolizmu masti, fosfatida i sterida, koji imaju najvažniji biološki značaj.
Metabolizam lipida, kao i ugljikohidrata, višestupanjski je proces koji se sastoji od probave, apsorpcije, transporta lipida krvlju, unutarstanične oksidacije i biosinteze.
Probava lipida
Probava triglicerida. Trigliceridi, ili neutralne masti, koncentrirani su izvori energije u tijelu. Kada se 1 g masti oksidira, oslobađa se oko 38,9 kJ energije. Kao hidrofobni spojevi, masti se pohranjuju u kompaktnom obliku, zauzimajući relativno malo prostora u tijelu. Zajedno s hranom, dnevno u ljudski organizam ulazi do 70 g biljnih i životinjskih masti. Po svojoj kemijskoj prirodi, oni su uglavnom trigliceridi.
Masti se razgrađuju enzimima tzv lipaze. Slina ne sadrži takve enzime, pa se masti ne mijenjaju u usnoj šupljini. U želucu je aktivnost lipaze vrlo slaba. To je zbog činjenice da je u želucu reakcija medija jako kisela (pH = 1,5-2,5), dok je optimalno djelovanje lipaze pri pH = 7,8 = 8,1. U tom smislu, samo 3-5% ulaznih masti probavlja se u želucu.
Probava masti u želucu događa se samo u novorođenčadi i dojenčadi. To je zbog činjenice da je pH okoliša u želucu novorođenčadi 5,6, au tim uvjetima lipaza je aktivnija. Osim toga, mast majčinog mlijeka, koja je osnovna hrana djece u tom razdoblju, je u visoko emulgiranom stanju, a samo mlijeko sadrži lipolitički faktor koji sudjeluje u probavi masti.
Međutim, želudac još uvijek igra ulogu u procesu probave masti kod odraslih. Regulira protok masti u crijeva i probavlja bjelančevine te tako oslobađa masnoću iz kompleksa lipoproteina hrane.
Glavno mjesto probave masti je duodenum i tanko crijevo. Budući da su masti netopive u vodi, a enzimi koji ih razgrađuju su spojevi topivi u vodi, nužan uvjet za hidrolitičku razgradnju masti na sastavne dijelove je njihov disperzija(drobljenje) da nastane tanka emulzija. Disperzija i emulgiranje masti nastaje kao posljedica djelovanja nekoliko čimbenika: žučnih kiselina, slobodnih viših masnih kiselina, mono- i diglicerida te proteina. Tome također doprinosi peristaltika crijeva i stalno formirani ugljični dioksid koji se oslobađa tijekom interakcije kiselih komponenti hrane koja dolazi iz želuca s karbonatima crijeva, koji stvaraju alkalna sredina. Nastali ugljični dioksid "mjehuriće" kroz masu hrane, sudjelujući tako u raspršivanju masti. Neutralizacija sadržaja želuca također je olakšana ulaskom žuči u lumen tankog crijeva, koja ima alkalni karakter.)
Žuč je viskozna tekućina svijetložute boje specifičnog mirisa, gorkog okusa. Žuč sadrži žučne kiseline. žučni pigmenti, produkti razgradnje hemoglobina, kolesterol, lecitin, masti, neki enzimi, hormoni itd. Žuč pospješuje peristaltiku tankog crijeva, ima bakteriostatski učinak na njegovu mikrofloru. Otrovi se izlučuju iz tijela žuči. Također je aktivator lipolitičkih enzima i povećava propusnost crijevne stijenke.
Dom sastavni diožuči su žučne kiseline. Nastaju u jetri iz kolesterola i nalaze se u žuči kako u slobodnom tako iu vezanom stanju, kao i u obliku natrijevih soli. Ljudska žuč sadrži uglavnom tri žučne kiseline. Najveći dio su holna (3,7,12-trihidroksiholanska) i deoksiholna (3,12-dihidroksiholanska), manji dio su litoholne (3-hidroksiholanske) kiseline koje su derivati holanske kiseline:

Količna kiselina se također može naći u žuči u vezanom stanju u obliku uparenih spojeva s glicinom i taurinom derivatom cisteina - glikokolna i tauroholna kiselina, respektivno:
 Natrijeva sol glikokolne kiseline
Natrijeva sol glikokolne kiseline
 Natrijeva sol tauroholne kiseline
Natrijeva sol tauroholne kiseline
Zbog prisutnosti žučnih kiselina dolazi do smanjenja površinska napetost lipidnih kapljica, što doprinosi stvaranju vrlo fine i stabilne emulzije promjera čestica od oko 0,5 mikrona. Stvaranje emulzije također olakšavaju monogliceridi i više masne kiseline. Emulgiranje masti dovodi do ogromnog povećanja kontaktne površine lipaze s Vodena otopina. Dakle, što je tanja emulzija masti, to ih lipaza bolje i brže razgrađuje. Osim toga, u obliku tanke emulzije, masti se čak mogu apsorbirati izravno u crijevnu stijenku, bez cijepanja na sastavne dijelove.
U prisutnosti žučnih kiselina, pod djelovanjem lipaze, dolazi do hidrolitičkog cijepanja masti u lumenu tankog crijeva. Kao rezultat toga nastaju proizvodi djelomične i potpune razgradnje masti - mono- i digliceridi, slobodne više masne kiseline i glicerol:


Sadrži i dio nerazdvojene masti u obliku vrlo tanke emulzije. Svi ovi proizvodi se dalje apsorbiraju u crijevnoj stijenci. U ovoj mješavini, trigliceridi su oko 10 % , mono-
idisaharidi - također 10 % , a najveći dio - oko 80% - proizvodi potpune razgradnje masti - glicerin i više masnoće
Probava fosfoglicerida. Glavno mjesto probave fosfatida je i duodenum. Do emulgiranja ovih lipida dolazi pod utjecajem istih tvari kao i trigliceridi. Međutim, hidrolitičko cijepanje fosfatida provodi se pod djelovanjem fosfolipaza A, B, C i D. Svaki enzim djeluje na specifičnu estersku vezu fosfolipida. Hidrolitičko cijepanje, na primjer, lecitina događa se na sljedeći način:








Neznatan dio fosfatida podliježe takvom potpunom cijepanju, budući da su njegovi međuprodukti vrlo topljivi u vodi i lako se apsorbiraju u crijevnoj stijenci. Osim toga, fosfogliceridi lako tvore emulzije, koje također može apsorbirati crijevna stijenka.
Probava steroida. Steridi hrane se emulgiraju pod utjecajem istih čimbenika kao i masti, nakon čega se podvrgavaju hidrolitičkom cijepanju na slobodne sterole i više masne kiseline. Taj se proces provodi djelovanjem enzima. kolesterolesteraza.
Apsorpcija lipida
Kao rezultat probave masti, fosfatida, sterida u lumenu tankog crijeva nastaje značajna količina proizvoda njihovog djelomičnog i potpunog hidrolitičkog cijepanja: mono- i digliceridi, više masne kiseline, steroli, dušične baze, fosfor kiselina. Također sadrži malu količinu triglicerida u fino emulgiranom stanju. Sve ove proizvode apsorbira stijenka tankog crijeva.
Proizvodi cijepanja kao što su masne kiseline i kolesterol, slabo topljivi u vodi, tvore u vodi topive komplekse sa žučnim kiselinama – tzv. koleinske kiseline. Ove kiseline lako prodiru u epitelne stanice crijevne stijenke, gdje se razgrađuju na sastavne dijelove. Oslobođene žučne kiseline vraćaju se u lumen crijeva i ponovno se koriste za transport u vodi netopivih proizvoda razgradnje masti.
Dio produkata cijepanja (glicerol, glicerol-fosforna kiselina, dušične baze) vrlo su topljivi u vodi i lako prodiru u epitelne stanice. Fosforna kiselina apsorbira u epitelne stanice stijenke tankog crijeva u obliku natrijevih i kalijevih soli. Apsorpcija lipida temelji se na nizu složenih fizikalno-kemijskih i bioloških procesa, za čiju provedbu se troši energija makroergijskih veza ATP-a.
U epitelnim stanicama crijevne sluznice ponovno se sintetiziraju lipidi iz apsorbiranih produkata hidrolitičkog cijepanja. Međutim, ta resinteza dovodi do stvaranja specifičnih masti karakterističnih za ovaj organizam.
Za stvaranje neutralnih masti koriste se više masne kiseline, glicerol, mono- i digliceridi. Istodobno dolazi i do sinteze fosfatida, za što se uglavnom koriste glicerol-fosfatna kiselina, gliceridi i digliceridi, kao i monogliceridi u maloj količini. Steridi nastaju od kolesterola i viših masnih kiselina.
U epitelnim stanicama crijevne stijenke od sintetiziranih lipida, kao i kapi apsorbiranih triglicerida, vitamina (A, D, E, K) i proteina nastaju kompleksi veličine 150-200 nm tzv. bolesnih mikrona. Unutarnji sadržaj hilomikrona, predstavljen raznim vrstama nastalih lipida, uglavnom triglicerida, okružen je vanjskim proteinskim omotačem, zbog čega se hilomikroni dobro otapaju u vodi. Hilomikroni difundiraju prvo u međustaničnu tekućinu, zatim u limfne kapilare, a na kraju ulaze u krvotok, gdje se pod djelovanjem heparina razgrađuju na male čestice. Protokom krvi se raznose po cijelom tijelu i talože u rezervi u masnim depoima - potkožnom i perirenalnom tkivu, omentumu, mezenteriju, mišićnom tkivu. Dio masnoća u krvi koristi se u plastične svrhe, kao izvor kemijska energija itd.
Dakle, hilomikroni su nosioci lipida koji nastaju u epitelnim stanicama tankog crijeva. U isto vrijeme transportiraju uglavnom trigliceride u krv.
Uz hilomikrone, postoje i drugi oblici transporta lipida u krvi, kao što su α- i β-lipoproteini. Njihove molekule su složeni kompleksi lipida s proteinima. α-Lipoproteini su glavni transportni oblici fosfatida, β-lipoproteini su prijenosnici kolesterola i njegovih estera.
Najmobilniji oblik lipida su slobodne više masne kiseline.
Važna uloga u aktivnom transportu lipida pripada krvnim stanicama. Eritrociti, na primjer, sudjeluju u prijenosu fosfatida i kolesterola, leukociti - triglicerida.
Veliku ulogu u metabolizmu lipida imaju depoi masti. Istraživanja su pokazala da se ne samo specifične vrste masti, novosintetizirane u tijelu, već i strane masnoće u malim količinama, odnosno talože u masnim depoima. uključeno u hranu. Eksperimenti provedeni na izgladnjelim psima pokazali su da nakon apsorpcije, prehrambene masti prvo ulaze u depoe masti iz kojih prelaze u krvnu plazmu.
Dakle, masno tkivo nije pasivni depo masti, njegov se sastav stalno ažurira zbog lipida koji se apsorbiraju iz crijeva ili sintetiziraju u tijelu.