Unutar date konfiguracije, makromolekula ima veliki broj unutarnji stupnjevi slobode povezani s rotacijom oko osi jednostrukih veza glavnog lanca. Kao posljedica toga, makromolekula može poprimiti različite oblike ( konformacije), tj. polimere karakterizira konformacijska izomerija.
Konformacija je prostorni raspored atoma i atomskih skupina koji se može mijenjati bez prekida kemijske veze glavna vrijednost kao rezultat toplinskog kretanja i (ili) vanjskih utjecaja.
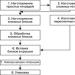
Dolje je shematski prikaz mehanizma konformacijske promjene izotaktičke trijade vinilnog polimera kao rezultat rotacije od 180° oko C-C veze. Očito, takvi konformacijski prijelazi nisu popraćeni promjenom zadane konfiguracije i kidanjem kemijskih veza.
Tako, konformacijski izomerizam makromolekula određen je unutarnjom rotacijom oko jednostrukih kemijskih veza strukture polimernog lanca.
Glavne odredbe konformacijske izomerije makromolekula
Razmotrimo glavne zakonitosti unutarnje rotacije oko kemijskih veza na primjeru niskomolekularnog modela - 1,2-dikloroetana.

Zbog međudjelovanja bočnih supstituenata (Hi C1), uz potpunu rotaciju oko osi veze -C-C- za 360° u molekuli 1,2-dikloroetana sukcesivno se ostvaruje više različitih rotacijskih izomera, odn. konformeri, s određenom potencijalnom energijom. Grafički se to može prikazati kao energetska karta - ovisnost potencijalne energije konformera o kutu rotacije. Za 1,2-dikloroetan, slična karta je shematski prikazana na Sl. 1.3.

Riža. 1.3. Ovisnost o potencijalnoj energiji U valentno nevezani atomi molekule 1,2-dikloroetana na kut zakreta
Molekule ovog tipa imaju tri stabilne konformacije: jednu trans- i dvije gauche konformacije (od fr. gauche- kosi, nakošeni), koji odgovaraju minimumima krivulje potencijala. Maksimumi odgovaraju nestabilnim pomračenim konformacijama, posebno r^u-konformeru.
U polimerima, unutarnja rotacija oko jednostrukih veza ima niz specifičnih značajki u usporedbi sa spojevima niske molekularne težine. Razmotrimo fragment polivinil kloridnog lanca u konfiguraciji glava-na-glava.

Za razliku od 1,2-dikloroetana, u izoliranom fragmentu, umjesto dva atoma II, supstituenti na ugljikovim atomima su nastavci -CH 2 - polimernog lanca. Drugim riječima, tijekom rotacije oko veze između i-tog i (r + 1)-tog atoma ugljika, (r + 2)-ti atom ugljika, praćen nastavkom lanca, ima ulogu supstituenta (Slika 1.4).

Riža. 1.4.
Položaj (r + 2) atoma u odnosu na prethodnu vezu dan je bazom stošca, uzimajući u obzir valentni kut 0. Međutim, rotacija od 360 ° moguća je samo kada se kreće u prostoru kao prošireni nastavak lanca, za što je potrebna ogromna toplinska energija, koja u pravilu premašuje energiju disocijacije kemijskih veza. Kao rezultat, unutarnja rotacija u polimerima je inhibiran a ostvaruje se unutar određenog luka kružnice. Veličina ovog luka određuje kut usporene unutarnje rotacije f. Vrijednost kuta otežane unutarnje rotacije ovisi o temperaturi, prirodi kemijske veze, polarnosti i volumenu supstituenata, konfiguracijskom sastavu polimera itd.
Tako se u prvoj aproksimaciji unutarnja rotacija u polimernim lancima svodi na rotaciju svake sljedeće veze u odnosu na prethodnu. U stvarnosti, ti događaji imaju izražen kooperativni karakter, budući da je rotacija dviju susjednih veza jedna u odnosu na drugu u velikoj mjeri određena sličnim procesima u bliskoj okolini i interakcijama na velikim udaljenostima. S tim u vezi, u slučaju polimera, kut otežane unutarnje rotacije je prosječna vrijednost. Kvantitativne procjene ove karakteristike bit će dane u nastavku.
Od istog polimera u visokoelastičnom stanju razlikuje se pokretljivošću elemenata struktura makromolekula, odnosno vremenima relaksacije: za makromolekule, segmente i supramolekulske tvorevine u staklastom stanju ona su vrlo velika i često premašuju ispitna ili radna vremena. vrijeme polimera. Potonje potvrđuje činjenica da vrijednost temperature staklenog prijelaza ovisi o vremenu izlaganja uzorka polimera u procesu fizičkog ili mehaničkog utjecaja.
Kristalizacija celuloznog triacetata odvija se na različite načine ovisno o uvjetima.U većini slučajeva savijanje polimernih makromolekula odvija se nepravilno. Najizraženija kristalna područja slabo su povezana s ostatkom polimerne mase. Ova izražena kristalna područja su, takoreći, uronjena u amorfno područje celuloznog triacetata. Neizražena kristalna područja jače su povezana s polimernom masom Ne mogu se odvojiti. od ostatka mase bez razaranja
U isto vrijeme, brzina stvaranja kristalne faze iz otopina s niskom prezasićenošću je vrlo niska. Spontano stvaranje jezgri nove (kristalne) faze zahtijeva fluktuacijsku kombinaciju skupine segmenata nekoliko polimernih makromolekula, i to ne samo kombinaciju u strogom geometrijskom poretku, već i takvu kvantitativnu kombinaciju da je kritična vrijednost jezgre prekoračen. Ukratko, ovdje su sačuvane sve zakonitosti nukleacije karakteristične za niskomolekularne sustave, s jedinom kompliciranom razlikom što je zbog niske pokretljivosti makromolekula znatno smanjena vjerojatnost pojave centra kristalizacije i potrebno je vrlo dugo vrijeme ili značajno prezasićenje otopine za odvajanje kristalne faze, što povećava vjerojatnost fluktuacijskog stvaranja jezgri. Drugo ograničenje kristalizacije može biti postizanje takvih koncentracija polimera pri kojima viskoznost sustava postaje vrlo visoka, pokretljivost makromolekula naglo opada (praktički nestaje tijekom staklastog prijelaza), a kristalizacija je nemoguća. "Ove ekstremne slučajeve treba detaljnije razmotriti, posebice, kada se analiziraju fazne transformacije u želeu.
Planarna cik-cak konformacija u makromolekuli polietilena može se lako postići zbog činjenice da su vodikovi atomi male veličine: njihov van der Waalsov polumjer je 0,12 nm (1,2 A). Kada se atomi vodika zamjenjuju drugim atomima ili skupinama, na primjer, atomi klora [radijus 0,18 nm (1,8 A) | ili fluor [radijus 0,15 nm (1,5 A)], u većini slučajeva lanac više ne može održavati planarnu konformaciju, budući da veliki atomi uzrokuju značajna naprezanja u makromolekuli. Stoga većina polimernih makromolekula ima spiralnu konformaciju. U tom slučaju razdoblje identiteta može uključivati jedno ili više njih. spiralni zavoji. Na primjer, u makromolekuli politetrafluoroetilena, koja ima oblik blago upletene spirale, na temperaturi ispod 20 °C, period identiteta [jednak 1,68 nm (16,8 A)] uključuje šest zavoja spirale, u kojima postoje trinaest CF2 jedinica. U temperaturnom rasponu od 20-30 °C lanac se lagano odmotava, tako da ima petnaest karika po razdoblju istovjetnosti. Oblik makromolekule politetrafluoretilena je blizak cilindričnom. Na temperaturama iznad 30 ° C, struktura postaje djelomično poremećena; lanci, bez narušavanja međusobnog rasporeda, osciliraju ili rotiraju zajedno oko svojih osi.
Planarna cik-cak konformacija u makromolekuli polietilena može se lako postići zbog činjenice da su vodikovi atomi male veličine: njihov van der Waalsov polumjer je 0,12 nm (1,2 A). Kada se atomi vodika zamijene drugim atomima ili skupinama, npr. klorom [radijus 0,18 nm (1,8 A)] ili fluorom [radijus 0,15 nm (1,5 A)], u većini slučajeva lanac više ne može održavati ravnu konformaciju, budući da veliki atomi uzrokuju značajna naprezanja u makromolekuli. Stoga većina polimernih makromolekula ima spiralnu konformaciju. U tom slučaju razdoblje identiteta može uključivati jedno ili više njih. spiralni zavoji. Na primjer, u makromolekuli politetrafluoroetilena, koja ima oblik blago uvijene spirale, na temperaturi ispod 20 °C, period identiteta [jednak 1,68 nm (16,8 A)] uključuje šest zavoja spirale, na kojoj je trinaest CF2 jedinice se nalaze. U temperaturnom rasponu od 20-30 °C lanac se lagano odmotava, tako da ima petnaest karika po razdoblju istovjetnosti. Oblik makromolekule politetrafluoretilena je blizak cilindričnom. Na temperaturama iznad 30 ° C, struktura postaje djelomično poremećena; lanci, bez narušavanja međusobnog rasporeda, osciliraju ili rotiraju zajedno oko svojih osi.
Na višoj razini kristalita moguće su dvije vrste disperzije. Prvi je raspodjela jedne komponente u drugoj na mikrorazini u obliku zasebnih kristalita smještenih u područjima matrice sa značajnim nedostatkom gustoće; drugi - makrodistribucija jedne od komponenti kao disperzne faze, a drugi tip distribucije vjerojatniji je pri značajnim koncentracijama dispergirane komponente iu slučaju lošeg prethodnog miješanja. Međutim, u oba slučaja treba očekivati pojavu još jednog tipa rasporeda polimernih makromolekula, koji je karakterističan za prijelazno područje. Treba napomenuti da kada je dispergirana komponenta raspoređena na razini kristalita, vjerojatno je da će se granice faza malo razlikovati od onih koje postoje u čistom polimeru, a koje su posljedica prisutnosti amorfne i kristalne faze.
Postoje mnogi eksperimentalni podaci koji potvrđuju prisutnost prijelaznog sloja na polimernoj površini. Dakle, u mješavini guma možete odrediti energiju kohezije. Kada bi smjesa bila jednofazna, tada bi se kohezijska energija mijenjala sa sastavom smjese duž krivulje koja leži iznad ili ispod aditivne na isti način kao što se mijenja toplina isparavanja smjese niskomolekularnih tekućina. U dvofaznoj smjesi interakcija polimera ograničena je samo međupovršinom, a u nedostatku prijelaznog sloja intenzitet interakcije trebao bi biti nizak. U ovom slučaju, može se misliti da se kohezijska energija aditivno mijenja sa sastavom. Odstupanje od aditivnosti kohezijske energije u smjesi polimera ukazuje na postojanje prijelaznog sloja u kojemu međudjelovaju makromolekule polimera. Prema , energija kohezije u smjesi guma
Plastificiranje polimera obično se smatra tehnološkom metodom za povećanje elastičnih i plastičnih svojstava materijala, odnosno smanjenje njegove krhkosti kao rezultat uvođenja posebno odabranih tvari niske molekulske mase - plastifikatora. U ovom slučaju, kao što je poznato, prijelazne točke polimera iz jedne
1.3. Konfiguracija makromolekula
Pojam konfiguracije uključuje određeni prostorni raspored atoma makromolekula, koji se ne mijenja tijekom toplinskog gibanja. Prijelaz iz jedne konfiguracije u drugu nemoguć je bez kidanja kemijskih veza.
Razlikuju se: 1) konfiguracija veze, 2) poredak kratkog dometa - konfiguracija spojnih veza, 3) poredak velikog dometa - konfiguracija velikih dionica (na primjer, blokovi i njihova izmjena, ili duljina i raspored grana), 5) konfiguracija izduženog lanca u cjelini.
Konfiguracija veze. Primjeri su cis i trans konfiguracije dienskih polimera
1,4-cis-poliizopren 1,4-trans-poliizopren (prirodna guma) (gutaperka) Drugi primjer bi bila l,d-izomerija. Na primjer,
za polimere s ~CH2 –CHR~ jedinicama, gdje je R bilo koji radikal, moguća je tvorba dva izomera: l je lijevo, a d desno
Konfiguracija privitka veze(kratki nalog). Karike u lancu mogu se povezati na način glava-rep i glava-na-čelo:

je vezanost glava-rep, a vezanost glava-na-glavu zahtijeva prevladavanje velikih aktivacijskih barijera.
Kod kopolimera, tipovi strukturnih izomera se povećavaju u usporedbi s homopolimerima. Na primjer, za kopolimere butadiena i stirena moguće je:
1. sekvencijalna izmjena veza -A-B-A-B-A-B-,
2. kombinacija karika u obliku dijada i trijada–AA–BBB–AA–BBB– ,
3. statistička kombinacija poveznica–AA–B–AA–BBB–A–B– . Red konfiguracije dalekoširi se dalje
deseci i stotine atoma u glavnom lancu. Na primjer, veliki nizovi blokova u blok kopolimerima ili veliki nizovi jedinica s istom stereopravilnošću (na primjer, polimeri s izotaktičkom, ataktičkom i sindiotaktičkom strukturom).
Izotaktički Ataktički Sindiotaktički
Ukupna konfiguracija kruga odlučan međusobni dogovor velike sekvence veza (s redoslijedom dugog dometa). Na primjer, za razgranate makromolekule Različite vrste konfiguracije prikazane su na sl.4.
Riža. 4. Konfiguracije makromolekula

1.4. Konformacija makromolekula
Konformacija je promjenjiva raspodjela atoma ili skupina atoma u prostoru koji tvore makromolekulu. Prijelaz iz jedne konformacije u drugu može se dogoditi zbog rotacije, rotacije ili osciliranja veza oko pojedinačnih veza pod djelovanjem toplinskog gibanja ili vanjskih sila i nije popraćen kidanjem kemijskih veza.
Polimeri mogu poprimiti različite konformacije:
Statistička zavrzlama je presavijena konformacija. Nastaje kada intenzitet unutarnjeg toplinskog gibanja prevladava nad vanjskim utjecajem. Karakteristika linearnih polimera [PE, PP, PB, PIB i ljestvičasti polimeri (polifenilensiloksan).
Heliks - nastaje u polimerima zbog H-veza (na primjer, u molekulama proteina i nukleinskih kiselina).
Globula je vrlo kompaktna čestica po obliku bliska sfernom. Karakterističan je za polimere s jakom unutarmolekularnom interakcijom (npr. u PTFE).
Šipka ili žica pronađena u alkil poliizocijanatima.
Konformacija nabora. Karakterističan je za polimere u kristalnom stanju (npr. u PE).
Konformacija radilice realiziran u poli-n-benzamidu.
sl.5. Konformacije makromolekula
1.5. Fleksibilnost makromolekula
Fleksibilnost je jedna od najvažnijih karakteristika polimera koja određuje visokoelastična, relaksacijska i termomehanička svojstva polimera, kao i svojstva njihovih otopina. Fleksibilnost karakterizira sposobnost makromolekula da mijenjaju svoj oblik pod utjecajem toplinskog gibanja karika ili vanjskih mehaničkih utjecaja. Fleksibilnost je posljedica unutarnje rotacije karika ili dijelova makromolekula jedni u odnosu na druge. Razmotrite fenomen unutarnje rotacije u molekulama na primjeru najjednostavnijeg organskog spoja - molekule etana.
U molekuli etana (CH3 -CH3) atomi ugljika povezani su s atomima vodika i međusobno kovalentnim (σ-vezama), a kut između smjerova σ-veza (valentni kut) je 1090 28/. To uzrokuje tetraedarski raspored supstituenata (vodikovih atoma) u prostoru u molekuli etana. Zbog toplinskog gibanja u molekuli etana, jedna CH3 skupina rotira u odnosu na drugu oko osi C-C. U tom se slučaju prostorni raspored atoma i potencijalna energija molekule neprestano mijenjaju. Grafički se različiti ekstremni rasporedi atoma u molekuli mogu prikazati kao projekcije molekule na horizontalnu ravninu (slika 6). Pretpostavimo da je u položaju a potencijalna energija molekule U1, a u položaju b U2, dok je U1 ≠ U2, tj. položaji molekula su energetski nejednaki. Položaj b, u kojem se atomi H nalaze jedan ispod drugog, energetski je nepovoljan, jer se između atoma H javljaju sile odbijanja koje nastoje atome prebaciti u energetski povoljan položaj a. Ako prihvati
U1 =0, zatim U2 =max.

Riža. 6. Projekcijske formule za ekstremni raspored H atoma u prostoru u molekuli etana.
Riža. 7. Ovisnost potencijalne energije molekule o kutu zakreta metilne skupine.
Kada se jedna CH3 skupina zakrene u odnosu na drugu za 600, molekula ide s položaja a na b, a zatim nakon 600 opet na položaj a, i tako dalje. Promjena vrijednosti potencijalne energije molekule etana od kuta rotacije φ prikazana je na sl.7. Molekule slabije simetrije (npr. molekula dikloroetana) imaju složeniju ovisnost U=f(φ).
Potencijalna (U 0 ) ili rotacija aktivacijske barijere
ion je energija potrebna za prijelaz molekule iz položaja minimalne u položaj maksimuma potencijalne energije. Za etan je U0 malen (U0 = 11,7 kJ/mol) i pri
Na normalnoj temperaturi, CH3 skupine rotiraju oko C-C veze velikom brzinom (1010 okretaja u minuti).
Ako molekula ima rezervu energije manju od U0, tada nema rotacije i događa se samo njihanje atoma u odnosu na položaj minimalne energije - to je ograničeno ili
spora rotacija.
U polimerima, zbog intra- i intermolekulskih interakcija, ovisnost U=f(φ) ima složen oblik.
Ako je jedan položaj karike lanca karakteriziran potencijalnom energijom U1, a drugi - U2, tada je energija prijelaza iz jednog položaja u drugi jednaka razlici ∆U= U1 - U2. Razlika između energija prijelaza ∆U iz jednog ravnotežnog položaja jedinice makromolekule u drugi karakterizira termodinamička fleksibilnost. Određuje sposobnost lanca da se savija pod utjecajem toplinskog gibanja.
Druga karakteristika fleksibilnosti je brzina kojom se veze pomiču s jedne pozicije na drugu. Brzina konformacijskih transformacija ovisi o omjeru U0 i energije vanjskih utjecaja. Što je više U0, sporiji su zavoji karika i manja je fleksibilnost. Fleksibilnost makromolekula, određena vrijednošću U0, naziva se kinetički fleksibilan
Čimbenici koji određuju fleksibilnost makromolekula
Ti čimbenici uključuju: vrijednost U0, MM polimera, gustoću prostorne mreže, veličinu supstituenata i temperaturu.
Potencijalna rotacijska barijera (U 0 ). Vrijednost U0 ovisi o intra- i intermolekularnim interakcijama. Razmotrimo čimbenike koji utječu na U0 i fleksibilnost lanca u polimerima ugljičnog lanca.
Karbolančani polimeri
U polimerima ugljikovog lanca, zasićeni ugljikovodici su najmanje polarni. Njihove intra- i intermolekularne interakcije su male, a vrijednosti U0 i ∆U također su male, stoga polimeri imaju visoku kinetičku i termodinamičku fleksibilnost. Primjeri: PE, PP, PIB.
Vrijednosti U0 posebno su niske za polimere u čijem lancu pored jednostruke postoji dvostruka veza.
–CH2 –CH=CH–CH2 – Polibutadien
velikih skupina dovodi do intra- i intermolekulskih interakcija. U ovom slučaju, stupanj polariteta značajno utječe
Uvođenjem polarnih skupina moguća su tri slučaja s obzirom na njihov učinak na fleksibilnost:
1. Polarne skupine su blisko razmaknute a među njima su moguće jake interakcije. Prijelaz takvih polimera iz jednog prostornog položaja u drugi zahtijeva svladavanje velikih U0, pa su lanci takvih polimera najmanje fleksibilni.
2. Polarne skupine rijetko se nalaze u lancu i među njima nema interakcije. Vrijednosti U0 i ∆U su male, a polimeri imaju visoku kinetičku i termodinamičku fleksibilnost.

-CF 2 -CF 2 -
Primjer: polikloropren
3. Polarne skupine raspoređene su tako da električna polja međusobno pomaknuti. U ovom slučaju ukupni dipolni moment makromolekule nula. Stoga su vrijednosti U0 i ∆U niske, a polimeri imaju visoku kinetičku i termodinamičku fleksibilnost.
Primjer: PTFE
Heterolančani polimeri
U heterolančanim polimerima moguća je rotacija oko C–O, C–N, Si–O i C–C veza. Vrijednosti U0 za ove veze su male i lanci imaju dovoljnu kinetičku fleksibilnost. Primjeri: poliesteri, poliamidi, poliuretani, silikonske gume.
Međutim, fleksibilnost heterolančanih polimera može biti ograničena međumolekularnim interakcijama zbog stvaranja H-veza (primjerice, u celulozi, poliamidima). Celuloza je jedan od krutih lančanih polimera. Sadrži veliki broj polarnih skupina (–OH) pa su za celulozu karakteristične intra- i međumolekularne interakcije te visoke vrijednosti U0 i niska fleksibilnost.
Molekularna težina polimera. Povećanje molekularne težine polimera povećava presavijanje lanca i stoga duge makromolekule
imaju veću kinetičku fleksibilnost u usporedbi s kratkim makromolekulama. Kako se MM povećava, povećava se broj konformacija koje makromolekula može usvojiti i povećava se fleksibilnost lanaca.
Prostorna gustoća mreže. Što je više kemijskih veza između makromolekula, manja je fleksibilnost lanca, tj. kako se gustoća prostorne mreže povećava, fleksibilnost se smanjuje. Primjer je smanjenje fleksibilnosti lanca s povećanjem broja poprečnih veza u rezol seriji.< резитол<резит.
Učinak veličine i broja supstituenata. Povećanje broja polarnih i velikih supstituenata smanjuje pokretljivost jedinica makromolekula i smanjuje kinetičku fleksibilnost. Primjer je smanjenje fleksibilnosti makromolekula butadien-stiren kopolimera s povećanjem sadržaja glomaznih fenilnih supstituenata u lancu.
Ako postoje dva supstituenta na jednom atomu ugljika u glavnom lancu polimera (na primjer, OCH3 i CH3 u PMMA jedinicama), tada makromolekula postaje kinetički kruta.
Temperatura. Kako temperatura raste, kinetička energija makromolekule raste. Sve dok je vrijednost kinetičke energije manja od U0, lanci izvode torzijske vibracije. Kada kinetička energija makromolekule postane jednaka ili premaši U0, karike se počinju okretati. S porastom temperature vrijednost U0 malo se mijenja, a povećava se brzina rotacije karika i povećava se kinetička fleksibilnost.
Kontrolna pitanja
1 Općenito o polimerima, pojmovi, definicije.
2 Definirajte i navedite primjere organskih, ne-
organski i organoelementni polimeri.
2 Klasifikacija homolančanih polimera, primjeri.
3 Klasifikacija heterolančanih polimera, primjeri.
4 Termodinamička i kinetička fleksibilnost makromolekula. Koji čimbenici utječu na fleksibilnost makromolekula?
5 Koja je konfiguracija makromolekula i koje su vrste konfiguracija makromolekula moguće? Primjeri.
6 Koja je konformacija makromolekula i koje vrste konformacija makromolekula su moguće? Primjeri.
7 Koji parametri karakteriziraju molekularnu težinu, raspodjela molekulske mase i polidisperznost polimera?
8 Molekulske karakteristike oligomera.
9 Frakcioniranje polimera i izrada molekularnih krivulja distribucija kularne mase.
· organski polimeri(u sastav ulaze organogeni elementi – C,N,O,P,S).Dijele se na homolančane (glavni lanac sadrži samo ugljikove atome) i heterolančane (glavni lanac uključuje i druge atome) Ovoj klasi polimera pripadaju biopolimeri.
· organoelementni polimeri(u sastavu glavnog lanca, uz atome ugljika, nalaze se atomi Si, Al, Ti, Ge, B).
· anorganski polimeri ( glavni lanac ne sadrži atome ugljika, kao što su silikoni).
1. Nabrojite vrste nomenklature polimera.
2. Kako nastaje nomenklatura na temelju naziva monomera?
3. Navedite primjere naziva polimera prema nomenklaturi na temelju kemijske strukture polimernog lanca.
4. Navedite vrste klasifikacije polimera. Navedite primjere.
5. Koje vrste kopolimera postoje?
6. Kako se provodi kemijska klasifikacija polimera?
Zadaci za samostalno rješavanje*
2. Klasifikacija i strukturne formule osnovnih polimera
2.1 Klasifikacija polimera
Pitanja 2501 - 2502, 2403 - 2406, 2307
2.2. Strukturne formule osnovnih polimera
Pitanja 3501, 3402, 3303 - 3309
*Ovdje i ubuduće zadaci su dani iz “Zbirke ispitnih zadataka za tematsku i završnu kontrolu iz discipline “Kemija i fizika polimera”, M., MITHT, 2009.
odjeljak 3. Glavne karakteristike makromolekula
Makromolekule karakteriziraju 4 glavna parametra:
1. Molekularna težina (MM), distribucija molekulske mase (MWD);
2. Konfiguracija makromolekule;
3. Konformacija makromolekule;
4. Topologija (linearna, razgranata).
MM vam omogućuje određivanje duljine, veličine makromolekula;
Konfiguracija određuje kemijsku strukturu makromolekula;
Konformacija određuje oblik makromolekula.
3.1. Molekularna težina (MW), distribucija molekulske težine (MWD)
Glavne razlike između koncepta MM za mornaricu i NMS:
MM je mjera molekulske duljine za linearne polimere i može se izraziti u smislu MM ponavljajućih jedinica spoja niske molekularne težine:
https://pandia.ru/text/78/135/images/image040_18.gif" width="12" height="2 src=">m0 je molekularna težina ponavljajuće jedinice spoja;
Pn - stupanj polimerizacije
Većina sintetskih polimera nisu pojedinačni spojevi, već se sastoje od mješavine molekula različitih veličina, ali istog sastava.
Ovo vodi do:
· za polimere, efektivna molekulska masa je prosječna vrijednost zbog polidisperznosti – rasprostranjenosti makromolekula u molekulskoj masi;
U većini polimera krajnje skupine razlikuju se od sastava karika polimernog lanca;
· određene bočne grane mogu postojati u makromolekulama, to također razlikuje makromolekule jedne od drugih;
Većina biopolimera su pojedinačni spojevi (svaki specifičan polimer je jedinstven u sastavu, strukturi i molekularnoj težini).
Razlozi polidisperznosti:
1. zbog statističke prirode procesa proizvodnje polimera: tijekom sinteze se dobivaju makromolekule različitih duljina;
2. zbog procesa djelomičnog razaranja makromolekula, na primjer, tijekom rada materijala;
3. zbog razlike u krajnjim skupinama molekule polimera;
4. zbog prisutnosti ogranaka u nekim polimerima na različitim mjestima i različite kemijske strukture.
3.1.1. Metode za određivanje prosjeka molekulskih masa
1) Usrednjavanje po broju molekula
Prosječan broj MM:
Mw=∑(NiMi2)/∑(NiMi) (3.1.1.2)
Masa ulomka danog Molekularna težina.
Mw se određuje kromatografijom, ultracentrifugiranjem, metodama raspršenja svjetlosti.
Kn=Mw/Mn (3.1.1.3)
Za monodisperzne (biološke) polimere Kn=1.
Uz usku distribuciju Kn=1,01÷1,05.
U industriji se najčešće dobivaju polimeri s Kn=3÷10.
3) MM srednjeg viskoziteta:
Mŋ=((∑NiMi)1+α/∑(NiMi))1/α, 0<α<1 (3.1.1.4)
![]()
3.1.2. Distribucija molekularne težine (MWD)
Najpotpunija karakteristika molekulskih masa polimera su funkcije raspodjele po molekulskim masama.
Dušik, bor, aluminij mogu biti elementi makromolekulskih lanaca u drugim komponentama strukture polimera, ili kao heteroatomi ulaziti u glavni lanac.

4.3. Ugljik
Ima veliku tendenciju stvaranja jakih kovalentnih veza, kako između vlastitih atoma tako i s drugim atomima.
https://pandia.ru/text/78/135/images/image064_12.gif" width="102" height="92"> - dvodimenzionalna struktura ugljik-ugljik grafena, grafita i čađe
Također je moguće dobiti linearni lanac ugljikovih atoma:
https://pandia.ru/text/78/135/images/image066_10.gif" width="238" height="14 src=">
Zagrijavanjem se pretvara u grafit.
Puno veće mogućnosti za izgradnju linearnih makromolekula od ugljikovih atoma otvaraju se kada su 1 ili 2 ugljikove valencije zasićene drugim atomima ili skupinama.
 - polietilen
- polietilen
 - polipropilen
- polipropilen
![]() - politetrafluoretilen
- politetrafluoretilen
Također, glavni lanac može sadržavati različite skupine koje sadrže heteroatome:
https://pandia.ru/text/78/135/images/image071_11.gif" width="93" height="43 src="> - grupiranje estera
https://pandia.ru/text/78/135/images/image073_9.gif" width="105" height="45 src="> - grupiranje karbamida (uree)
https://pandia.ru/text/78/135/images/image076_9.gif" width="185 height=84" height="84">
Ali oni nisu vrlo kemijski stabilni, a kada se oksidiraju, silicij se veže s kisikom, tvoreći vrlo jake veze silicij-kisik.
U prirodi se silicij javlja u obliku kvarca:

Ovo je kruta trodimenzionalna struktura koja ne pokazuje "polimerna" svojstva linearnih makromolekula. Linearne makromolekule se dobivaju zamjenom dviju valencija na svakom atomu silicija s organskim radikalima (CH3-, C2H5- itd.). U ovom slučaju pojavljuju se silicij-organski polimeri.
Moguće je sintetizirati polimere koji sadrže silicij:
 - polisiloksani
- polisiloksani
Atomi Al, B, Ti, Zn i neki drugi mogu biti ugrađeni u lanac.
4.5. Fosfor
Atomi fosfora mogu tvoriti polimere, ali glavni lanac mora uključivati i druge atome (najčešće kisik):
 - polifosfati
- polifosfati
 - polifosforna kiselina
- polifosforna kiselina
Ostaci fosforne kiseline uključeni su u prirodne polimere ( nukleinske kiseline, DNK i RNK):

Dakle, dva ili polivalentna atoma (C, O, P, N, S, Si, Al, B i neki drugi) mogu biti u obliku elemenata glavnog lanca makromolekula ili biti u bočnim fragmentima; jednovalentni atomi (H, F, Cl, J, Br i neki drugi) mogu se poredati samo kao supstituenti.
![]()
Kemija polimera temelji se na ovim elementima.
4.6. Vrste polimera
Polimeri se dobivaju ili sintetski, ili ekstrahiranim iz živih organizama (biopolimeri), ili preradom već izoliranih prirodnih polimera.
Neki sintetski stvoreni polimeri postoje u prirodi. Polimeri se dobivaju iz monomera - tvari niske molekulske mase ili kao rezultat transformacija gotovih polimera (sintetskih ili prirodnih) - polimer-analogne transformacije.

1,4-cis-polibutadien ne postoji u prirodi, dobiva se sintetski iz butadiena.

1,4-cis-poliizopren postoji u prirodi (prirodni kaučuk), ali se u prirodi sintetizira iz glukoze i drugih tvari (ali ne iz izoprena, kao u industriji)

Ovaj poliester se može dobiti kondenzacijom poli-β-hidroksibutirata, a istovremeno ga sintetiziraju brojne bakterije.
Sinteze biopolimera neće se razmatrati u ovom kolegiju.
Mnoge prirodne polimere vrlo je teško dobiti sintetičkim putem. Dobivaju se u živim organizmima kao rezultat složenih biokemijskih reakcija.
Najvažniji prirodni polimeri:
Primjeri su reakcije poliesterifikacija:
HO-R-COOH + HO-R-COOH > HO-R-COO-R-COOH + H2O itd.
poliamidiranje:
H2N-R-NH2 + ClOC-R"-COCl > H2N-R-NHCO-R"-COCl + HCl, itd.
U ovom slučaju, za razliku od polimerizacije, elementarni sastav proizvoda polikondenzacije u ovom slučaju ne podudara se sa sastavom monomernih spojeva, budući da je svaki kemijski čin polikondenzacije popraćen oslobađanjem molekule proizvoda niske molekularne težine.
Iznad opća shema Polikondenzacija također odgovara nekim vrstama procesa koji nisu popraćeni oslobađanjem proizvoda niske molekularne težine. To uključuje, na primjer, sintezu poliuretana iz glikola i diizocijanata:
HO-R-OH + O=C=N-R "-N=C=O > HO-R-O-CO-NH-R"-N=C=O itd.
Takvi procesi polikondenzacije često se nazivaju poliadicija. Prema kinetičkim zakonitostima reakcije poliadicije vrlo su slične reakcijama polikondenzacije. U oba tipa polikondenzacijskih procesa rast makromolekula odvija se međudjelovanjem funkcionalnih skupina monomernih molekula ili istih skupina smještenih na krajevima već formiranih lanaca različite molekulske mase. Intermedijarni polimerni produkti dobiveni kao rezultat ovih reakcija prilično su stabilni i mogu se izolirati u slobodnom obliku. Međutim, oni sadrže reaktivne skupine na svojim krajevima i stoga su sposobni za daljnje kondenzacijske reakcije, kako međusobno tako i s odgovarajućim monomernim molekulama. Iz toga slijedi da se, teoretski, polikondenzacija može smatrati potpunom tek kada su sve terminalne funkcionalne skupine reagirale, uslijed čega bi trebala nastati jedna divovska ciklička makromolekula. U praksi se to, međutim, nikada ne postiže.
Pitanja za samostalno učenje:
1. Koji su elementi Periodni sustav sposobni formirati polimerne lance?
2. Navedite primjere polimera dobivenih sintetskim putem.
3. Navedite primjere prirodnih polimera.
Konformacija, veličina i oblik makromolekula
Dimenzije makromolekule određene su njezinom duljinom I i promjerom d. Ako je makromolekula predstavljena u obliku izduženog lanca određene konfiguracije, izračunajte l I d nije teško. Na primjer, za poliizobutilen (PIB), promjer i duljina monomerne jedinice su 0,5 odnosno 0,154 nm. Ako je broj takvih veza 10 4 , tada će makromolekula PIB-a imati duljinu od 0,154-10 4 nm, a omjer duljine i promjera bit će 3100. odbijanje) atoma i njihovih skupina, posebno bočnih, i utjecaj toplinskog gibanja, koji postoji na bilo kojoj temperaturi osim apsolutne nule.
Riža. Sl. 18. Ovisnost potencijalne energije U(u) molekule etana (a) i molekule dikloroetana (b) o kutu zakreta u metilne skupine (c - cis-konformacija, r - trans-konformacija, r - gauche konformacija)
Uzimajući u obzir te čimbenike, u svakom određenom trenutku vremena makromolekule preuzimaju određene konformacije. Svaku konformaciju karakterizira samo svoj specifični raspored u prostoru atoma i skupina. Prijelaz iz jedne konformacije u drugu provodi se rotacijom, rotacijom ili oscilacijom oko jednostrukih veza pod djelovanjem toplinskog gibanja ili vanjskih sila i nije popraćen kidanjem valentnih kemijskih veza.
Konformacijske promjene također se događaju u malim molekulama organski spojevi. Kao primjer, razmotrimo molekulu etana CH3-CH3. Titranje skupine atoma oko C-C veze frekvencijom ?10 10 s -1 prati promjena potencijalne energije molekule koja se opisuje sinusoidnom krivuljom. Konformacije koje odgovaraju minimalnoj energiji su stabilne, tzv konformatori ili konformacijski izomeri. Ostatak konformacija su energetska stanja kroz koja molekula mora proći kada se kreće iz jedne stabilne konformacije u drugu. Molekula etana može postojati u dva položaja: cis I trans:

Ovi položaji su energetski neravnopravni: u cis- obliku, odbojne sile će biti jače, dakle trans oblik je energetski povoljniji i odgovara minimumu energije (sl. 1.8). Prijelaz iz jednog oblika u drugi, na primjer iz cis- V trans-, nastaje zbog rotacije skupine CH 3 pod kutom od 60 °. Pri tome se potencijalna energija mijenja od U c do U t. Pri sljedećem prijelazu trans- CH 3 skupina mora prijeći u cis-formu za još 60°, pri čemu je potrebno svladati potencijalnu barijeru rotacije zbog akumulirane kinetičke energije ( k T). Rotacija skupina u takvim molekulama je praktički slobodna, tj. nesputana (kT>Uo) Kako struktura postaje složenija, rotacija grupa oko veza postaje sve usporenija, budući da se vrijednost potencijalne barijere rotaciji mijenja. Dakle, u molekuli dikloroetana CH 2 C1 - CH 2 Cl, sloboda rotacije i time postojanje određenih konformacija ograničava atom klora. Trans-oblik je energetski najpovoljniji, a cis-oblik je nestabilan zbog manifestacije odbojnih sila. Da bi se izravnale odbojne sile, Cl se zakreće za kut od 120°, tvoreći takozvani "kosi" gauche oblik (lijevo +120°, desno -120°):

Ovi gosh oblici su manje stabilni od trans-(U G > U T ) , ali stabilniji u usporedbi s cis-formom (U G kT veća od potencijalne rotacijske barijere Uo. Ako se to ne poštuje, tada grupe samo osciliraju oko pozicija s minimalnom energijom. Za većinu organskih spojeva vrijednost potencijalne barijere U 0 u plinovitoj fazi je 4--19 kJ / mol:

U 0 ovisi o vrsti supstituenta i njegovoj polarnosti: s povećanjem volumena supstituenata ili njihovog polariteta (na primjer, pri zamjeni CH 3 s C1 ili F), vrijednost U Q diže se. Atomi kisika, sumpora, dušika, kao i dvostruke veze smanjuju ovu vrijednost.
Razmotrimo kako se mijenja konformacija makromolekule. Moguće je uvjetno predstaviti polimer u obliku molekule etana CH 3 -CH 3, u kojoj su atomi vodika zamijenjeni radikalima R i R ", koji su veze makromolekule. Na primjer, makromolekula polipropilena može biti predstavljen kao

Veze se mogu okretati oko veza samo ako vezni kutovi nisu fiksni i nema utjecaja supstituenata glavnog lanca. Karike takvog lanca mogu poprimiti bilo koju konformaciju. U stvarnosti, takvi lanci ne postoje, oni se uvjetno nazivaju slobodno artikuliran. U pravim makromolekulama vezni kutovi su strogo fiksni, pa je stoga broj konformacija ograničen. Osim toga, vjerojatnost postojanja pojedinih konformera, kao i za jednostavne kemijske spojeve, bit će određena omjerom sila privlačenja i odbijanja, odnosno unutarmolekulskim i međumolekularnim međudjelovanjem. Ova interakcija za polimere, kao što smo već rekli, može biti kratkog dometa (na primjer, između susjednih atoma i skupina) i dugog dometa (između skupina koje se nalaze na znatnoj udaljenosti). Mnogo veći utjecaj ima interakcija reda kratkog dometa.
Prijelaz iz jedne konformacije u drugu, kao i kod spojeva niske molekulske mase, određen je omjerom potencijalne barijere rotaciji i kinetičke energije molekule. Postojanje međudjelovanja kratkog i dugog dometa nameće tako značajna ograničenja na rotaciju veza oko jednostrukih veza da ona postaje usporena i rotira samo za određeni kut F, čija je vrijednost određena kemijskom strukturom i konfiguracijom makromolekule, moguće su.
Konformacija jedinice Ponavljajuće jedinice većine polimera obično su mješavina rotacijskih izomera. Dakle, za vinilne polimere CH 2 -CHX karakteristično je postojanje tri rotacijska izomera: trans i dva Bože(lijevo i desno).
Konformacijski poredak kratkog dometa očituje se u formiranju različitih konformacija kada su jedinice vezane jedna za drugu. Za vinil i viniliden polimere, susjedne jedinice mogu postojati u trans- i gauche konformacije (a-- ponavljajuća veza):

Za polimere diena (polikloropren, polibutadien), isto trans- i gauche konformacije u odnosu na CH 2 --CH 2 skupine.
Konformacijski red kratkog dometa također osigurava konformacijski skup u malim nizovima, na primjer, dijade, trijade itd. Udaljenost između skupina koje su jednako udaljene naziva se razdoblje identiteta. Promjena skupa konformera povlači za sobom promjenu perioda identiteta. Ispod su podaci o razdoblju identiteta (tip konformacije i vrijednost perioda) za vinilne polimere ( T --trans, G l i G PR -- Bože- lijevo i desno; znamenke - broj ponavljajućih konformera):

Konformacijski poredak velikog dometa osigurava određenu pravilnu ili nepravilnu kombinaciju malih sekvenci konformera tijekom dovoljno dugačke duljine lanca. Na formiranje konformacijskog reda velikog dometa značajno utječu položaj i volumen supstituenata u lancu. Razmotrimo, kao primjer, vinilne polimere, čiji je najjednostavniji predstavnik polietilen. Minimalna slobodna energija za ovaj polimer postiže se u jednoj od tri konformacije (trans-, bože-lijevo, bože-desno), što bi trebalo odgovarati maksimalnoj udaljenosti između dovoljno voluminoznih CH 2 skupina. Ovaj uvjet je zadovoljen kada makromolekula formira cik-cak uzorak na dovoljno velikoj udaljenosti. trans- konformacija (slika 1.9). U polipropilenu je vodikov atom zamijenjen CH3 skupinom, koja ima veći volumen. Supstituenti su obično raspoređeni tako da se njihovi elektronski oblaci ne preklapaju i time ne uzrokuju pojavu odbojnih sila.
Da bi se zadovoljio ovaj uvjet, makromolekula izotaktičkog polipropilena formira spiralnu konformaciju umjesto ravnog cik-cak, u kojem postoji jedan zavoj na tri monomerne jedinice, a CH3 grupe su rotirane jedna u odnosu na drugu za 120°. Za sindiotaktički polipropilen, odbojne sile koje stvaraju CH 3 skupine praktički se ne pojavljuju, pa je za njega očuvana ravna cik-cak konformacija (vidi sliku 1.9).

Riža. 1.9 Shematski prikaz planarne trans konformacije polietilenskog lanca (a) do raznih spiralnih konformacija u izotaktičkim loliolefinima (b) s različitim supstituentima R (svijetli kružići)
Stupanj uvijenosti ili uvijanja spirale procjenjuje se klasom spirale x na , Gdje x- broj poveznica, na-- broj zavoja Ove vrijednosti određene su prirodom supstituenta i njegovim položajem. Dakle, ako za polipropilen postoje tri ponavljajuće veze po zavoju, onda za politetrafluoretilen postoji pet zavoja za svakih osam ponavljajućih veza.
Konformacija makromolekule (lanca) je dimenzija i specifični oblik koje makromolekula poprima kao rezultat ukupnog utjecaja toplinskog gibanja i vanjskih sila. (Treba napomenuti da toplinsko gibanje dovodi do usrednjavanja konformacija, a kada govorimo o jednoj ili drugoj konformaciji, mislimo na prosječnu konformaciju.) Ovisno o omjeru tih sila i intenzitetu toplinskog gibanja, mogu se ostvariti različite konformacije (Slika 1.10):
- - statistički svitak, tj. više ili manje naborana konformacija; takvu konformaciju obično poprimaju makromolekule polimera, kod kojih intenzitet unutarnjeg toplinskog gibanja prevladava nad vanjskim utjecajima; karakteristična je za mnoge polimere, na primjer, linearne (polietilen, polipropilen, polibutadien, poliizopren, trinitroceluloza itd.), ljestve (polifeilensiloksan);
- - konformacija spirale; ovu konformaciju obično usvajaju makromolekule u kojima je dugotrajni konformacijski poredak u obliku spirale imobiliziran, na primjer, vodikovim vezama; spiralna konformacija tipična je, u pravilu, za proteine i nukleinske kiseline;
- - konformacija globule, tj. vrlo kompaktne čestice bliske sferičnom obliku; takvu konformaciju imaju makromolekule polimera s vrlo jakim unutarmolekulskim međudjelovanjima, npr. polimeri koji sadrže atome fluora (politetrafluoretilen);
- - konformacija šipke ili žice (pronađena za neke alkil poliizocijanate); konformacija molekule
- - sklopljena konformacija; karakteristika polimera u kristalnom stanju;
- - konformacija koljenastog vratila (na primjer, poli-n-benzamid).
Dakle, konformacija makromolekule je zbroj najnižih konformacijskih razina. Na primjer, konformacija polipropilenske makromolekule može se okarakterizirati na sljedeći način: konformacija veze -- trans I Bože konformacijski poredak kratkog dometa trans I Bože udaljena -- spirala 3 1 ; konformacija makromolekule je statistička zavojnica u amorfnom stanju i presavijena u kristalnom stanju.

Riža. 1.10
c - statistički klupko; b - spirala (O - supstituenti, između kojih se stvaraju vodikove veze); a je globula; g - niz; d - presavijeni; e - koljenasto vratilo
Treba napomenuti da se konformacija makromolekule može mijenjati ovisno o vanjskim čimbenicima - temperaturi, naprezanju itd. U tom slučaju zahvaćene su sve konformacijske razine: na primjer, tijekom vlačne deformacije u makromolekuli polibutadiena, konformacijski poredak kratkog dometa može se mijenjati ovisno o vanjskim čimbenicima. promjene (gauche oblici postaju trans-) i konformacija molekule -- statistička zavojnica prelazi u konformaciju koja se približava izduženom nizu. Stoga se konformacija makromolekule obično procjenjuje u odsutnosti ometajućih čimbenika. Idealni uvjeti su plinovita faza, no budući da makromolekule polimera ne postoje u plinovitom stanju, najrealniji model tog stanja je razrijeđena otopina u tzv. 0-otapalu na 0-temperaturi, kada nema interakcije između polimer i otapalo i lančane makromolekule imaju neporemećene dimenzije.
Za sve konformacije koje makromolekula poprima, karakteristika je njezine duljine l je udaljenost između krajeva r. Teorijski proračun dimenzija lanca proveden je za slobodno artikulirani lanac, tj. lanac koji nema kruto fiksne vezne kutove i moguća je slobodna rotacija atoma i skupina oko jednostrukih veza (slika 1.11). Ako je molekula potpuno razmotana, tada je r= l, tj. duljina molekule, izračunata iz duljine ponavljajuće jedinice b i broja tih jedinica P, osim toga, izračun uzima u obzir duljinu veza, vrijednosti kutova veze i konfiguraciju veze. Ova vrijednost ja nazvao kontura ili duljina hidrodinamičkog lanca. Za maksimalno savijenu molekulu r>0 za sve međupozicije 0
Budući da je makromolekula u pokretu, zauzimajući u svakom trenutku ja th konformacije, tada je vrijednost r prosječna karakteristika i smatra se vektorom povučenim s jednog kraja lanca na drugi. Prosječna vrijednost r za sve konformacije je nula, jer su svi smjerovi jednako vjerojatni. Stoga je udaljenost između krajeva lanca karakterizirana ili srednjim kvadratom udaljenosti r 2, ili korijenom srednje kvadratne udaljenosti

Gdje W(r)-- termodinamička vjerojatnost postojanja lanca; n je broj veza koje se ponavljaju; b je duljina takve veze; r St - razmak između krajeva slobodno zglobnog lanca.
Analiza ovog izraza pokazuje da za r>0 i r>? W(r)>0, tj. ova stanja su malo vjerojatna. Maksimalna vrijednost W(r) max,oni. najvjerojatniji razmak između krajeva lanca, može se izračunati iz uvjeta za određivanje maksimuma, tj.
Gdje l sv - duljina veze; n=M/M EV (M i M EV -- molekularne težine polimera i jedinice); c je kut komplementaran valentnom kutu.
Stupanj savijanja makromolekule procjenjuje se omjerom 1/(r 2) 1/2, tj. ovisi i o molekulskoj masi polimera.
Udaljenost između krajeva makromolekule također se može procijeniti iz postojana duljina makromolekule. Ako je makromolekula predstavljena kao kontinuirani crvoliki lanac s kontinuiranom zakrivljenošću (vidi sliku 1.11, c), tada je a projekcija vektora udaljenosti između krajeva zavojnice na smjer tangente na početak zavojnice. zavojnica - i je trajna duljina lanca.
Veličinu molekule karakterizira i prosječni radijus vrtnje, odnosno polumjer rotacije R 2 . Za Gaussove zavojnice
Pravi lanac se može smatrati slobodno artikuliranim ako su dijelovi uvjetno odvojeni od dugog lanca, čije će konformacije biti neovisne jedna o drugoj, a utjecaj intramolekularne interakcije će se očitovati unutar ovog odjeljka. Takav dio lanca duljine A, čiji položaj ne ovisi o položaju susjednih dijelova, naziva se termodinamički segment ili Kuhnov segment. Za stvarne lance gornje ovisnosti vrijede ako umjesto duljine ponavljajuće veze b koristimo duljinu segmenta A, a umjesto broja karika n - broj segmenata Z. Tada

(gdje je r 2 kvadrat prosječne udaljenosti između krajeva realnog lanca). U točki maksimuma (tj. najvjerojatnije) veličina zavojnice je:
- (gdje je q prosječni kut unutar kojeg je dopuštena rotacija). Kada je cosc= 0 (uvjet slobodne rotacije) formula
- (1.23) ulazi u (1.20), a kada je cosc=l r 2 >?, tj. e. vjerojatna konformacija produženog lanca. Za sve slučajeve inhibirane rotacije (0
gdje je U 0 (c) potencijalna prepreka rotaciji; k je Boltzmannova konstanta.
Osim pokazatelja koji karakterizira udaljenost između krajeva makromolekule, odnosno duljinu, pojam veličine, kao što smo već rekli, uključuje i promjer makromolekule. d je promjer cilindra opisanog oko molekule. Određuje se uzimajući u obzir bočne skupine, grane i druge karakteristike konfiguracije (Sl. 1.13). Baš kao i dužina d je prosječna karakteristika, jer se oblik makromolekule mijenja zbog mikro-Brownovog gibanja. Volumen koji zauzima jedna makromolekula je takozvana koordinacijska sfera koja okružuje zavojnicu. Koncentracija polimera ovisi o vrsti konformacija: niska je u nasumičnim svicima i iznosi ~3% u 0-otapalu. Što je jača interakcija unutar zavojnice, to je veća njegova gustoća i manja sfera, odnosno volumen, stoga je koncentracija polimera veća u globularnoj konformaciji u odnosu na konformaciju nasumične zavojnice.

Slika 1.13 Metode određivanja promjera makromolekula d(R -- supstituenti)
Ako je makromolekula u uvjetima interakcije dugog dometa (na primjer, u interakciji s otapalom), tada se njezine dimenzije određuju uzimajući u obzir te sile. U ovom slučaju dimenzije ovise o parametru bubrenja b:
(gdje je r e udaljenost između krajeva lanca u otapalu). Kako se termodinamički afinitet polimera i otapala povećava, veličina zavojnice se povećava, koncentracija polimera u zavojnici opada i, pri bliskim vrijednostima parametara topljivosti, iznosi oko 1%.
Dimenzije makromolekule također ovise o takozvanom V zahtjevu isključenog volumena. To je volumen iz kojeg određena molekula polimera isključuje sve ostale molekule, što je rezultat odbojnih sila među njima. Između V zahtjeva i b postoji odnos:

(gdje je x konstanta u rasponu od 1 do 6,67; A je konstanta).
Razgranate molekule karakteriziraju manje veličine zavojnica zbog njihove veće gustoće:
Dakle, konformacije i veličine stvarnih makromolekula određene su kombinacijom sila reda kratkog i dugog dometa, intenzitetom unutarnjeg toplinskog gibanja te ovise o kemijskoj strukturi, molekularnoj težini i konfiguraciji makromolekule. Sasvim je prirodno pretpostaviti da će se u kondenziranom stanju, kada se zbog visokog kooperativnog sustava uvelike povećava uloga djelovanja dugog dometa, konformacije makromolekula razlikovati od onih izolirane makromolekule.