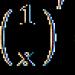Pitanje 1. Koje procese znanstvenici proučavaju na molekularnoj razini?
Na molekularnoj razini proučavaju se najvažniji procesi života organizma: njegov rast i razvoj, metabolizam i pretvorba energije, pohranjivanje i prijenos nasljednih informacija, varijabilnost. Elementarna jedinica na molekularnoj razini je gen - fragment molekule nukleinske kiseline u kojem je zabilježena određena količina biološke informacije u kvalitativnom i kvantitativnom smislu.
Pitanje 2. Koji elementi prevladavaju u sastavu živih organizama?
Živi organizam sadrži više od 70-80 kemijskih elemenata, ali prevladavaju ugljik, kisik, vodik, dušik i fosfor.
Pitanje 3. Zašto se molekule proteina, nukleinskih kiselina, ugljikohidrata i lipida smatraju biopolimerima samo u stanici?
Molekule proteina, nukleinskih kiselina, ugljikohidrata i lipida su polimeri jer se sastoje od ponavljajućih monomera. Ali samo u živom sustavu (stanici, organizmu) te tvari manifestiraju svoje biološki entitet, posjedujući niz specifičnih svojstava i obavljajući mnoge važne funkcije. Stoga se u živim sustavima takve tvari nazivaju biopolimeri. Izvan živog sustava te tvari gube svoja biološka svojstva i nisu biopolimeri.
Pitanje 4. Što se podrazumijeva pod univerzalnošću biopolimernih molekula?
Bez obzira na razinu složenosti i funkcije koje obavljaju u stanici, svi biopolimeri imaju sljedeće značajke:
njihove molekule imaju nekoliko dugih grana, ali mnogo kratkih;
polimerni lanci su jaki i ne raspadaju se spontano;
sposoban za nošenje različitih funkcionalnih skupina i molekularnih fragmenata koji osiguravaju biokemijsku funkcionalnu aktivnost, tj. sposobnost provođenja biokemijskih reakcija i transformacija potrebnih za stanicu u okruženju unutarstanične otopine;
imaju dovoljnu fleksibilnost za formiranje vrlo složenih prostornih struktura potrebnih za obavljanje biokemijskih funkcija, tj. za rad proteina kao molekularnih strojeva, nukleinskih kiselina kao programskih molekula, itd.;
S-N veze I C-C biopolimeri, unatoč svojoj snazi, također su baterije elektroničke energije.
Glavno svojstvo biopolimera je linearnost polimernih lanaca, budući da se samo linearne strukture lako kodiraju i "sastavljaju" iz monomera. Osim toga, ako je polimerna nit savitljiva, od nje je vrlo lako oblikovati željenu prostornu strukturu, a nakon što se ovako konstruiran molekularni stroj amortizira i polomi, može se lako rastaviti na sastavne elemente kako bi se ponovno ih upotrijebite. Kombinacija ovih svojstava nalazi se samo u polimerima na bazi ugljika. Svi biopolimeri u živim sustavima sposobni su ispuniti određena svojstva i obavljati mnoge važne funkcije. Svojstva biopolimera ovise o broju, sastavu i redoslijedu njihovih sastavnih monomera. Sposobnost mijenjanja sastava i slijeda monomera u polimernoj strukturi omogućuje postojanje velike raznolikosti biopolimernih opcija, bez obzira na vrstu organizma. U svim živim organizmima biopolimeri su izgrađeni prema jednom planu.
Trenutna stranica: 2 (knjiga ima ukupno 16 stranica) [dostupan odlomak za čitanje: 11 stranica]
Biologija– Znanost o životu jedna je od najstarijih znanosti. Čovjek je prikupljao znanje o živim organizmima tisućama godina. Akumulacijom znanja biologija se diferencirala u samostalne znanosti (botaniku, zoologiju, mikrobiologiju, genetiku itd.). Sve više raste važnost graničnih disciplina koje povezuju biologiju s drugim znanostima - fizikom, kemijom, matematikom itd. Kao rezultat integracije nastale su biofizika, biokemija, svemirska biologija itd.
Trenutno je biologija složena znanost, nastala kao rezultat diferencijacije i integracije različitih disciplina.
U biologiji se koriste različite metode istraživanja: promatranje, eksperiment, usporedba itd.
Biologija proučava žive organizme. Otvoreni su biološki sustavi dobivanje energije i hranjivih tvari iz okoline. Živi organizmi reagiraju na vanjske utjecaje, sadrže sve podatke potrebne za razvoj i razmnožavanje te su prilagođeni određenom staništu.
Svi živi sustavi, bez obzira na stupanj organizacije, imaju zajedničke značajke, a sami sustavi su u neprekidnoj interakciji. Znanstvenici razlikuju sljedeće razine organizacije žive prirode: molekularnu, staničnu, organizmsku, populacijsko-vrstnu, ekosustavnu i biosfernu.
Poglavlje 1. Molekularna razina
Molekularnu razinu možemo nazvati početnom, najdubljom razinom organizacije živih bića. Svaki živi organizam sastoji se od molekula organskih tvari - bjelančevina, nukleinskih kiselina, ugljikohidrata, masti (lipida), koje se nazivaju biološkim molekulama. Biolozi proučavaju ulogu ovih esencijalnih bioloških spojeva u rastu i razvoju organizama, pohranjivanju i prijenosu nasljednih informacija, metabolizmu i pretvorbi energije u živim stanicama i drugim procesima.
U ovom ćete poglavlju naučiti
Što su biopolimeri;
Kakvu strukturu imaju biomolekule?
Koje funkcije obavljaju biomolekule?
Što su virusi i koje su njihove značajke?
§ 4. Molekularna razina: opće karakteristike
1. Što je kemijski element?
2. Što se naziva atom i molekula?
3. Što organska tvar znaš li?
Svaki živi sustav, koliko god složeno organiziran bio, očituje se na razini funkcioniranja bioloških makromolekula.
Proučavajući žive organizme naučili ste da su sastavljeni od istih kemijskih elemenata kao i neživi organizmi. Trenutno je poznato više od 100 elemenata, većina ih se nalazi u živim organizmima. Najzastupljeniji elementi u živoj prirodi su ugljik, kisik, vodik i dušik. Upravo ti elementi tvore molekule (spojeve) tzv organska tvar.
Osnova svega organski spojevi ugljik služi. Može doći u dodir s mnogim atomima i njihovim skupinama, tvoreći lance koji se razlikuju po kemijski sastav, struktura, duljina i oblik. Molekule se formiraju iz skupina atoma, a iz potonjih - više složene molekule, razlikuju se u strukturi i funkcijama. Ti organski spojevi koji čine stanice živih organizama nazivaju se biološki polimeri ili biopolimeri.
Polimer(od grčkog politike- brojni) - lanac koji se sastoji od brojnih karika - monomeri, od kojih je svaki relativno jednostavan. Molekula polimera može se sastojati od više tisuća međusobno povezanih monomera, koji mogu biti isti ili različiti (slika 4).
Riža. 4. Shema strukture monomera i polimera
Svojstva biopolimera ovise o strukturi njihovih molekula: o broju i raznolikosti monomernih jedinica koje tvore polimer. Svi su oni univerzalni, jer su izgrađeni prema istom planu za sve žive organizme, bez obzira na vrstu.
Svaki tip biopolimera karakterizira specifična struktura i funkcija. Da, molekule bjelančevine Oni su glavni strukturni elementi stanica i reguliraju procese koji se u njima odvijaju. Nukleinske kiseline sudjeluju u prijenosu genetske (nasljedne) informacije od stanice do stanice, od organizma do organizma. Ugljikohidrati I masti Oni su najvažniji izvori energije potrebne za život organizama.
Na molekularnoj razini događa se transformacija svih vrsta energije i metabolizma u stanici. Mehanizmi ovih procesa također su univerzalni za sve žive organizme.
Istodobno se pokazalo da su raznolika svojstva biopolimera od kojih se sastoje svi organizmi posljedica različitih kombinacija samo nekoliko vrsta monomera, tvoreći mnoge varijante dugih polimernih lanaca. Ovo načelo leži u osnovi raznolikosti života na našem planetu.
Specifična svojstva biopolimera pojavljuju se samo u živoj stanici. Jednom izolirane iz stanica, molekule biopolimera gube svoju biološku bit i karakterizirane su samo fizikalno-kemijskim svojstvima klase spojeva kojoj pripadaju.
Samo proučavanjem molekularne razine može se razumjeti kako su se odvijali procesi nastanka i evolucije života na našem planetu, koje su molekularne osnove nasljeđa i metabolički procesi u živom organizmu.
Kontinuitet između molekularne razine i sljedeće stanične razine osiguran je činjenicom da su biološke molekule materijal od kojeg nastaju supramolekularne – stanične strukture.
Organske tvari: bjelančevine, nukleinske kiseline, ugljikohidrati, masti (lipidi). Biopolimeri. Monomeri
Pitanja
1. Koje procese znanstvenici proučavaju na molekularnoj razini?
2. Koji elementi prevladavaju u sastavu živih organizama?
3. Zašto se molekule proteina, nukleinskih kiselina, ugljikohidrata i lipida smatraju biopolimerima samo u stanici?
4. Što se podrazumijeva pod univerzalnošću molekula biopolimera?
5. Kako se postiže raznolikost svojstava biopolimera koji izgrađuju žive organizme?
Zadaci
Koji se biološki obrasci mogu formulirati na temelju analize teksta odlomka? Raspravite o njima s članovima razreda.
§ 5. Ugljikohidrati
1. Koje tvari vezane uz ugljikohidrate poznajete?
2. Kakvu ulogu imaju ugljikohidrati u živom organizmu?
3. Kao rezultat kojeg procesa nastaju ugljikohidrati u stanicama zelenih biljaka?
Ugljikohidrati, ili saharidi, jedna je od glavnih skupina organskih spojeva. Oni su dio stanica svih živih organizama.
Ugljikohidrati se sastoje od ugljika, vodika i kisika. Naziv "ugljikohidrati" dobili su jer većina njih ima isti omjer vodika i kisika u molekuli kao iu molekuli vode. Opća formula ugljikohidrata je C n (H 2 0) m.
Svi ugljikohidrati se dijele na jednostavne, odn monosaharidima, i složeni, odn polisaharidi(slika 5). Od monosaharida najveća vrijednost jer živi organizmi imaju riboza, deoksiriboza, glukoza, fruktoza, galaktoza.

Riža. 5. Građa molekula jednostavnih i složenih ugljikohidrata
Di- I polisaharidi nastaju spajanjem dviju ili više molekula monosaharida. Tako, saharoza(šećerna trska), maltoza(sladni šećer), laktoza(mliječni šećer) – disaharidi, nastao kao rezultat spajanja dviju molekula monosaharida. Disaharidi su po svojstvima slični monosaharidima. Na primjer, oba horonija su topiva u vodi i imaju sladak okus.
Polisaharidi se sastoje od veliki broj monosaharidima. To uključuje škrob, glikogen, celuloza, hitin itd. (slika 6). S povećanjem broja monomera smanjuje se topljivost polisaharida i nestaje slatki okus.
Glavna funkcija ugljikohidrata je energije. Tijekom razgradnje i oksidacije molekula ugljikohidrata oslobađa se energija (uz razgradnju 1 g ugljikohidrata - 17,6 kJ) koja osigurava vitalne funkcije organizma. Kada postoji višak ugljikohidrata, oni se nakupljaju u stanici kao rezervne tvari (škrob, glikogen) i po potrebi ih tijelo koristi kao izvor energije. Pojačana razgradnja ugljikohidrata u stanicama može se uočiti, na primjer, tijekom klijanja sjemena, intenzivnog rada mišića i produljenog posta.
Ugljikohidrati se također koriste kao gradevinski materijal. Stoga je celuloza važna strukturna komponenta staničnih stijenki mnogih jednostaničnih organizama, gljiva i biljaka. Zbog svoje posebne strukture, celuloza je netopljiva u vodi i ima veliku čvrstoću. U prosjeku 20-40% materijala u stjenkama biljnih stanica je celuloza, a pamučna vlakna su gotovo čista celuloza, zbog čega se koriste za izradu tekstila.

Riža. 6. Shema strukture polisaharida
Hitin je dio staničnih stijenki nekih protozoa i gljiva; također se nalazi u određenim skupinama životinja, kao što su člankonošci, kao važna komponenta njihovog egzoskeleta.
Poznati su i složeni polisaharidi koji se sastoje od dvije vrste jednostavnih šećera, koji se redovito izmjenjuju u dugim lancima. Takvi polisaharidi obavljaju strukturne funkcije u potpornim tkivima životinja. Dio su međustanične tvari kože, tetiva i hrskavice, dajući im čvrstoću i elastičnost.
Neki su polisaharidi dio staničnih membrana i služe kao receptori, omogućujući stanicama međusobno prepoznavanje i interakciju.
Ugljikohidrati, odnosno saharidi. Monosaharidi. Disaharidi. polisaharidi. Riboza. Dezoksiriboza. Glukoza. Fruktoza. galaktoza. Saharoza. Maltoza. Laktoza. Škrob. Glikogen. hitin
Pitanja
1. Kakav sastav i strukturu imaju molekule ugljikohidrata?
2. Koji se ugljikohidrati nazivaju mono-, di- i polisaharidi?
3. Koje funkcije ugljikohidrati obavljaju u živim organizmima?
Zadaci
Analizirajte sliku 6 “Dijagram strukture polisaharida” i tekst odlomka. Koje pretpostavke možete napraviti na temelju usporedbe strukturnih značajki molekula i funkcija koje obavljaju škrob, glikogen i celuloza u živom organizmu? Raspravite o ovom problemu sa svojim kolegama iz razreda.
§ 6. Lipidi
1. Koje tvari slične mastima poznajete?
2. Koje su namirnice bogate mastima?
3. Koja je uloga masti u organizmu?
Lipidi(od grčkog lipos-mast) velika je skupina tvari sličnih mastima koje su netopljive u vodi. Većina lipida sastoji se od masnih kiselina visoke molekularne težine i trohidričnog alkohola glicerola (slika 7).
Lipidi su prisutni u svim stanicama bez iznimke, obavljajući specifične biološke funkcije.
masti- najjednostavniji i najrašireniji lipidi - imaju važnu ulogu kao izvor energije. Kada se oksidiraju, daju više nego dvostruko više energije od ugljikohidrata (38,9 kJ pri razgradnji 1 g masti).

Riža. 7. Struktura molekule triglicerida
Masti su glavni oblik skladištenje lipida u kavezu. Kod kralježnjaka, otprilike polovica energije koju stanice troše u mirovanju dolazi od oksidacije masti. Masti se također mogu koristiti kao izvor vode (oksidacijom 1 g masti nastaje više od 1 g vode). Ovo je posebno vrijedno za arktičke i pustinjske životinje koje žive u uvjetima nedostatka slobodne vode.
Zbog niske toplinske vodljivosti lipidi obavljaju zaštitne funkcije, tj. služe za toplinsku izolaciju organizama. Na primjer, mnogi kralješnjaci imaju dobro definiran sloj potkožnog masnog tkiva, što im omogućuje život u hladnim klimatskim uvjetima, a kod kitova ima još jednu ulogu - potiče plutanje.
Lipidi obavljaju i građevna funkcija, budući da ih njihova netopljivost u vodi čini bitnim sastavnim dijelovima staničnih membrana.
Puno hormoni(npr. kora nadbubrežne žlijezde, gonade) su derivati lipida. Stoga se karakteriziraju lipidi regulatorna funkcija.
Lipidi. masti. Hormoni. Funkcije lipida: energetska, skladišna, zaštitna, građevna, regulatorna
Pitanja
1. Koje tvari su lipidi?
2. Kakvu strukturu ima većina lipida?
3. Koje funkcije obavljaju lipidi?
4. Koje su stanice i tkiva najbogatije lipidima?
Zadaci
Nakon analize teksta odlomka, objasnite zašto mnoge životinje prije zime, a ribe selice prije mrijesta, imaju tendenciju nakupljanja više masti. Navedi primjere životinja i biljaka kod kojih je ova pojava najizraženija. Je li višak masnoće uvijek dobar za tijelo? Raspravite o ovom problemu u razredu.
§ 7. Sastav i struktura proteina
1. Koja je uloga proteina u organizmu?
2. Koje su namirnice bogate proteinima?
Među organskim tvarima vjeverice, ili bjelančevine, najbrojniji su, najraznovrsniji i od iznimne važnosti biopolimeri. Oni čine 50-80% suhe mase stanice.
Molekule bjelančevina velike su veličine, zbog čega se i zovu makromolekule. Osim ugljika, kisika, vodika i dušika, proteini mogu sadržavati sumpor, fosfor i željezo. Proteini se međusobno razlikuju po broju (od sto do nekoliko tisuća), sastavu i redoslijedu monomera. Proteinski monomeri su aminokiseline (slika 8).
Beskonačna raznolikost proteina stvorena je različitim kombinacijama od samo 20 aminokiselina. Svaka aminokiselina ima svoje ime, posebnu strukturu i svojstva. Njihovo opća formula može se predstaviti u sljedećem obliku:

Molekula aminokiseline sastoji se od dva dijela identična svim aminokiselinama, od kojih je jedan amino skupina (-NH 2) s bazičnim svojstvima, a drugi je karboksilna skupina (-COOH) s kiselim svojstvima. Dio molekule koji se naziva radikal (R) ima različitu strukturu za različite aminokiseline. Prisutnost bazičnih i kiselih skupina u jednoj molekuli aminokiseline određuje njihovu visoku reaktivnost. Preko ovih skupina aminokiseline se spajaju u tvorbu proteina. U tom se slučaju pojavljuje molekula vode i formiraju se oslobođeni elektroni peptidna veza. Zato se proteini nazivaju polipeptidi.

Riža. 8. Primjeri strukture aminokiselina – monomera proteinskih molekula

Proteinske molekule mogu imati različite prostorne konfiguracije - struktura proteina, a u njihovoj strukturi postoje četiri razine strukturna organizacija(slika 9).
Redoslijed aminokiselina u polipeptidnom lancu je primarna struktura vjeverica. Jedinstven je svakom proteinu i određuje njegov oblik, svojstva i funkcije.
Većina proteina ima spiralni oblik kao rezultat stvaranja vodikovih veza između CO i NH skupina različitih aminokiselinskih ostataka polipeptidnog lanca. Vodikove veze su slabe, ali zajedno daju prilično jaku strukturu. Ova spirala je sekundarna struktura vjeverica.
Tercijarna struktura– trodimenzionalno prostorno “pakiranje” polipeptidnog lanca. Rezultat je bizarna, ali specifična konfiguracija za svaki protein - kap. Snaga tercijarne strukture osigurava se različitim vezama koje nastaju između radikala aminokiselina.

Riža. 9. Shema građe proteinske molekule: I, II, III, IV – primarna, sekundarna, tercijarna, kvaternarna struktura
Kvartarna struktura nije tipično za sve proteine. Nastaje kao rezultat kombinacije nekoliko makromolekula s tercijarnom strukturom u složen kompleks. Na primjer, hemoglobin ljudske krvi je kompleks od četiri proteinske makromolekule (slika 10).
Ova složenost strukture proteinskih molekula povezana je s raznolikošću funkcija svojstvenih tim biopolimerima.
Kršenje prirodne strukture proteina naziva se denaturacija(slika 11). Može nastati pod utjecajem temperature, kemijske tvari, energija zračenja i drugi čimbenici. Slabim udarom raspada se samo kvaternarna struktura, jačim tercijarna, a potom i sekundarna, a protein ostaje u obliku polipeptidnog lanca.

Riža. 10. Shema strukture molekule hemoglobina
Taj je proces djelomično reverzibilan: ako primarna struktura nije uništena, tada denaturirani protein može obnoviti svoju strukturu. Iz toga slijedi da su sve strukturne značajke proteinske makromolekule određene njenom primarnom strukturom.
Osim jednostavnih proteina, koji se sastoji samo od aminokiselina, također postoje složenih proteina, što može uključivati ugljikohidrate ( glikoproteini), masti ( lipoproteini), nukleinske kiseline ( nukleoproteini) i tako dalje.
Uloga proteina u životu stanice je ogromna. Moderna biologija je pokazala da su sličnosti i razlike između organizama u konačnici određene skupom proteina. Što su organizmi bliži jedan drugome u sustavnom položaju, to su njihovi proteini sličniji.

Riža. 11. Denaturacija proteina
Proteini, odnosno proteini. Jednostavni i složeni proteini. Aminokiseline. polipeptid. Primarna, sekundarna, tercijarna i kvaternarna struktura proteina
Pitanja
1. Koje se tvari nazivaju bjelančevine ili bjelančevine?
2. Koja je primarna struktura proteina?
3. Kako nastaju sekundarne, tercijarne i kvaternarne strukture proteina?
4. Što je denaturacija proteina?
5. Na temelju čega se proteini dijele na jednostavne i složene?
Zadaci
Znate da se bjelanjak kokošjeg jajeta sastoji uglavnom od bjelančevina. Razmislite o tome što objašnjava promjenu strukture proteina kuhanog jajeta. Navedite druge primjere za koje znate gdje se struktura proteina može promijeniti.
§ 8. Funkcije proteina
1. Koja je funkcija ugljikohidrata?
2. Koje funkcije proteina poznajete?
Proteini obavljaju iznimno važne i raznolike funkcije. To je uvelike moguće zahvaljujući raznolikosti oblika i sastava samih proteina.
Jedna od najvažnijih funkcija proteinskih molekula je konstrukcija (plastični). Proteini su dio svih staničnih membrana i staničnih organela. Stijenke krvnih žila, hrskavica, tetive, kosa i nokti sastoje se pretežno od proteina.
Od velike važnosti katalitički, ili enzimska, proteinska funkcija. Posebni proteini - enzimi sposobni su desetke i stotine milijuna puta ubrzati biokemijske reakcije u stanicama. Poznato je oko tisuću enzima. Svaku reakciju katalizira određeni enzim. U nastavku ćete saznati više o tome.
Motorička funkcija izvode posebne kontraktilne bjelančevine. Zahvaljujući njima, trepavice i flagele se pomiču u protozoama, kromosomi se pomiču tijekom stanične diobe, mišići se skupljaju u višestaničnim organizmima, a druge vrste kretanja u živim organizmima se poboljšavaju.
To je važno transportna funkcija bjelančevine. Dakle, hemoglobin prenosi kisik iz pluća u stanice drugih tkiva i organa. U mišićima, osim hemoglobina, postoji još jedan protein za prijenos plina - mioglobin. Serumski proteini potiču transport lipida i masnih kiselina, biološki raznolikih djelatne tvari. Transportni proteini u vanjskoj membrani stanica nose razne tvari iz okoline u citoplazmu.
Specifični proteini obavljaju zaštitnu funkciju . Oni štite tijelo od invazije stranih bjelančevina i mikroorganizama te od oštećenja. Dakle, antitijela koja proizvode limfociti blokiraju strane proteine; fibrin i trombin štite tijelo od gubitka krvi.
Regulatorna funkcija svojstvena proteinima - hormoni. Održavaju konstantnu koncentraciju tvari u krvi i stanicama, sudjeluju u rastu, razmnožavanju i drugim vitalnim funkcijama. važne procese. Na primjer, inzulin regulira šećer u krvi.
Proteini također imaju signalna funkcija. Stanična membrana sadrži proteine koji mogu promijeniti svoju tercijarnu strukturu kao odgovor na čimbenike okoliša. Tako se primaju signali iz vanjskog okruženja i informacije prenose u stanicu.
Proteini mogu izvesti energetska funkcija, kao jedan od izvora energije u stanici. Kada se 1 g proteina potpuno razgradi na konačne produkte, oslobađa se 17,6 kJ energije. Međutim, proteini se iznimno rijetko koriste kao izvor energije. Aminokiseline koje se oslobađaju kada se proteinske molekule razgrade koriste se za izgradnju novih proteina.
Funkcije proteina: građevna, motorna, transportna, zaštitna, regulatorna, signalna, energetska, katalitička. Hormon. Enzim
Pitanja
1. Što objašnjava raznolikost funkcija proteina?
2. Koje funkcije proteina poznajete?
3. Koju ulogu igraju hormonski proteini?
4. Koju funkciju obavljaju proteini enzima?
5. Zašto se proteini rijetko koriste kao izvor energije?
§ 9. Nukleinske kiseline
1. Koja je uloga jezgre u stanici?
2. Uz koje je stanične organele vezan prijenos nasljednih karakteristika?
3. Koje se tvari nazivaju kiselinama?
Nukleinske kiseline(od lat. jezgra– nucleus) prvi su put otkriveni u jezgri leukocita. Naknadno je utvrđeno da se nukleinske kiseline nalaze u svim stanicama, ne samo u jezgri, već iu citoplazmi i raznim organelama.
Postoje dvije vrste nukleinskih kiselina - deoksiribonukleinske(skraćeno DNK) I ribonukleinske(skraćeno RNA). Razlika u imenima objašnjava se činjenicom da molekula DNA sadrži ugljikohidrat deoksiriboza, a molekula RNA je riboza.
Nukleinske kiseline su biopolimeri koji se sastoje od monomera - nukleotidi. Nukleotidni monomeri DNA i RNA imaju sličnu strukturu.
Svaki nukleotid sastoji se od tri komponente povezane jakim kemijskim vezama. Ovaj dušična baza, ugljikohidrat(riboza ili deoksiriboza) i ostatak fosforna kiselina (slika 12).
Dio molekule DNA Postoje četiri vrste dušičnih baza: adenin, gvanin, citozin ili timin. Oni određuju nazive odgovarajućih nukleotida: adenil (A), gvanil (G), citidil (C) i timidil (T) (slika 13).

Riža. 12. Shema strukture nukleotida - DNA (A) i RNA (B) monomera
Svaki lanac DNA je polinukleotid koji se sastoji od nekoliko desetaka tisuća nukleotida.
Molekula DNA ima složenu strukturu. Sastoji se od dva spiralno uvijena lanca, koji su cijelom svojom dužinom međusobno povezani vodikovim vezama. Ova struktura, karakteristična samo za molekule DNA, naziva se dvostruka spirala.

Riža. 13. DNA nukleotidi

Riža. 14. Komplementarna veza nukleotida
Kada se formira dvostruka spirala DNK, dušične baze jednog lanca raspoređene su u strogo definiranom redoslijedu nasuprot dušičnim bazama drugog. U ovom slučaju otkriva se važan obrazac: timin drugog lanca uvijek se nalazi nasuprot adeninu jednog lanca, citozin se uvijek nalazi nasuprot gvaninu i obrnuto. To se objašnjava činjenicom da nukleotidni parovi adenin i timin, kao i gvanin i citozin međusobno strogo odgovaraju i komplementarni su, odn. komplementarni(od lat. komplementum- zbrajanje), međusobno. I sam uzorak se zove načelo komplementarnosti. U tom slučaju između adenina i timina uvijek nastaju dvije vodikove veze, a između gvanina i citozina tri (slika 14).
Prema tome, u svakom organizmu broj adenilnih nukleotida jednak je broju timidilnih nukleotida, a broj gvanilnih nukleotida jednak je broju citidilnih nukleotida. Poznavajući redoslijed nukleotida u jednom lancu DNK, principom komplementarnosti može se uspostaviti redoslijed nukleotida u drugom lancu.
Pomoću četiri vrste Nukleotidi u DNK sadrže sve informacije o tijelu, koje se prenose sljedećim generacijama. Drugim riječima, DNK je nositelj nasljedne informacije.
Molekule DNA uglavnom se nalaze u jezgrama stanica, ali male količine nalaze se u mitohondrijima i plastidima.
Molekula RNA, za razliku od molekule DNA, je polimer koji se sastoji od jednog lanca mnogo manjih dimenzija.
RNA monomeri su nukleotidi koji se sastoje od riboze, ostatka fosforne kiseline i jedne od četiri dušične baze. Tri dušične baze - adenin, gvanin i citozin - iste su kao one u DNK, a četvrta - uracil.
Stvaranje RNA polimera događa se kovalentnim vezama između riboze i ostatka fosforne kiseline susjednih nukleotida.
Postoje tri vrste RNA koje se razlikuju po strukturi, veličini molekule, položaju u stanici i funkcijama koje obavljaju.
Ribosomska RNA (rRNA) dio su ribosoma i sudjeluju u formiranju njihovih aktivnih centara, gdje se odvija proces biosinteze proteina.
Prijenosne RNA (tRNA) – najmanji po veličini – transportiraju aminokiseline do mjesta sinteze proteina.
Informacija, ili predložak, RNA (mRNA) sintetiziraju se na dijelu jednog od lanaca molekule DNA i prenose informacije o strukturi proteina od stanične jezgre do ribosoma, gdje se te informacije implementiraju.
Tako, Različite vrste RNA predstavljaju jedan funkcionalni sustav usmjeren na implementaciju nasljednih informacija kroz sintezu proteina.
Molekule RNA nalaze se u jezgri, citoplazmi, ribosomima, mitohondrijima i plastidima stanice.
Nukleinske kiseline. Deoksiribonukleinska kiselina ili DNK. Ribonukleinska kiselina ili RNA. Dušične baze: adenin, gvanin, citozin, timin, uracil, nukleotid. Dvostruka spirala. Komplementarnost. Prijenosna RNA (tRNA). Ribosomska RNA (rRNA). glasnička RNA (mRNA)
Pitanja
1. Kakva je struktura nukleotida?
2. Kakva je struktura molekule DNA?
3. Što je načelo komplementarnosti?
4. Koje su sličnosti i razlike u građi molekula DNA i RNA?
5. Koje vrste molekula RNA poznajete? Koje su njihove funkcije?
Zadaci
1. Ocrtajte svoj odlomak.
2. Znanstvenici su otkrili da fragment lanca DNA ima sljedeći sastav: C-G G A A A T T C C. Koristeći načelo komplementarnosti dovršite drugi lanac.
3. Tijekom istraživanja utvrđeno je da u proučavanoj molekuli DNA adenini čine 26% ukupnog broja dušičnih baza. Izbrojte druge dušične baze u ovoj molekuli.
Koji elementi prevladavaju u živim organizmima?
Zašto se molekule proteina, nukleinskih kiselina, ugljikohidrata i lipida smatraju biopolimerima samo u stanici?
Što se podrazumijeva pod riječju univerzalnost molekula biopolimera?
a) redoslijed izmjene aminokiselina
b) broj aminokiselina u molekuli
c) oblik tercijarne strukture
d) sve navedene značajke
3. U kojem je slučaju ispravno naznačen sastav nukleotida DNA?
a) riboza, ostatak fosforne kiseline, timin
b) fosforna kiselina, uracil, deoksiriboza
c) ostatak fosforne kiseline, deoksiriboza, adenin
d) fosforna kiselina, riboza, gvanin
4. Monomeri nukleinskih kiselina su:
a) dušične baze
b) riboza ili deoksiriboza
c) deoksiribozne i fosfatne skupine
d) nukleotidi
5. Aminokiseline u proteinskoj molekuli povezane su preko:
a) ionska veza
b) peptidna veza
c) vodikova veza
6. Koja je funkcija prijenosne RNA?
a) prenosi aminokiseline na ribosome
b) prenosi informacije iz DNK
c) stvara ribosome
d) sve navedene funkcije
7. Enzimi su biokatalizatori koji se sastoje od:
a) bjelančevine b) nukleotidi c) lipidi c) masti
8. Polisaharidi uključuju:
a) škrob, riboza
b) glikogen, glukoza
c) celuloza, škrob
d) škrob, saharoza
9. Ugljik kao element uključuje:
a) bjelančevine i ugljikohidrati
b) ugljikohidrati i lipidi
c) ugljikohidrati i nukleinske kiseline
d) svi organski spojevi stanice
10. Stanica sadrži DNK:
a) u jezgri i mitohondrijima
b) u jezgri, citoplazmi i raznim organelama
c) u jezgri, mitohondrijima i citoplazmi
d) u jezgri, mitohondrijima, kloroplastima
ŠTO JE MONOMETAR NUKLEINSKIH KISEINA? OPCIJE (AMINOKISELINA, NUKLEOTID, MOLEKULA PROTEINA?) ŠTO JE UKLJUČENOSASTAV NUKLEOTIDA
OPCIJE: (AMINOKISELINA, DUŠIČNA BAZA, OSTATAK FOSFORNE KISELINE, UGLJIKOHIDRAT?)
Pomozi mi molim te!1. Znanost koja proučava stanice zove se:
A) Genetika;
B) Odabir;
B) ekologija;
B) Citologija.
2. Organske tvari stanice:
A) Voda, minerali, masti;
B) Ugljikohidrati, lipidi, proteini, nukleinske kiseline;
C) Ugljikohidrati, minerali, masti;
D) Voda, minerali, proteini.
3. Od svih organskih tvari, glavninu stanice čine:
A) Proteini.
B) Ugljikohidrati
B) Masti
D) Voda.
4. Istaknute riječi zamijenite jednom riječju:
A) Male molekule organskih tvari tvore u stanici složene molekule.
B) Stalne strukturne komponente stanice obavljaju vitalne funkcije za stanicu.
C) Visoko uređeno, polutekuće unutarnje okruženje stanice osigurava kemijsku interakciju svih staničnih struktura.
D) Glavni fotosintetski pigment daje zelenu boju kloroplastima.
5. Akumulacija i pakiranje kemijski spojevi u kavezu provode:
A) Mitohondriji;
B) Ribosomi;
B) Lizosomi;
D) Golgijev kompleks.
6. Funkcije unutarstanične probave obavljaju:
A) Mitohondriji;
B) Ribosomi;
B) Lizosomi;
D) Golgijev kompleks.
7. "Sklapanje" polimerne proteinske molekule se provodi:
A) Mitohondriji;
B) Ribosomi;
B) Lizosomi;
D) Golgijev kompleks.
8. Ukupnost kemijske reakcije pri čemu dolazi do razgradnje organskih tvari i oslobađanja energije naziva se:
A) Katabolizam;
B) anabolizam;
B) Metabolizam;
D) Asimilacija
9. "Varanje" genetske informacije iz molekule DNA stvaranjem mRNA naziva se:
A) Emitiranje;
B) Transkripcija;
B) Biosinteza;
D) Glikoliza.
10. Proces stvaranja organskih tvari na svjetlu u kloroplastima pomoću vode i ugljičnog dioksida naziva se:
A) Fotosinteza;
B) Transkripcija;
B) Biosinteza;
D) Glikoliza.
11. Enzimski i bezkisikov proces razgradnje organskih tvari naziva se:
A) Fotosinteza;
B) Transkripcija;
B) Biosinteza;
D) Glikoliza.
12. Navedite glavne odredbe stanične teorije.
Pogledaj korijen!
Kozma Prutkov
Koji kemijski elementi su dio žive stanice? Kakvu ulogu igraju šećeri i lipidi? Kako su proteini strukturirani i kako njihove molekule dobivaju određeni prostorni oblik? Što su enzimi i kako prepoznaju svoje supstrate? Kakva je struktura molekula RNA i DNA? Koje značajke molekule DNK omogućuju joj da igra ulogu nositelja genetske informacije?
Lekcija-predavanje
ELEMENTARNI I MOLEKULARNI SASTAV ŽIVIH BIĆA. Upoznavanje sa živim sustavima započinjemo s molekularne genetske razine. To je razina molekula koje čine strukturnu i funkcionalnu osnovu stanica živih organizama.
Retrovirus. Virusi pokazuju nevjerojatne geometrijske oblike!
Sjetimo se da je od svih poznatih elemenata uključenih u Periodni sustav elemenata D. I. Mendelejeva, u živoj ćeliji pronađeno ih je oko 80. Štoviše, među njima nema niti jednog koji bi bio odsutan u neživoj prirodi. To služi kao jedan od dokaza zajedništva žive i nežive prirode.
Više od 90% mase stanice sastoji se od ugljika, vodika, dušika i kisika. Sumpor, fosfor, kalij, natrij, kalcij, magnezij, željezo i klor u stanici se nalaze u mnogo manjim količinama. Svi ostali elementi (cink, bakar, jod, fluor, kobalt, mangan itd.) zajedno ne čine više od 0,02% stanične mase. Zato se i zovu mikroelementi. Mikroelementi su dio hormona, enzima i vitamina, odnosno spojeva visoke biološke aktivnosti.
Na primjer, nedostatak joda u tijelu, neophodnog za proizvodnju hormona štitnjače - tiroksina, dovodi do smanjenja proizvodnje ovog hormona i, kao posljedica toga, do razvoja ozbiljnih bolesti, uključujući kretenizam.
Većina sadržaja stanice je voda. Mnoge tvari ulaze ili izlaze iz stanice u obliku vodene otopine, većina unutarstaničnih reakcija događa se i u vodenom okolišu. Štoviše, voda također izravno sudjeluje u nizu kemijskih reakcija, donirajući H + ili OH - ione nastalim spojevima. Zbog svog visokog toplinskog kapaciteta, voda stabilizira temperaturu unutar ćelije, čineći je manje ovisnom o temperaturnim fluktuacijama u okolini koja okružuje stanicu.
Osim vode, koja čini 70% volumena stanice, sadrži i organske tvari – spojeve ugljika. Među njima ima male molekule koji sadrže do 30 atoma ugljika, te makromolekule. Prvi uključuju jednostavne šećere (monosaharide), lipide, aminokiseline i nukleotide. Oni služe kao strukturne komponente za izgradnju makromolekula, a osim toga igraju se značajnu ulogu u procesima metabolizma i energije žive stanice.
Pa ipak, temelj života na molekularnoj razini su proteini i nukleinske kiseline, o kojima ćemo detaljnije govoriti.
AMINOKISELINE I PROTEINI. Posebnu ulogu u živoj prirodi imaju vjeverice. Oni služe kao građevni materijal stanice, a gotovo nijedan od procesa koji se odvijaju u stanicama ne može se dogoditi bez njihovog sudjelovanja.
Molekula proteina je lanac aminokiselina, a broj karika u takvom lancu može varirati od desetaka do nekoliko tisuća. Susjedne aminokiseline su međusobno povezane na poseban način kemijska veza, koji se zove peptid. Ova veza nastaje tijekom procesa sinteze proteina, kada se karboksilna skupina jedne aminokiseline veže na susjednu amino skupinu druge aminokiseline (slika 32).

Riža. 32. Peptidna veza
Svih 20 vrsta aminokiselina sudjeluje u izgradnji proteina. Međutim, redoslijed njihove izmjene u proteinskom lancu je vrlo različit, što stvara mogućnost za veliki broj kombinacija, a time i za izgradnju brojnih vrsta proteinskih molekula. Treba napomenuti da samo biljke mogu sintetizirati svih 20 aminokiselina potrebnih za izgradnju proteina. Životinje dobivaju niz aminokiselina, koje se nazivaju esencijalne aminokiseline, jedući biljke.
Redoslijed aminokiselina u proteinskoj molekuli označava se kao primarna struktura vjeverica (slika 33). Postoje također sekundarna struktura protein, koji se razumijeva kao priroda prostornog rasporeda pojedinih fragmenata lanca aminokiselina. U sekundarna struktura dijelovi proteinske molekule imaju oblik spirala ili presavijenih slojeva. U njihovu nastanku važnu ulogu imaju vodikove veze uspostavljene između kisika i vodika. peptidne veze(-N-H...0=C-) različite aminokiseline.

Riža. 33. Struktura proteina
Pod, ispod tercijarna struktura protein se odnosi na prostorni raspored cijelog lanca aminokiselina.
Tercijarna struktura ima izravan utjecaj na oblik proteinske molekule, koja može biti nitasta ili okrugla. U potonjem slučaju, molekula je presavijena na takav način da su njezina hidrofobna područja unutra, a polarne hidrofilne skupine na površini. Dobivena prostorna struktura naziva se kap.
Konačno, neki proteini mogu sadržavati nekoliko globula, od kojih je svaka formirana neovisnim lancem aminokiselina. Kombinacija nekoliko globula u jedan kompleks označena je pojmom kvartarna struktura vjeverica. Na primjer, molekula proteina hemoglobina sastoji se od četiri globule koje sadrže neproteinski dio - hem.
Molekula proteina sposobna je samoorganizirati se u složenu prostornu strukturu čija je konfiguracija specifična i određena slijedom aminokiselina, odnosno primarnom strukturom proteina.
Samoorganizacija je jedno od jedinstvenih svojstava proteina, koje je u osnovi mnogih funkcija koje obavljaju. Konkretno, mehanizam prepoznavanja vlastitim enzimima (biološkim katalizatorima) temelji se na specifičnosti prostorne strukture proteinske molekule. supstrat, tj. molekula koja nakon interakcije s enzimom prolazi kroz određene kemijske transformacije i pretvara se u proizvod.
Enzimi su proteini čiji određeni dio molekule čini aktivno središte. Veže supstrat specifičan za određeni enzim i pretvara ga u proizvod. U ovom slučaju, enzim je sposoban razlikovati svoj supstrat zahvaljujući posebnoj prostornoj konfiguraciji aktivnog centra, specifičnoj za svaki enzim. Možete zamisliti da supstrat pristaje enzimu poput ključa u bravu.
Uvjereni ste da se sva svojstva proteina temelje na njegovoj primarnoj strukturi – slijedu aminokiselina u molekuli. Može se usporediti s riječju koja je napisana abecedom koja se sastoji od 20 slova aminokiselina. A ako postoje riječi, onda može postojati šifra kojom se te riječi mogu kodirati. Kako? Poznavanje strukture nukleinskih kiselina pomoći će odgovoriti na ovo pitanje.
NUKLEOTIDE I NUKLEINSKE KISELINE. Nukleotidi se sastoje od cikličkog spoja koji sadrži dušik (dušikova baza), šećera s pet ugljika i ostatka fosforne kiseline. Od njih su građene makromolekule nukleinskih kiselina.
Sastav molekula RNA(ribonukleinska kiselina) uključuje nukleotide izgrađene na šećeru ribozi i sadrže adenin (A), gvanin (G), citozin (C) i uracil (U) kao dušične baze. Nukleotidi koji čine molekulu DNK(deoksiribonukleinska kiselina), sadrže deoksiribozu, a umjesto uracila - timin (T).
Međusobno povezivanje nukleotida u molekuli DNA (RNA) nastaje zbog povezivanja fosfornog ostatka jednog nukleotida s deoksiribozom (ribozom) drugog (slika 34).

Riža. 34. Sastav lanca i struktura molekule DNA
U tijeku proučavanja sastava molekula DNA, utvrđeno je da je u svakoj od njih broj dušičnih baza adenina (A) jednak broju timina (T), a broj gvanina (G) jednak je na broj citozina (C). Ovo je otkriće poslužilo kao preduvjet da su J. Watson i F. Crick 1953. godine stvorili model molekule DNA - poznatu dvostruku spiralu.
Prema tom modelu, molekula DNA se sastoji od dva lanca koji su uvijeni u desnu spiralu (slika 35).

Riža. 35. Model strukture DNA
Svaki lanac sadrži niz nukleotida koji strogo odgovara (komplementaran) nizu drugog lanca. Ova korespondencija se postiže prisutnošću vodikovih veza između dušičnih baza dvaju lanaca usmjerenih jedan prema drugom - A i T ili G i C.
Komunikacija između ostalih parova dušičnih baza je nemoguća, budući da je prostorna struktura molekula dušikovih baza takva da se samo A i T, kao i G i C, mogu dovoljno približiti da tvore međusobne vodikove veze.
Najvažnija značajka DNK je mogućnost njenog samodupliciranja – replikacija, koji se provodi uz sudjelovanje skupine enzima (slika 36).

Riža. 36. Shema replikacije DNA
U određenim područjima, uključujući na jednom od krajeva, dvolančane spiralne molekule DNA, vodikove veze između lanaca se prekidaju. Odvoje se i odmotaju.
Ovaj proces postupno preuzima cijelu molekulu. Kako se lanci roditeljske molekule odvajaju na njima, kao na matrici, od onih dostupnih u okoliš nukleotida, grade se lanci kćeri. Sklapanje novog lanca odvija se u strogom skladu s načelom komplementarnosti: protiv svakog A postoji T, protiv G - C, itd. Kao rezultat, dobivene su dvije nove molekule DNA, od kojih svaka ima jedan lanac lijevo od originalna molekula DNK, a druga je nova. U ovom slučaju, dvije molekule DNK nastale tijekom replikacije identične su originalnoj.
Sposobnost molekule DNA da se sama kopira je osnova za prijenos nasljednih informacija od strane živih organizama. Slijed nukleotidnih baza u molekuli DNA služi kao šifra koja kodira informacije o proteinima potrebnim za funkcioniranje organizma.
Za razliku od DNA, molekula RNA sastoji se od jednog polinukleotidnog lanca. Postoji nekoliko vrsta RNA koje obavljaju različite funkcije u stanici. RNA kopija dijela lanca DNA naziva se informacija ili messenger RNA(mRNA) i ima ulogu posrednika u prijenosu genetske informacije od DNA do staničnih struktura koje sintetiziraju protein – ribosome. Osim toga, stanica sadrži ribosomska RNA(rRNA), koja zajedno s proteinima tvori ribosome, prijenosne RNA(tRNA), transport aminokiselina do mjesta sinteze proteina, i neki drugi.
Molekula DNA sastoji se od dvaju komplementarnih lanaca nukleotida umotanih u spiralu, koji se zajedno drže vodikovim vezama. tvoreći A-T I G-C parovi osnove. Nukleotidni slijed lanca DNA služi kao kod koji kodira genetske informacije. Dešifriranje ovih informacija provodi se uz sudjelovanje RNA molekula. Sposobnost samokopiranja (umnožavanja) DNA daje mogućnost prijenosa genetske informacije u živoj prirodi.
- Zašto se proteini nazivaju molekulama života?
- Koja je uloga prostornih struktura proteina u životnim procesima stanice?
- Koje je načelo u osnovi procesa replikacije DNA?