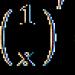Pošaljite svoj dobar rad u bazu znanja jednostavno je. Koristite obrazac u nastavku
Studenti, diplomanti, mladi znanstvenici koji koriste bazu znanja u svom studiju i radu bit će vam vrlo zahvalni.
Objavljeno na http://www.allbest.ru/
Državna proračunska obrazovna ustanova visokog stručnog obrazovanja "Baškirsko državno medicinsko sveučilište"
Ministarstvo zdravstva Rusije
Zavod za mikrobiologiju, virusologiju i imunologiju
glava odjela, doktor medicinskih znanosti
Profesor Z.G. Gabidulin
U mikrobiologiji na temu: “Faze formiranja imunologije”
Izvršila studentica 2. god
Medicinski fakultet gr. L-306A
Afanasjev V.A.
Uvod
Imunologija je nastala kao dio mikrobiologije kao rezultat njezine praktična aplikacija za liječenje zaraznih bolesti, stoga se infektivna imunologija razvila u prvom stupnju.
Od svog nastanka, imunologija je bila u bliskoj interakciji s drugim znanostima: genetikom, fiziologijom, biokemijom, citologijom. Tijekom proteklih 30 godina postala je golema, neovisna temeljna biološka znanost. Medicinska imunologija praktički rješava većinu pitanja dijagnostike i liječenja bolesti i po tom pitanju zauzima središnje mjesto u medicini.
Počeci imunologije leže u promatranjima starih naroda. U Egiptu i Grčkoj se znalo da ljudi više ne obolijevaju od kuge i stoga su oni koji su bili bolesni uključeni u brigu o bolesnima. Prije nekoliko stoljeća u Turskoj, na Bliskom istoku i u Kini, kako bi se spriječile boginje, gnoj iz osušenih čireva velikih boginja utrljavao se u kožu ili sluznicu nosa. Takva infekcija obično je uzrokovala blaži oblik malih boginja i stvarala imunitet na ponovnu infekciju. Ova metoda sprječavanja malih boginja naziva se variolacija. Međutim, kasnije se pokazalo da je ova metoda daleko od sigurne, jer ponekad dovodi do teških boginja i smrti.
Imunologija u antičko doba
Od davnina su ljudi znali da pacijenti koji su imali kravlje boginje ne razviju prirodnu bolest. Engleski liječnik E. Jenner je 25 godina kroz brojne studije provjeravao te podatke i došao do zaključka da infekcija kravljim boginjama sprječava velike boginje. Godine 1796. Jenner je u osmogodišnjeg dječaka ucijepio materijal iz apscesa malih boginja žene zaražene kravljim boginjama. Nekoliko dana kasnije dječak je dobio temperaturu i pojavili su se čirevi na mjestu ubrizgavanja zaraznog materijala. Zatim su ti fenomeni nestali. Nakon 6 tjedana ubrizgan mu je materijal iz pustula oboljelog od malih boginja, ali dječak se nije razbolio. Ovim pokusom Jenner je prvi utvrdio mogućnost prevencije velikih boginja. Metoda je postala široko rasprostranjena u Europi, zbog čega se učestalost velikih boginja naglo smanjila.
Glavna imena mikrobiologije i imunologije
Znanstveno utemeljene metode za sprječavanje zaraznih bolesti razvio je veliki francuski znanstvenik Louis Pasteur. Godine 1880. Pasteur je proučavao pileću koleru. U jednom od pokusa, za zarazu pilića, koristio je staru kulturu uzročnika kokošje kolere, koja je dugo bila pohranjena na temperaturi od 37 °C. Neki od zaraženih pilića su preživjeli, a nakon ponovne infekcije sa svježom kulturom, pilići nisu umrli. Pasteur je o ovom eksperimentu izvijestio Parišku akademiju znanosti i predložio da se oslabljeni mikrobi mogu koristiti za sprječavanje zaraznih bolesti. Oslabljene kulture nazvane su cjepivima (Vacca – krava), a način prevencije cijepljenjem. Nakon toga, Pasteur je dobio cjepiva protiv antraksa i bjesnoće. Načela dobivanja cjepiva i metode njihove upotrebe koje je razvio ovaj znanstvenik već se 100 godina uspješno koriste za prevenciju zaraznih bolesti. Međutim, dugo se nije znalo kako se stvara imunitet.
Razvoju imunologije kao znanosti uvelike su pridonijela istraživanja I. I. Mečnikova. Po obrazovanju, I. I. Mechnikov je bio zoolog, radio je u Odesi, zatim u Italiji i Francuskoj, na Institutu Pasteur. Dok je radio u Italiji, vršio je pokuse s ličinkama morskih zvijezda u koje je ubrizgavao ružino trnje. Istodobno je primijetio da se mobilne stanice nakupljaju oko bodlji, obavijaju ih i zarobljavaju. I. I. Mečnikov razvio je fagocitnu teoriju imuniteta, prema kojoj se tijelo oslobađa od mikroba uz pomoć fagocita.
Drugi smjer u razvoju imunologije zastupao je njemački znanstvenik P. Ehrlich. Smatrao je da su glavni zaštitni mehanizam protiv infekcije humoralni čimbenici krvnog seruma - antitijela. DO kraj 19. stoljeća stoljeća postalo je jasno da se ta dva gledišta ne isključuju, nego nadopunjuju. Godine 1908. I. I. Mečnikov i P. Ehrlich dobili su Nobelovu nagradu za razvoj doktrine imuniteta.
Posljednja dva desetljeća 19. stoljeća obilježena su izvanrednim otkrićima na području medicinske mikrobiologije i imunologije. Antitoksični tetanusni i antidifterijski serumi dobiveni su imunizacijom kunića toksinom difterije i tetanusa. Tako se prvi put u medicinskoj praksi pojavio učinkovit lijek za liječenje i prevenciju difterije i tetanusa. Za ovo otkriće Bering je 1902. godine dobio Nobelovu nagradu.
Godine 1885. Buchner i suradnici ustanovili su da se u svježem krvnom serumu mikrobi ne razmnožavaju, odnosno da on ima bakteriostatska i baktericidna svojstva. Tvar sadržana u serumu bila je uništena zagrijavanjem i dugotrajnim skladištenjem. Ehrlich je kasnije ovu tvar nazvao komplementom.
Belgijski znanstvenik J. Bordet pokazao je da baktericidna svojstva seruma određuju ne samo komplement, već i specifična protutijela.
Godine 1896. Gruber i Durham ustanovili su da kod imunizacije životinja različitim mikrobima u serumu nastaju protutijela koja uzrokuju lijepljenje (aglutinaciju) tih mikroba. Ta su otkrića proširila razumijevanje mehanizama antibakterijske zaštite i omogućila primjenu reakcije aglutinacije u praktične svrhe. Vidal je već 1895. upotrijebio test aglutinacije za dijagnosticiranje trbušnog tifusa. Nešto kasnije razvijene su serološke metode za dijagnosticiranje tularemije, bruceloze, sifilisa i mnogih drugih bolesti koje se sve do danas široko koriste u klinici zaraznih bolesti.
Godine 1897. Krause je otkrio da osim aglutinina kod imunizacije životinja mikrobima nastaju i precipitini koji se spajaju ne samo s mikrobnim stanicama, već i s produktima njihova metabolizma. Kao rezultat toga nastaju netopivi imunološki kompleksi koji se talože.
Godine 1899. Ehrlich i Morgenroth ustanovili su da crvene krvne stanice adsorbiraju specifična protutijela na svojoj površini i da se liziraju kada im se doda komplement. Ta je činjenica bila važna za razumijevanje mehanizma reakcije antigen-antitijelo.
Imunologija kao temeljna znanost
Početak 20. stoljeća obilježilo je otkriće koje je imunologiju transformiralo iz empirijske u temeljnu znanost i postavilo temelje za razvoj neinfektivne imunologije. Godine 1902. austrijski znanstvenik K. Landsteiner razvio je metodu za konjugaciju haptena s nosačima. To je otvorilo temeljno nove mogućnosti za proučavanje antigene strukture tvari i procesa sinteze protutijela. Landsteiner je otkrio izoantigene ljudskih eritrocita ABO sustava i krvne grupe. Postalo je jasno da postoji heterogenost u antigenskoj strukturi različitih organizama (antigenska individualnost), te da je imunitet biološki fenomen, što je izravno povezano s evolucijom.
Godine 1902. francuski znanstvenici Richet i Portier otkrili su fenomen anafilaksije, na temelju čega je kasnije stvorena doktrina alergije.
Godine 1923. Gleny i Ramon otkrili su mogućnost pretvaranja bakterijskih egzotoksina pod utjecajem formaldehida u netoksične tvari - toksoide s antigenskim svojstvima. To je omogućilo korištenje toksoida kao cjepiva.
Serološke metode istraživanja koriste se u drugom smjeru - za klasifikaciju bakterija. Koristeći antipneumokokne serume, Griffith je 1928. godine podijelio pneumokoke u 4 tipa, a Lensfield je, koristeći antiserume protiv grupno specifičnih antigena, sve streptokoke razvrstao u 17 seroloških skupina. Mnoge vrste bakterija i virusa već su klasificirane prema njihovim antigenskim svojstvima.
Nova etapa u razvoju imunologije započela je 1953. godine istraživanjem engleskih znanstvenika Billinghama, Brenta, Medawara i češkog znanstvenika Haseka o reprodukciji tolerancije. Na temelju ideje koju je 1949. izrazio Burnet i dalje razvio u Jerneovoj hipotezi da sposobnost razlikovanja vlastitih i stranih antigena nije urođena, već se formira u embrionalnom i postnatalnom razdoblju, Medawar i njegovi kolege u ranim šezdesetima dobili su toleranciju za transplantaciju kože kod miševa. Tolerancija na transplantate kože donora javila se kod zrelih miševa ako su im ubrizgane limfoidne stanice donora tijekom embrionalnog razdoblja. Takvi primatelji, nakon što su postali spolno zreli, nisu odbacili transplantate kože od donora iste genetske linije. Za ovo otkriće Burnet i Medawar nagrađeni su 1960. godine Nobelova nagrada.
Nagli porast interesa za imunologiju povezan je sa stvaranjem klonske selekcijske teorije imuniteta 1959. godine od strane F. Burneta, istraživača koji je dao veliki doprinos razvoju imunologije. Prema ovoj teoriji, imunološki sustav nadzire postojanost staničnog sastava tijela i uništavanje mutiranih stanica. Burnetova teorija klonske selekcije bila je osnova za izgradnju novih hipoteza i pretpostavki.
U studijama L. A. Zilbera i njegovih kolega, provedenih 1951.-1956., stvorena je virusno-imunološka teorija nastanka raka, prema kojoj provirus integriran u genom stanice uzrokuje njezinu transformaciju u stanicu raka.
Godine 1959. proučavao je engleski znanstvenik R. Porter molekularna struktura antitijela i pokazao da se molekula gama globulina sastoji od dva laka i dva teška polipeptidna lanca povezana disulfidnim vezama.
Naknadno je razjašnjena molekularna struktura protutijela, utvrđen slijed aminokiselina u lakim i teškim lancima, imunoglobulini su podijeljeni u klase i podklase te su dobiveni važni podaci o njihovim fizikalno-kemijskim i biološkim svojstvima. Za istraživanje molekularne strukture protutijela R. Porter i američki znanstvenik D. Edelman dobili su 1972. Nobelovu nagradu.
A. Komza je još 30-ih godina otkrio da uklanjanje timusa dovodi do slabljenja imuniteta. No, pravi značaj ovog organa razjašnjen je nakon što je australski znanstvenik J. Miller 1961. godine izveo neonatalnu timektomiju kod miševa, nakon čega se razvio specifičan sindrom imunološke deficijencije, prvenstveno stanične imunosti. Brojna istraživanja pokazala su da je timus središnji organ imuniteta. Zanimanje za timus posebno je naglo poraslo nakon otkrića njegovih hormona, kao i T i B limfocita, 70-ih godina.
Godine 1945.-1955. Brojne su studije objavljene koje pokazuju da kada se pticama ukloni limfoepitelni organ koji se zove Fabriciusova burza, sposobnost stvaranja antitijela se smanjuje. Tako se pokazalo da postoje dva dijela imunološkog sustava - onaj ovisan o timusu, koji je odgovoran za stanične imunološke reakcije, i onaj ovisan o burzi, koji utječe na sintezu antitijela. J. Miller i engleski istraživač G. Claman prvi su 70-ih godina prošlog stoljeća pokazali da u imunološkim reakcijama stanice ova dva sustava stupaju u međusobnu kooperativnu interakciju. Proučavanje stanične suradnje jedno je od središnjih područja moderne imunologije.
A. Fagreus je 1948. godine utvrdio da antitijela sintetiziraju plazma stanice, a J. Gowens je 1959. godine prijenosom limfocita dokazao ulogu limfocita u imunološkom odgovoru.
Godine 1956. Jean Dosset i njegovi kolege otkrili su sustav antigena histokompatibilnosti HLA kod ljudi, što je omogućilo izvođenje tipizacije tkiva.
Mac Devwit je 1965. dokazao da geni imunološke reaktivnosti (Ir geni), o kojima ovisi sposobnost odgovora na strane antigene, pripadaju glavnom kompleksu histokompatibilnosti. Godine 1974. P. Zinkernagel i R. Dougherty pokazali su da su antigeni glavnog histokompatibilnog kompleksa predmet primarnog imunološkog prepoznavanja u reakcijama T limfocita na različite antigene.
Od velike važnosti za razumijevanje mehanizama regulacije aktivnosti imunokompetentnih stanica i njihove interakcije s pomoćnim stanicama bilo je otkriće D. Dumonda 1969. limfokina koje proizvode limfociti, te stvaranje teorije N. Ernea 1974. imunoregulacijske mreže “idiotip-anti-idiotip”.
Nove metode istraživanja bile su od velike važnosti za razvoj imunologije, uz dobivene temeljne podatke. Tu spadaju metode uzgoja limfocita (P. Nowell), kvantitativno određivanje stanica koje stvaraju antitijela (N. Erne, A. Nordin), stanica koje stvaraju kolonije (Mc Culloch), metode uzgoja limfoidnih stanica (T. Meikinodan) i otkrivanje receptora na membranama limfocita. Mogućnosti korištenja imunoloških metoda istraživanja i povećanja njihove osjetljivosti znatno su se povećale uvođenjem radioimunološke metode u praksu. Za razvoj ove metode američki je istraživač R. Yalow 1978. godine dobio Nobelovu nagradu.
Na razvoj imunologije, genetike i opće biologije uvelike je utjecala hipoteza koju su 1965. iznijeli W. Dreyer i J. Bennett da laki lanac imunoglobulina nije kodiran jednim, nego dvama različitim genima. Prije toga, općeprihvaćena hipoteza bila je ona F. Jacoba i J. Monoda, prema kojoj je sinteza svake proteinske molekule kodirana posebnim genom.
Razdoblje proučavanja subpopulacija limfocita i hormona timusa
Sljedeća faza u razvoju imunologije bilo je proučavanje subpopulacija limfocita i hormona timusa, koji imaju i stimulirajući i inhibicijski učinak na imunološki proces.
Tijekom posljednja dva desetljeća bilo je dokaza o postojanju matičnih stanica u koštanoj srži sposobnih transformirati se u imunokompetentne stanice.
Napredak imunologije u proteklih 20 godina potvrdio je Burnetovu ideju da je imunitet homeostatski fenomen i da je po svojoj prirodi prvenstveno usmjeren protiv mutantnih stanica i autoantigena koji se pojavljuju u tijelu, a antimikrobno djelovanje je privatna manifestacija imuniteta. Tako je infektivna imunologija, koja se dugo razvijala kao jedno od područja mikrobiologije, bila temelj za nastanak novog područja znanstveno znanje- neinfektivna imunologija.
Moderna imunologija
Glavni zadatak suvremene imunologije je identificirati biološke mehanizme imunogeneze na staničnoj i molekularnoj razini. Proučavaju se struktura i funkcije limfoidnih stanica, svojstva i priroda fizikalno-kemijskih procesa koji se odvijaju na njihovim membranama, u citoplazmi i organelama. Kao rezultat ovih istraživanja, danas se imunologija približila razumijevanju intimnih mehanizama prepoznavanja, sinteze protutijela, njihove strukture i funkcija. Značajan napredak postignut je u proučavanju receptora T-limfocita, stanične suradnje i mehanizama staničnih imunoloških reakcija.
Zaključak
immunology znanost hormone microbiology
Razvoj imunologije doveo je do izdvajanja niza samostalnih područja u njoj: opća imunologija, imunotolerancija, imunokemija, imunomorfologija, imunogenetika, imunologija tumora, transplantacijska imunologija, imunologija embriogeneze, autoimuni procesi, radioimuna imunologija, alergije, imunobiotehnologija, imunologija okoliša. itd.
Bibliografija
1. Vorobyov A.A. "Mikrobiologija". Udžbenik za studente medicine. Sveučilišta, 1994. (monografija).
2. Korotyaev A.I. „Medicinska mikrobiologija, virolozi
3. Pokrovski V.I. "Medicinska mikrobiologija, imunologija, virologija." Udžbenik za studente farmacije. Sveučilišta, 2002. (monografija).
4. Borisov L.B. "Medicinska mikrobiologija, virologija i imunologija." Udžbenik za studente medicine. Sveučilišta, 1994. (monografija).
Objavljeno na Allbest.ru
Slični dokumenti
Zadaci medicinske mikrobiologije, virologije, imunologije i bakteriologije. Povijest razvoja mikrobiologije na svjetskoj razini. Izum mikroskopa A. Leeuwenhoeka. Nastanak domaće bakteriologije i imunologije. Radovi domaćih mikrobiologa.
sažetak, dodan 16.04.2017
Mikroorganizmi kao važan faktor prirodni odabir u ljudskoj populaciji. Njihov utjecaj na kruženje tvari u prirodi, normalno postojanje i patologije biljaka, životinja i ljudi. Glavne faze u razvoju mikrobiologije, virologije, imunologije.
sažetak, dodan 21.01.2010
Sastav i djelovanje Zavoda za mikrobiologiju i imunologiju. Principi rada u mikrobiološkom laboratoriju. Priprema posuđa i alata. Tehnike uzorkovanja, inokulacije i pripreme hranjivih podloga. Metode identifikacije mikroorganizama.
izvješće o praksi, dodano 19.10.2015
Glavne vrste limfocita prema funkciji i morfološke karakteristike kao stanice imunološkog sustava i njegova ključna karika. Dezoksiribonukleaze sekretornih granula limfocita periferne krvi bolesnika s AAA. Metode izolacije i proučavanja limfocita.
kolegij, dodan 07.12.2013
Znanost koja proučava mikroorganizme, njihovu sistematiku, morfologiju, fiziologiju, nasljeđe i varijabilnost. Metode i ciljevi mikrobiologije, faze formiranja. Znanstvenici koji su dali značajan doprinos razvoju mikrobiologije, njeno praktično značenje i postignuća.
prezentacija, dodano 14.12.2017
Opće karakteristike B-limfocita. Obilježja subpopulacija, receptora i markera B-limfocita. Receptori za prepoznavanje antigena B stanica: opće karakteristike. Subpopulacije B-limfocita, prepoznavanje antigena imunoglobulinskim receptorima.
sažetak, dodan 02.10.2014
Imunološki sustav organizma i njegove funkcije. Vrste stanica imunološkog sustava (limfociti, fagociti, zrnati leukociti, mastociti, neke epitelne i retikularne stanice). Slezena je poput filtera krvi. Stanice ubojice kao moćno oružje imunološkog sustava.
prezentacija, dodano 13.12.2015
Vitalni i kreativni put Ilya Ilyich Mechnikov - izvanredan ruski biolog. Mečnikovljev doprinos razvoju imunologije. Fagocitna teorija imuniteta. Razvoj ideja I.I. Mečnikov u Rusiji i inozemstvu, njihova praktična primjena.
sažetak, dodan 25.05.2017
Definicija pojma "hormon". Upoznavanje s poviješću proučavanja endokrinih žlijezda i hormona, njihova kompilacija opća klasifikacija. Razmatranje specifičnosti biološkog djelovanja hormona. Opis uloge receptora u ovom procesu.
prezentacija, dodano 23.11.2015
Pojava mikrobiologije kao znanosti. Leeuwenhoek je otkrio mikroskop. Proučavanje prirode fermentacije. Zasluge R. Kocha u proučavanju mikroorganizama kao uzročnika zaraznih bolesti. Studija infekcije i imuniteta. Razvoj veterinarske mikrobiologije.
– određuje se udaljenost od referentne točke do specifičnih vrijednosti pokazatelja objekata koji se ocjenjuju.
U ovoj metodi, pokazatelj sveobuhvatne procjene uzima u obzir ne samo apsolutne vrijednosti uspoređivanih parcijalnih pokazatelja, već i njihovu blizinu najboljim vrijednostima.
Za izračun vrijednosti pokazatelja sveobuhvatne procjene poduzeća predlaže se sljedeća matematička analogija.
Svako poduzeće se smatra točkom u n-dimenzionalnom euklidskom prostoru; koordinate točke su vrijednosti pokazatelja po kojima se vrši usporedba. Uvodi se pojam standarda - poduzeća čiji svi pokazatelji imaju najbolje vrijednosti među datim skupom poduzeća. Kao standard možete uzeti i uvjetni objekt u kojem svi pokazatelji odgovaraju preporučenim ili standardnim vrijednostima. Što je poduzeće bliže standardnim pokazateljima, to je njegova udaljenost do standardne točke kraća i ocjena je viša. Najviša ocjena daje se poduzeću s minimalnom sveobuhvatnom vrijednošću procjene.
Za svako analizirano poduzeće vrijednost njegove ocjene rejtinga određena je formulom
gdje su x ij koordinate točaka matrice - standardizirani pokazatelji j-tog poduzeća, koji se određuju korelacijom stvarnih vrijednosti svakog pokazatelja s referencom prema formuli
X ij = a ij: a ij max
gdje je a ij max referentna vrijednost indikatora.
Potrebno je obratiti pozornost na valjanost udaljenosti između vrijednosti pokazatelja određenog predmeta proučavanja i standarda. Pojedini aspekti djelatnosti različito utječu na financijsko stanje i učinkovitost proizvodnje. U takvim uvjetima uvode se težinski koeficijenti; pridaju važnost određenim pokazateljima. Da biste dobili sveobuhvatnu procjenu uzimajući u obzir težinske koeficijente, koristite formulu
gdje su k 1 ... k n težinski koeficijenti pokazatelja utvrđeni stručnim procjenama.
Na temelju ove formule, vrijednosti koordinata se kvadriraju i množe s odgovarajućim težinskim koeficijentima; zbrajanje se vrši po stupcima matrice. Rezultirajući subradikalni zbrojevi raspoređeni su silaznim redoslijedom. U ovom slučaju, ocjena se utvrđuje maksimalnom udaljenošću od ishodišta koordinata, a ne minimalnim odstupanjem od referentnog poduzeća. Najveću ocjenu dobiva poduzeće koje ima najveće ukupne rezultate po svim pokazateljima.
1. Rezultati financijskih i gospodarskih aktivnosti iskazuju se u obliku početne matrice u kojoj su istaknute referentne (najbolje) vrijednosti pokazatelja.
2. Matrica se sastavlja sa standardiziranim koeficijentima, izračunatim dijeljenjem svakog stvarnog pokazatelja s maksimalnim (referentnim) koeficijentom. Referentne vrijednosti indikatora jednake su jedinici.
3. Sastavlja se nova matrica, gdje se za svako poduzeće izračunava udaljenost od koeficijenta do referentne točke. Dobivene vrijednosti sažete su za svako poduzeće.
4. Poduzeća su rangirana silaznim redoslijedom ocjenjivanja. Najvišu ocjenu ima tvrtka s minimalnom ocjenom.
PLAN
1. Definicija pojma "imunitet".
2. Povijest razvoja imunologije.
3. Vrste i oblici imuniteta.
4. Mehanizmi nespecifične rezistencije i njihove karakteristike.
5. Antigeni kao induktori stečenog antimikrobnog djelovanja
imunitet, njihovu prirodu i svojstva.
6. Antigeni mikroorganizama i životinja.
1. Definicija pojma "imunitet".
Imunitet je skup zaštitno-adaptivnih reakcija i prilagodbi usmjerenih na održavanje postojanosti unutarnje okoline (homeostaze) i zaštitu organizma od infektivnih i drugih genetski stranih agenasa.
Imunitet je biološki fenomen koji je univerzalan za sve organske oblike materije, višekomponentan i raznolik u svojim mehanizmima i manifestacijama.
Riječ "imunitet" dolazi od latinske riječi " imunitas"– imunitet.
Povijesno gledano, usko je povezan s konceptom imuniteta na patogene zaraznih bolesti, jer doktrina imuniteta (imunologija) - rođena je i formirana krajem 19. stoljeća u dubinama mikrobiologije, zahvaljujući istraživanjima Louisa Pasteura, Ilya Ilyich Mechnikov, Paul Ehrlich i drugih znanstvenika.
Uvod. Glavne faze razvoja imunologije.
Imunologija je znanost o građi i funkciji imunološkog sustava životinja, uključujući ljude i biljke, odnosno znanost o obrascima imunološke reaktivnosti organizama i metodama korištenja imunoloških fenomena u dijagnostici terapije i prevenciji zaraznih i imunoloških bolesti.
Imunologija je nastala kao dio mikrobiologije kao rezultat praktične primjene potonje u liječenju zaraznih bolesti. Stoga se prva razvila infektivna imunologija.
Od svog nastanka, imunologija je bila u bliskoj interakciji s drugim znanostima: genetikom, fiziologijom, biokemijom, citologijom. Krajem 20. stoljeća postaje samostalna funkcionalna biološka znanost.
U razvoju imunologije može se razlikovati nekoliko faza:
Zarazna(L. Pasteur i dr.), kada je počelo proučavanje imuniteta na infekcije. Neinfektivno, nakon otkrića krvnih grupa K. Landsteinera i
fenomen anafilaksije C. Richeta i P. Portiera.
Stanično-humoralni, koji je povezan s otkrićima dobitnika Nobelove nagrade:
I. I. Mečnikov - razvio je staničnu teoriju imunosti (fagocitoza), P. Ehrlich - razvio humoralnu teoriju imunosti (1908.).
F. Burnet i N. Ierne - stvorili modernu klonsko-selektivnu teoriju imunosti (1960.).
P. Medawar - otkrio imunološku prirodu odbacivanja alografta (1960).
Molekularna genetika, karakteriziraju izvanredna otkrića koja su nagrađena Nobelovom nagradom:
R. Porter i D. Edelman - dešifrirali strukturu protutijela (1972.).
Ts. Melstein i G. Koehler razvili su metodu za proizvodnju monoklonskih protutijela na temelju hibrida koje su stvorili (1984.).
S. Tonegawa - otkrio je genetske mehanizme somatske rekombinacije imunoglobulinskih gena kao osnovu za stvaranje raznolikosti receptora za prepoznavanje antigena limfocita (1987.).
R. Zinkernagel i P. Dougherty - otkrili su ulogu MHC (major histocompatibility complex) molekula (1996).
Jean Dosset i njegovi kolege otkrili su sustav ljudskih antigena i leukocita (antigeni histokompatibilnosti) - HLA, što je omogućilo tipizaciju tkiva (1980.).
Značajan doprinos razvoju imunologije dali su ruski znanstvenici: I. I. Mečnikov (teorija fagocitoze), N. F. Gamaleya (cjepiva i imunitet), A. A. Bogomolets (imunitet i alergije), V. I. Ioffe (antiinfektivni imunitet) , P. M. Kosjakov i E. A. Zotikov (izoserologija i izoantigeni), A. D. Ado i I. S. Gushchin (alergija i alergijske bolesti),
R. V. Petrov i R. M. Khaltov (imunogenetika, interakcija stanica, umjetni antigeni i cjepiva, novi imunomodulatori), A. A. Vorobyov (toksoidi i imunitet tijekom infekcija), B. F. Semenov (antiinfektivni imunitet), L V. Kovalchuk, B. V. Pinechin, A. N. Cheredeev ( procjena imunološkog statusa), N. V. Medunicin (cjepiva i citotoksini), V. Ya. Arlon, A. A. Yarilin (hormoni i funkcija timusa) i mnogi drugi.
U Bjelorusiji je 1974. godine D. K. Novikov obranio prvu doktorsku disertaciju iz imunologije, “Reakcije transplantacijske imunosti in vivo i in vitro u različitim imunogenetskim sustavima”.
Bjeloruski znanstvenici daju određeni doprinos razvoju imunologije: I. I. Generalov (abzimi i njihov klinički značaj), N. N. Voitenyuk (citokini), E. A. Dotsenko (ekologija, bronhijalna astma), V. M. Kozin (imunopatologija i imunoterapija psorijaze), D. K. Novikov ( imunodeficijencije i alergije), V. I. Novikova (imunoterapija i procjena imunološkog statusa u djece), N. A. Skepyan (alergijske bolesti), L. P. Titov (patologija sustava komplementa) , M. P. Potaknev (citokini i patologija), S. V. Fedorovich (profesionalne alergije).
DRŽAVNO SVEUČILIŠTE PENZA
Odjel "Mikrobiologija, epidemiologija i zarazne bolesti"
Disciplina : Medicinska mikrobiologija
Predavanje
Tema predavanja: UVOD U IMUNOLOGIJU. VRSTE IMUNITETA. NESPECIFIČNI ZAŠTITNI ČIMBENICI
Cilj:
Upoznati vrste i oblike imuniteta, proučiti nespecifične čimbenike obrane organizma.
Plan:
Pitanja za pregled:
- Opišite faze razvoja imunologije.
- Koje oblike i vrste imuniteta poznajete?
- Koje nespecifične čimbenike obrane organizma poznajete?
- Opišite sustav komplementa.
Literatura za pripremu:
Vorobyov A.A., Bykov A.S., Pashkov E.P., Rybakova A. M . Mikrobiologija (udžbenik).- M: Medicina, 1998.
Medicinska mikrobiologija (Priručnik) ur. V. I. Pokrovski, D. K. Pozdejev. - M: GOETAR, “Medicina”, 1999.
Mikrobiologija s virologijom i imunologijom / Urednici L.B. Borisov, A.M. Smirnova.-M., 1994.
Mikrobiologija i imunologija / Uredio A.A. Vorobyov. - M., 1999.
Vodič za laboratorijsku nastavu iz mikrobiologije / Ed. L. B. Borisova - M., 1984.
Virologija. U 3 sv./ Priredili B. Filsts, D. Knipe.- M, 1989.
Mesroveanu L., Punescu E. Fiziologija bakterija - Bukurešt: Izdavačka kuća Akademije znanosti RPRD960.
Virusne, klamidijske i mikoplazmatske bolesti. V. I. Kozlova i drugi - M.: “Avicena”, 1995.
Predavač Mitrofanova N.N.
1. Priče o razvoju imunologije
Imunologija (od lat. immunity imunost, nepovredivost, logos znanost) znanost koja proučava metode i mehanizme zaštite organizma od genetski stranih tvari radi održavanja homeostaze.
U slučaju poremećaja homeostaze razvijaju se zarazne bolesti, autoimune reakcije i onkološki procesi.
Glavna funkcija imunološkog sustava je prepoznavanje i uništavanje stranih, genetski modificiranih stanica koje su prodrle izvana ili nastale u samom tijelu.
Razvoj imunologije kao znanosti može se podijeliti u tri faze.
1. Prva faza (protoimunologija) povezana je s empirijskim razvojem infektivne imunologije
2. Druga faza je završetak formiranja klasične imunologije, proširenje temeljnih principa imunosti na neinfektivne procese (transplantacijska i antitumorska imunost) i stvaranje jedinstvene opće biološke teorije imunosti.
3. Treći stupanj molekularne genetike - (od sredine 20. stoljeća) razvoj molekularne i stanične imunologije, imunogenetike.
Podrijetlo doktrine imuniteta seže u davna vremena i povezano je s opažanjem da se mnoge, osobito dječje bolesti, poput ospica, vodenih kozica, zaušnjaka itd., ne ponavljaju. U tom razdoblju počinju se koristiti metode variolacije za stvaranje imuniteta. Nakon što je engleski seoski liječnik E. Jenner uveo novu metodu zaštite od velikih boginja, javlja se metoda cijepljenja. E. Jenner se ponekad naziva "rodonačelnikom" imunologije.
Međutim, nakon što je primio cjepivo za zaštitu od velikih boginja, nije formulirao opća načela za stvaranje imuniteta protiv bilo koje druge infekcije.
Razvoj imunologije započeo je radovima istaknutog francuskog znanstvenika L. Pasteura (1881.). On i njegovi studenti pronašli su metode za slabljenje (atenuaciju) virulentnih svojstava mikroorganizama, stvorili cjepiva uz njihovu pomoć i objasnili mehanizam stvaranja imuniteta pri primjeni cjepiva. I. I. Mečnikov (1882) otkrio je fenomen fagocitoze i formulirao staničnu (fagocitnu) teoriju imunosti. Istodobno su francuski istraživači E. Roux i A. Yersin (1888.) utvrdili sposobnost uzročnika difterije da izlučuje poseban toksin, za čiju su neutralizaciju razvili njemački znanstvenik E. Behring i japanski istraživač S. Kitazato (1890.). metoda za proizvodnju antitoksičnog imunološkog seruma protiv difterije. U Rusiji je takav serum pripremio G. N. Gabrichevsky (1894.). Dobiveni su antitoksični serumi za liječenje botulizma, plinske anaerobne infekcije i dr. Nastala je humoralna teorija imuniteta čiji je začetnik njemački istraživač P. Ehrlich.
Započelo je razdoblje aktivne specifične prevencije zaraznih bolesti. Od oslabljenih živih mikroorganizama dobivena su nova cjepiva za prevenciju tuberkuloze (1919.), kuge (1931.), žute groznice (1936.), tularemije (1939.), dječje paralize (1954.) itd. Razvijena je metoda za pripravu toksoida, koji su se koristili za prevenciju difterije i tetanusa. Uvedene su nove metode dijagnosticiranja zaraznih bolesti koje se temelje na interakciji antigena protutijela.
U 40-im godinama 20. stoljeća počeo se razvijati novi smjer u imunologiji vezan uz transplantaciju organa i tkiva. To se zove transplantacijski imunitet. Njegovo proučavanje započelo je radom J. Bordeta i N. Ya. Chistovicha (kolege I. I. Mečnikova), koji su ustanovili da strana crvena krvna zrnca i serum stimuliraju stvaranje antitijela. K. Landsteiner (1900) otkrio je krvne grupe i razvio teoriju tkivnih izoantigena.
Engleski znanstvenik P. Medovar (1945.) iznio je postavku da imunitet štiti ne samo od mikroorganizama, već i od stanica ili tkiva genetski stranog organizma. Jasno je rečeno da je proces odbacivanja presađenog stranog tkiva posljedica imunoloških mehanizama. Pojavile su se nove ideje o malignim novotvorinama, specifičnim tumorskim antigenima [Zilber L.A., 1944.], antitumorskom imunitetu, novim metodama liječenja tumora i alergija.
P. Medovar i sur. (1953.) i češki istraživač M. Hasek (1960.), proučavajući transplantacijski imunitet, neovisno o sebi otkrili su fenomen imunološke tolerancije kao manifestacije tolerancije na strano, genetski različito od “vlastitog”. Australski znanstvenik F.M. Burnet i suradnici (1949.) otkrili su da se tolerancija može inducirati umjetno uvođenjem stranog antigena u životinju prije rođenja. Za to su učenje P. Medovar i M. Burnet dobili titulu laureata Nobelove nagrade.
Obrasci nasljeđivanja antigenske specifičnosti, genetička kontrola imunološkog odgovora, genetski aspekti nekompatibilnosti tkiva tijekom transplantacije i problemi homeostaze somatskih stanica makroorganizma proučava nova grana imunologije - imunogenetika.
Razvoj imunologije se nastavlja, au sadašnjoj fazi proučava se organizacija imunološkog sustava, uloga timusa u formiranju staničnih populacija (T- i B-limfocita), mehanizmi njihovog funkcioniranja, kooperativni odnosi između identificirane su glavne stanice imunološkog sustava, utvrđena je struktura protutijela (D. Edelman, R Porter).
Otkriveni su novi fenomeni stanične imunosti (citopatogeni učinci, alogena inhibicija, fenomen blast transformacije itd.).
Stvorena je doktrina preosjetljivosti i imunodeficijencije.
Proučavani su oblici imunološkog odgovora i čimbenici nespecifične zaštite.
Razvijene su teorije o imunitetu.
Stvaranje jedinstvene općebiološke teorije imuniteta otvorilo je put njegovoj uporabi u borbi za zdravu dugovječnost, uzimajući kao temelj moćne Prirodni resursi ustavna zaštita u borbi protiv zaraznih i mnogih drugih bolesti ljudi i životinja.
2. Čimbenici i mehanizmi imunosti
Imunitet (od latinskog immunitas nepovrediv, zaštićen, oslobođenje, oslobađanje od bolesti) je sustav biološke zaštite unutarnjeg okoliša višestaničnog organizma (homeostaze) od genetski stranih tvari egzogene i endogene prirode.
Ovaj sustav osigurava strukturnu i funkcionalnu cjelovitost organizama određene vrste tijekom njihova života. Genetski strane tvari („ne naše“) ulaze u tijelo izvana u obliku patogenih mikroorganizama i helminta, njihovih toksina, proteina i drugih komponenti, ponekad u obliku presađenih tkiva ili organa. Zastarjele, mutirane ili oštećene stanice vlastitog tijela mogu postati "strane".
Funkcije obrambenog sustava, koji se naziva imunološki sustav, su prepoznavanje takvih stranih agenasa i specifičan odgovor na njih.
2.1. Vrste i oblici imuniteta
Imunost je višekomponentna pojava i raznolika u svojim mehanizmima i manifestacijama, a poznata su dva glavna obrambena mehanizma.
Prvi je posljedica djelovanja urođenih, konstitutivnih čimbenika nespecifične rezistencije (od lat. r otpornost na esistentia) i kontrolirana je genetskim mehanizmima (urođena, imunitet vrste). Oni pružaju neselektivan odgovor u odnosu na stranog agenta. To znači da svojstva takvog sredstva nisu bitna. Primjerice, ljudi su imuni na uzročnike pseće kuge i kokošje kolere, a životinje su neosjetljive na šigele, gonokoke i druge mikroorganizme patogene za ljude.
Drugi je određen zaštitnim mehanizmima koji se javljaju uz sudjelovanje limfnog sustava. Oni su temelj formiranja individualne adaptivne (stečene) imunosti stečene tijekom života. Takvu imunost karakterizira razvoj specifičnih reakcija imunološkog sustava na specifično strano sredstvo (tj. inducibilna je) u obliku stvaranja imunoglobulina ili senzibiliziranih limfocita. Ovi čimbenici imaju visoku aktivnost i specifičnost djelovanja.
Ovisno o načinu formiranja, razlikuje se nekoliko oblika stečene individualne imunosti.
Stečena imunost može nastati kao posljedica zarazne bolesti i tada se naziva prirodna aktivna (postinfektivna). Traje od nekoliko tjedana i mjeseci (nakon dizenterije, gonoreje i dr.) do nekoliko godina (nakon ospica, difterije i dr.). Ponekad se može pojaviti kao posljedica latentne infekcije ili prijevoza (na primjer, kroz "kućansku" imunizaciju za meningokoknu infekciju). Postoje vrste stečenog imuniteta:
Antimikrobno se proizvodi nakon bakterijske infekcije (kuga, trbušni tifus, itd.);
Antitoksičan nastaje kao posljedica toksične infekcije (tetanus, botulizam, difterija, itd.);
Antivirusno nakon virusnih infekcija (ospice, zaušnjaci, dječja paraliza, itd.);
Antiprotozoa nakon infekcija uzrokovanih protozoama;
Antimikotik nakon gljivičnih oboljenja.
U nekim slučajevima, nakon zarazne bolesti, potpuno oslobođenje makroorganizam od patogena. Takav imunitet nazivamo sterilnim. Imunitet kod kojeg uzročnici neograničeno dugo opstaju u tijelu klinički zdravih osoba koje su preboljele naziva se nesterilnim.
Stečena imunost prenosi se s majke na dijete kroz placentu tijekom razvoja fetusa, a osiguravaju je imunoglobulini. Naziva se prirodnim pasivnim (transplacentalnim). Njegovo trajanje je 3-4 mjeseca, ali se može produžiti kada su djeca dojena, budući da se antitijela nalaze i u majčinom mlijeku. Značaj takvog imuniteta je velik. Osigurava imunitet dojenčadi na zarazne bolesti.
Stečena umjetna imunost nastaje kao rezultat imunizacije. Postoje aktivni i pasivni oblik umjetni imunitet. Aktivna umjetna imunost nastaje nakon unošenja u organizam oslabljenih ili ubijenih mikroorganizama ili njihovih neutraliziranih otrova. Istodobno, u tijelu toplokrvnih životinja dolazi do aktivnog restrukturiranja, usmjerenog na stvaranje tvari koje imaju štetan učinak na patogene i njegove toksine; dolazi do promjene u svojstvima stanica koje uništavaju mikroorganizme i njihov metabolizam. proizvoda. Trajanje ovog imuniteta je od 1 godine do 3×7 godina.
Pasivna umjetna imunost nastaje kada se u organizam unesu gotova protutijela koja se nalaze u serumima životinja posebno imuniziranih određenim vrstama uzročnika (imuni serumi) ili su dobivena iz seruma ozdravljenih ljudi (imunoglobulini). Ova vrsta imuniteta javlja se odmah nakon unošenja antitijela, ali traje samo 15-20 dana, zatim se antitijela uništavaju i izlučuju iz organizma.
2.2. Čimbenici nespecifične rezistencije
Čimbenici nespecifične otpornosti (zaštite), koji osiguravaju neselektivni odgovor na antigen i najstabilniji su oblik imuniteta, određeni su urođenim biološkim karakteristikama vrste. Na stranog agenta reagiraju stereotipno i bez obzira na njegovu prirodu. Glavni mehanizmi nespecifične obrane formiraju se pod kontrolom genoma tijekom razvoja organizma i povezani su s prirodnim fiziološkim reakcijama širokog spektra - mehaničkim, kemijskim i biološkim.
Među čimbenicima nespecifične rezistencije su:
reaktivnost stanica domaćinana patogene mikroorganizme i toksine, određene genotipom i povezane s odsutnošću receptora za adheziju patogenog agensa na površini takvih stanica;
funkciju barijere kože i sluznice, što je osigurano odbacivanjem epitelnih stanica kože i aktivnim pokretima trepetljika trepljastog epitela sluznica. Osim toga, uzrokuje ga oslobađanje egzokreta iz znojnih i lojnih žlijezda kože, specifičnih inhibitora, lizozima, kiselog okoliša želučanog sadržaja i drugih agenasa. Biološki faktori zaštita na ovoj razini je zbog štetnog djelovanja normalne mikroflore kože i sluznice na patogene mikroorganizme;
temperaturna reakcija,koji zaustavlja razmnožavanje većine patogenih bakterija. Na primjer, otpornost pilića na patogen antraksa (B. anthracis) je zbog činjenice da je njihova tjelesna temperatura unutar 4142 ° C, pri kojoj bakterije nisu sposobne za samoreprodukciju;
stanični i humoralni čimbenici tijela.
Kada uzročnici uđu u tijelo, aktiviraju se humoralni čimbenici koji uključuju proteine sustava komplementa, properdin, lizine, fibronektin i sustav citokina (interleukini, interferoni i dr.). Vaskularne reakcije razvijaju se u obliku brzog lokalnog edema na mjestu ozljede, koji hvata mikroorganizme i ne dopušta im da uđu u unutarnje okruženje. U krvi se pojavljuju proteini akutne faze: C-reaktivni protein i lektin koji veže manan, koji imaju sposobnost interakcije s bakterijama i drugim patogenima. U ovom slučaju, njihovo hvatanje i apsorpcija od strane fagocitnih stanica je pojačano, tj. Dolazi do opsonizacije patogena, a ti humoralni čimbenici igraju ulogu opsonina.
Stanični čimbenici nespecifične zaštite uključuju mastocite, leukocite, makrofage, stanice prirodne ubojice (NK stanice, od engleskog “natural killer”).
Mastociti su velike stanice tkiva koje sadrže citoplazmatske granule koje sadrže heparin i biološki djelatne tvari kao što su histamin, serotonin. Tijekom degranulacije mastociti oslobađaju posebne tvari koje su posrednici upalnih procesa (leukotrieni i niz citokina). Medijatori povećavaju propusnost vaskularnih stijenki, što omogućuje ulazak komplementa i stanica u tkivo lezije. Sve to inhibira prodiranje patogena u unutarnje okruženje tijela. NK stanice su veliki limfociti koji nemaju T- ili B-stanične markere i sposobni su spontano ubiti tumorske i virusom zaražene stanice bez prethodnog kontakta. U perifernoj krvi oni čine do 10% svih mononuklearnih stanica. NK stanice su lokalizirane uglavnom u jetri, crvenoj pulpi slezene i sluznicama.
Leukociti sadrže snažne baktericidne čimbenike i osiguravaju primarnu ili preimunu fagocitozu mikrobnih stanica. Takvi leukociti nazivaju se fagociti (fagocitne stanice). Predstavljaju ih monociti, polimorfonuklearni neutrofili i makrofagi.
Fagocitoza biološki fenomen koji se temelji na prepoznavanju, hvatanju, apsorpciji i obradi stranih tvari od strane eukariotske stanice. Objekti za fagocitozu su mikroorganizmi, vlastite umiruće stanice organizma, sintetičke čestice itd. Fagociti su polimorfonuklearni leukociti (neutrofili, eozinofili, bazofili), monociti i fiksni makrofagi alveolarne, peritonealne, Kupfferove stanice, dendritične stanice slezene i limfnih čvorova, stanice Langerhans et al.
U procesu fagocitoze (od grčkog phago proždire, cytos stanice) postoji nekoliko faza (Sl. 15.1):
Približavanje fagocita stranom korpuskularnom objektu (stanici);
Adsorpcija predmeta na površini fagocita;
Apsorpcija objekta;
Uništavanje fagocitiranog objekta.
Prva faza fagocitoze odvija se zahvaljujući pozitivnoj kemotaksiji.
Adsorpcija se događa vezanjem stranog tijela na receptore fagocita.
Treća faza se provodi na sljedeći način.
Fagocit obavija svoju vanjsku membranu oko adsorbiranog objekta i uvlači ga (invaginira) u stanicu. Ovdje nastaje fagosom, koji se potom stapa s lizosomima fagocita. Nastaje fagolizosom. Lizosomi su specifične granule koje sadrže baktericidne enzime (lizozim, kisele hidrolaze itd.).
U stvaranju aktivnih slobodnih radikala O sudjeluju posebni enzimi 2 i H202.
U završnoj fazi fagocitoze dolazi do razgradnje apsorbiranih predmeta u spojeve male molekularne težine.
Ta se fagocitoza odvija bez sudjelovanja specifičnih humoralnih obrambenih čimbenika i naziva se preimuna (primarna) fagocitoza. Upravo je ovu varijantu fagocitoze prvi opisao I. I. Mechnikov (1883) kao faktor nespecifične obrane tijela.
Rezultat fagocitoze je ili smrt stranih stanica (završena fagocitoza) ili preživljavanje i razmnožavanje zarobljenih stanica (nepotpuna fagocitoza). Nepotpuna fagocitoza jedan je od mehanizama dugotrajne perzistencije (preživljavanja) patogenih uzročnika u makroorganizmu i kronizacije infektivnih procesa. Takva se fagocitoza najčešće događa u neutrofilima i završava njihovom smrću. Nepotpuna fagocitoza otkrivena je kod tuberkuloze, bruceloze, gonoreje, jersinioze i drugih infektivnih procesa.
Povećanje brzine i učinkovitosti fagocitne reakcije moguće je uz sudjelovanje nespecifičnih i specifičnih humoralnih proteina, koji se nazivaju opsonini. Tu spadaju proteini sustava komplementa S3 b i C4 b , proteini akutne faze, IgG, IgM itd. Opsonini imaju kemijski afinitet za neke komponente stanične stijenke mikroorganizama, vežu se na njih, a zatim se takvi kompleksi lako fagocitiraju jer fagociti imaju posebne receptore za molekule opsonina. Suradnja različitih opsonina krvnog seruma i fagocita čini opsonofagocitni sustav tijela. Procjena opsonske aktivnosti krvnog seruma provodi se određivanjem opsoničnog indeksa ili opsonofagocitnog indeksa, koji karakteriziraju učinak opsonina na apsorpciju ili lizu mikroorganizama od strane fagocita. Fagocitoza, u kojoj sudjeluju specifični (IgG, IgM) proteini opsonin, naziva se imunološkom.
Sustav komplementa(lat. complementum dodatak, sredstvo za nadopunjavanje) to je skupina proteina krvnog seruma koji sudjeluju u nespecifičnim obrambenim reakcijama: staničnoj lizi, kemotaksi, fagocitozi, aktivaciji mastocita itd. Komplementni proteini pripadaju globulinima ili glikoproteinima. Proizvode ih makrofagi, leukociti, hepatociti i čine 5x10% svih proteina krvi.
Sustav komplementa predstavlja 20 x 26 proteina krvnog seruma, koji cirkuliraju u obliku zasebnih frakcija (kompleksa), razlikuju se po fizikalno-kemijskim svojstvima i označavaju se simbolima C1, C2, C3 ... C9, itd. Svojstva i funkcija 9 glavnih komponenti komplementa dobro je proučena.
Sve komponente cirkuliraju u krvi u neaktivnom obliku, u obliku koenzima. Aktivaciju proteina komplementa (tj. sklapanje frakcija u jednu cjelinu) provode specifični imunološki i nespecifični čimbenici u procesu višestupanjskih transformacija. U ovom slučaju svaka komponenta komplementa katalizira aktivnost sljedeće. Time se osigurava redoslijed i kaskada ulaska komponenti komplementa u reakcije.
Proteini sustava komplementa sudjeluju u aktivaciji leukocita, razvoju upalnih procesa, lizi ciljnih stanica i, pričvršćivanjem na površinu staničnih membrana bakterija, sposobni su ih opsonizirati ("odjenuti"), potičući fagocitozu.
Postoje 3 poznata puta za aktivaciju sustava komplementa: alternativni, klasični i lektinski.
Najvažnija komponenta komplementa je S3, koji se cijepa konvertazom, formiranom tijekom bilo kojeg puta aktivacije, na fragmente S3 i S3 b. Ulomak SZ b sudjeluje u stvaranju C5 konvertaze. Ovo je početna faza formiranja membransko-litičkog kompleksa.
U alternativnom putu, komplement mogu aktivirati polisaharidi, bakterijski lipopolisaharidi, virusi i drugi antigeni bez sudjelovanja protutijela. Inicijator procesa je komponenta SZ b , koji se veže na površinske molekule mikroorganizama. Zatim, uz sudjelovanje niza enzima i proteina properdina, ovaj kompleks aktivira C5 komponentu koja se pričvršćuje na membranu ciljne stanice. Zatim se na njemu od komponenti C6 x C9 stvara membranski napadni kompleks (MAC). Proces završava perforacijom membrane i lizom mikrobnih stanica. Upravo se taj put pokretanja kaskade komplementarnih proteina odvija u ranim fazama infektivnog procesa, kada još nisu razvijeni specifični čimbenici imuniteta (antitijela). Osim toga, komponenta SZ b , vezanjem na površinu bakterija, može djelovati kao opsonin, pojačavajući fagocitozu.
Klasični put aktivacije komplementa započinje i odvija se uz sudjelovanje kompleksa antigen-antitijelo. Molekule IgM i neke frakcije IgG u kompleksu antigen-antitijelo imaju posebna mjesta koja su sposobna vezati komponentu komplementa C1. Molekula C1 sastoji se od 8 podjedinica od kojih je jedna aktivna proteaza. Sudjeluje u cijepanju komponenti C2 i C4 uz stvaranje C3-konvertaze klasičnog puta, koja aktivira komponentu C5 i osigurava stvaranje membranskog napadačkog kompleksa C6xC9, kao i u alternativnom putu.
Lektinski put aktivacije komplementa uzrokovan je prisutnošću u krvi posebnog proteina koji veže šećer ovisnog o kalciju, lektina koji veže manan (MBL). Ovaj protein je sposoban vezati ostatke manoze na površini mikrobnih stanica, što dovodi do aktivacije proteaze koja cijepa komponente C2 i C4. To izaziva stvaranje kompleksa koji razlaže membranu, kao u klasičnom putu aktivacije komplementa. Neki istraživači ovaj put smatraju varijantom klasičnog puta.
U procesu cijepanja komponenti C5 i C3 nastaju mali fragmenti C5a i C3a koji služe kao posrednici upalnog odgovora i iniciraju razvoj anafilaktičkih reakcija uz sudjelovanje mastocita, neutrofila i monocita. Ove komponente se nazivaju anafilatoksini komplementa.
Aktivnost komplementa i koncentracija njegovih pojedinih komponenti u ljudskom tijelu može se povećati ili smanjiti u različitim patološkim stanjima. Mogu postojati i nasljedni nedostaci. Sadržaj komplementa u životinjskom serumu ovisi o vrsti, dobi, godišnjem dobu pa čak i dobu dana.
Najviša i najstabilnija razina komplementa uočena je kod zamoraca, stoga se kao izvor komplementa koristi nativni ili liofilizirani krvni serum ovih životinja. Proteini sustava komplementa vrlo su labilni. Brzo se kvare kada se čuvaju na sobnoj temperaturi, izlažu svjetlu, ultraljubičastim zrakama, proteazama, otopinama kiselina ili lužina te uklanjanju iona Ca++ i Mg++. Zagrijavanje seruma na 56 °C tijekom 30 minuta dovodi do razaranja komplementa, pa se takav serum naziva inaktiviranim.
Određuje se kvantitativni sadržaj komponenata komplementa u perifernoj krvi kao jedan od pokazatelja aktivnosti humoralne imunosti. Kod zdravih osoba sadržaj komponente C1 je 180 µg/ml, C2 20 µg/ml, C4 - 600 µg/ml, S3 - 13 001 µg/ml.
Upala, kao najvažnija manifestacija imuniteta, razvija se kao odgovor na oštećenje tkiva (prije svega pokrovnog) i usmjerena je na lokalizaciju i uništavanje mikroorganizama koji su ušli u tijelo. Upalna reakcija temelji se na kompleksu humoralnih i staničnih čimbenika nespecifične rezistencije. Klinički se upala očituje crvenilom, otokom, boli, lokalnim povišenjem temperature, poremećajem funkcije oštećenog organa ili tkiva.
Središnju ulogu u razvoju upale imaju vaskularne reakcije i stanice mononuklearnog fagocitnog sustava: neutrofili, bazofili, eozinofili, monociti, makrofagi i mastociti. Pri oštećenju stanica i tkiva, osim toga, oslobađaju se razni medijatori: histamin, serotonin, prostaglandini i leukotrieni, kinini, proteini akutne faze, uključujući C-reaktivni protein i dr., koji igraju važnu ulogu u razvoju upalnih reakcija.
Bakterije koje su ušle u organizam tijekom oštećenja i njihovi produkti metabolizma aktiviraju sustav zgrušavanja krvi, sustav komplementa i stanice makrofagno-mononuklearnog sustava. Nastaju krvni ugrušci, što sprječava širenje uzročnika kroz krv i limfu i sprječava generalizaciju procesa. Kada se aktivira sustav komplementa, nastaje membranski napadajući kompleks (MAC) koji lizira mikroorganizme ili ih opsonizira. Potonji pojačava sposobnost fagocitnih stanica da apsorbiraju i probave mikroorganizme.
Priroda tijeka i ishod upalnog procesa ovisi o mnogim čimbenicima: prirodi i intenzitetu djelovanja stranog agensa, obliku upalnog procesa (alterativni, eksudativni, proliferativni), njegovoj lokalizaciji, stanju imunološkog sustava. sustava itd. Ako upala ne prestane kroz nekoliko dana postaje kronična i tada nastaje imunološka upala u kojoj sudjeluju makrofagi i T-limfociti.
Imunologija je znanost o specifičnim reakcijama tijela na unošenje tvari i struktura stranih tijelu. Imunologija se u početku smatrala znanošću o imunosti organizma na bakterijske infekcije, a od svog nastanka imunologija se razvijala kao primijenjeno područje drugih znanosti (fiziologije čovjeka i životinja, medicine, mikrobiologije, onkologije, citologije).
U proteklih 40 godina imunologija je postala samostalna fundamentalna biološka znanost.
Povijest razvoja .
Prva faza razvoja: prvi podaci u 5. st. pr. e. U davna vremena čovječanstvo je bilo bespomoćno protiv zaraznih bolesti (kuga, boginje). Epidemije su odnijele mnoge živote. Prva imunološka opažanja odnose se na drevna grčka. Grci su primijetili da ljudi koji su imali boginje nisu osjetljivi na ponovnu infekciju. U drevna Kina Uzimali su kraste boginja, samljeli ih i davali namirisati. Ovu metodu koristili su Perzijanci i Turci i zvali su je metoda varijacije. Rasprostranjen je i u Europi.
U 18. stoljeću u Engleskoj je primijećeno da mljekarice koje su opsluživale bolesne krave rijetko obolijevaju od boginja. Na temelju toga Jeher je 1796. razvio sigurnu metodu prevencije velikih boginja cijepljenjem osobe kravljim boginjama. Ova metoda je dodatno poboljšana: virusu velikih boginja dodan je virus kravljih boginja. Zahvaljujući potpunoj procijepljenosti stanovništva, velike boginje su iskorijenjene. Međutim, nastanak imunologije kao znanosti seže u rane 80-e godine 19. stoljeća i povezuje se s Pasteurovim otkrićem mikroorganizmi, patogeni. Proučavajući vodene kozice Pasteur je došao do zaključka da mikrobi gube sposobnost izazivanja smrti životinja zbog promjena bioloških svojstava te je predložio mogućnost sprječavanja zaraznih bolesti oslabljenim mikrobima velikih boginja.
Godine 1884. Mečnikov je formulirao teorija fagocitoze. To je bila prva eksperimentalno potkrijepljena teorija imuniteta. Predstavio je koncept stanični imunitet. Ehrlich je vjerovao da se imunitet temelji na tvarima koje potiskuju strane objekte. Kasnije se pokazalo da su i jedni i drugi bili u pravu.
Krajem 19.st. došlo se do sljedećih otkrića: Leffler i Roux su pokazali da mikrobi izlučuju egzotoksine, koji, kada se daju životinjama, uzrokuju iste bolesti kao i sami mikrobi. U tom razdoblju dobiveni su antitoksični serumi za razne infekcije (antidifterija, antitetanus). Buckner je otkrio da se mikrobi ne množe u svježoj krvi sisavaca, jer ima baktericidna svojstva, koja su uzrokovana supstancom aleksin (komplement).
AT - aglutinini su otkriveni 1896. godine. Godine 1900. Ehrlich je stvorio teoriju nastanka AT.
Druga faza počinje od početka do sredine 20. stoljeća. Ova faza počinje otkrićem Langsteiner Ar (senzibilizirane T stanice) skupine A, B, 0, koje određuju krvnu grupu čovjeka, a 1940. Langsteiner i Wiener otkrili su Ar na crvenim krvnim stanicama, koji su nazvali Rh faktor. Godine 1902. otvorili su Richet i Portier fenomen alergije. Godine 1923. Ramon je otkrio mogućnost pretvaranja vrlo toksičnih bakterijskih egzotoksina u netoksične tvari pod utjecajem farmolina.
Treća faza sredinom 20. stoljeća do našeg vremena. Počinje Burnetovim otkrićem tolerancije tijela na vlastiti Ar. Godine 1959. Burnet je razvio teoriju klonske selekcije formiranja AT. Porter je otkrio molekularnu strukturu AT.
Imunološki sustav zajedno s drugim sustavima (živčani, endokrini, kardiovaskularni) osigurava postojanost unutarnjeg okruženja tijela (homeostaza). Imunološki sustav ima 3 komponente:
- mobilni,
- humoralni.
- genetski
Stanična komponenta postoji u 2 oblika – organiziran(- limfne stanice koje su dio timusa, koštane srži, slezene, krajnika, limfnih čvorova) i neorganizirano(slobodni limfociti koji cirkuliraju u krvi).
Stanična komponenta nije homogena: T i B stanice. Molekularna komponenta je Ig, kojeg proizvode B limfociti. Poznato je 5 klasa Ig: G, D, M, A, E. Trenutno je utvrđena struktura Ig različitih klasa, od kojih u krvnom serumu čovjeka prevladavaju Ig G (70-75% ukupne količine od Iga).
Osim Ig, molekularna komponenta uključuje imunotransmitere (citokine), koje izlučuju različite stanice imunološkog sustava (makrofagi i limfociti).
Citokini se ne otpuštaju stalno, stupaju u interakciju s receptorima na površini stanice i reguliraju snagu i trajanje imunološkog odgovora. Genetska komponenta uključuje mnoge gene koji određuju sintezu Ig. Svaki od 4 lanca AT proteina kodiran je s 2 strukturna gena.
Imunologija kao specifično područje istraživanja proizašla je iz praktične potrebe borbe protiv zaraznih bolesti. Imunologija se kao zasebno znanstveno područje pojavila tek u drugoj polovici dvadesetog stoljeća. Povijest imunologije kao primijenjene grane infektivne patologije i mikrobiologije mnogo je duža. Višestoljetna promatranja zaraznih bolesti postavila su temelj modernoj imunologiji: unatoč širokom širenju kuge (5. st. pr. Kr.), nitko nije obolio dva puta, barem smrtno, a oni koji su ozdravili korišteni su za pokapanje leševa.
Postoje dokazi da su prva cijepljenja protiv velikih boginja provedena u Kini tisuću godina prije rođenja Krista. Inokulacija sadržaja pustula malih boginja zdravi ljudi kako bi ih zaštitio od akutnog oblika bolesti, zatim se proširio u Indiju, Malu Aziju, Europu i Kavkaz.
Inokulaciju je zamijenila metoda cijepljenja (od latinskog "vacca" - krava), razvijena krajem 18. stoljeća. engleski doktor E. Jenner. Skrenuo je pozornost na činjenicu da su mljekarice koje su se brinule o bolesnim životinjama ponekad oboljele od kravljih boginja u izrazito blagom obliku, ali nikada nisu oboljele od velikih boginja. Takvo zapažanje dalo je istraživaču pravu priliku za borbu protiv bolesti kod ljudi. Godine 1796., 30 godina nakon početka istraživanja, E. Jenner odlučio je isprobati metodu cijepljenja protiv kravljih boginja. Eksperiment je bio uspješan i od tada je metoda cijepljenja E. Jenner našla široku primjenu u cijelom svijetu.
Podrijetlo infektivne imunologije povezano je s imenom izvanrednog francuskog znanstvenika Louis Pasteur. Prvi korak prema ciljanoj potrazi za pripravcima cjepiva koji stvaraju stabilnu imunost na infekcije učinjen je nakon Pasteurovog promatranja patogenosti uzročnika kokošje kolere. Iz ovog zapažanja Pasteur je zaključio: ostarjela kultura, nakon što je izgubila svoju patogenost, ostaje sposobna stvoriti otpornost na infekcije. To je desetljećima određivalo načelo stvaranja materijala za cjepivo - na ovaj ili onaj način (za svaki patogen svoj) postići smanjenje virulencije patogena uz zadržavanje njegovih imunogenih svojstava.
Iako je Pasteur razvio principe cijepljenja i uspješno ih primijenio u praksi, nije bio svjestan čimbenika uključenih u proces zaštite od infekcije. Prvi koji su rasvijetlili jedan od mehanizama imuniteta na infekcije bili su Emil von Behring I Kitazato. Pokazali su da je serum miševa prethodno imuniziranih toksinom tetanusa, ubrizgan intaktnim životinjama, štitio potonje od smrtonosne doze toksina. Serumski faktor nastao kao rezultat imunizacije - antitoksin - prvo je otkriveno specifično protutijelo. Rad ovih znanstvenika postavio je temelj za proučavanje mehanizama humoralne imunosti.
Ruski evolucijski biolog bio je u izvorištu znanja o pitanjima stanične imunosti Ilja Iljič Mečnikov. Godine 1883. napravio je prvo izvješće o fagocitnoj teoriji imuniteta na kongresu liječnika i prirodnih znanstvenika u Odesi. Ljudi imaju ameboidne pokretne stanice – makrofage i neutrofile. One “jedu” posebnu vrstu hrane - patogene mikrobe, funkcija tih stanica je borba protiv agresije mikroba.
Paralelno s Mečnikovim, njemački farmakolog je razvio svoju teoriju imunološke obrane od infekcije Paul Ehrlich. Bio je svjestan činjenice da se u krvnom serumu životinja zaraženih bakterijama pojavljuju proteinske tvari koje mogu ubiti patogene mikroorganizme. Kasnije je te tvari nazvao "antitijela". Najviše karakteristično svojstvo antitijela - to je njihova izražena specifičnost. Stvorivši se kao zaštitni agens protiv jednog mikroorganizma, neutraliziraju i uništavaju samo njega, ostajući ravnodušni prema drugima.
Dvije teorije - fagocitna (stanična) i humoralna - u razdoblju svog nastanka stajale su na antagonističkim pozicijama. Škole Mečnikova i Ehrlicha borile su se za znanstvenu istinu, ne sluteći da svaki udarac i svaka parcija zbližavaju njihove protivnike. Godine 1908. oba su znanstvenika istodobno dobila Nobelovu nagradu.
Krajem 40-ih i početkom 50-ih godina 20. stoljeća završava prvo razdoblje razvoja imunologije. Stvoren je cijeli arsenal cjepiva protiv širokog spektra zaraznih bolesti. Epidemije kuge, kolere i malih boginja više nisu uništavale stotine tisuća ljudi. Izolirana, sporadična izbijanja ovih bolesti još uvijek se javljaju, ali to su samo vrlo lokalni slučajevi koji nemaju epidemiološki, a još manje pandemijski značaj.
Riža. 1. Imunološki znanstvenici: E. Jenner, L. Pasteur, I.I. Mečnikov, P. Erlich.
Nova faza u razvoju imunologije povezana je prvenstveno s imenom izvanrednog australskog znanstvenika M.F. Burnet. Upravo je on uvelike odredio lice moderne imunologije. Promatrajući imunitet kao reakciju usmjerenu na razlikovanje svega "svog" od svega "tuđeg", postavio je pitanje važnosti imunoloških mehanizama u održavanju genetske cjelovitosti organizma u razdoblju individualnog (ontogenetskog) razvoja. Upravo je Burnet skrenuo pozornost na limfocit kao glavnog sudionika u specifičnom imunološkom odgovoru, dajući mu naziv "imunocyte". Bio je Burnet koji je predvidio, a Englez Peter Medawar i češki Milan Hašek eksperimentalno potvrdio stanje suprotno imunološkoj reaktivnosti – toleranciju. Upravo je Burnet ukazao na posebnu ulogu timusa u formiranju imunološkog odgovora. I konačno, Burnet je ostao zapisan u povijesti imunologije kao tvorac klonske selekcijske teorije imuniteta. Formula ove teorije je jednostavna: jedan klon limfocita sposoban je odgovoriti samo na jednu specifičnu, antigensku, specifičnu odrednicu.
Posebnu pažnju zaslužuju Burnetova stajališta o imunitetu kao reakciji organizma koja razlikuje sve "svoje" od svega "stranog". Nakon što je Medawar dokazao imunološku prirodu odbacivanja stranog transplantata, nakon nakupljanja činjenica o imunologiji zloćudnih neoplazmi, postalo je očito da se imunološka reakcija razvija ne samo na mikrobne antigene, već i kada postoje bilo kakvi, iako manji, antigeni razlike između tijela i tog biološkog materijala (transplantat, maligni tumor) s kojim se susreće.
Danas znamo, ako ne sve, onda mnoge mehanizme imunološkog odgovora. Znamo genetsku osnovu iznenađujuće široke raznolikosti antitijela i receptora za prepoznavanje antigena. Znamo koji su tipovi stanica odgovorni za stanične i humoralne oblike imunološkog odgovora; mehanizmi povećane reaktivnosti i tolerancije uvelike su shvaćeni; mnogo se zna o procesima prepoznavanja antigena; identificirani su molekularni sudionici u međustaničnim odnosima (citokini); U evolucijskoj imunologiji formiran je koncept uloge specifične imunosti u progresivnoj evoluciji životinja. Imunologija kao samostalna grana znanosti stoji ravnopravno s istinski biološkim disciplinama: molekularnom biologijom, genetikom, citologijom, fiziologijom, evolucijskim učenjem.