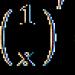Esej
Kurs sadrži: ___ stranica, 4 tablice, 2 slike, 8 literarni izvori. Predmet istraživanja u predmetni rad su složeni prehrambeni proizvodi kemijski sastav.
Svrha rada je odrediti sadržaj olova u prehrambenim proizvodima i usporediti ga s MDK.
Metoda istraživanja je atomska apsorpcija.
Navedene su metode pripreme uzoraka. Analizirani su i sažeti podaci o sadržaju spojeva olova u prehrambenim objektima (objektima).
Područje primjene: analitička i toksikološka kemija, laboratoriji za standardizaciju i kvalitetu prehrambenih proizvoda lake industrije, farmaceutska kemija.
Ključne riječi: OLOVO, ATOMSKA APSORCIJSKA SPEKTROSKOPIJA, APSORPCIJA, STANDARDNA OTOPINA, KALIBRACIONI GRAF, SADRŽAJ, MPC
Uvod
1. Pregled literature
1.3 Priprema uzorka
2. Eksperimentalni dio
zaključke
Uvod
Korištenje materijala koji sadrže olovo i njegove spojeve dovelo je do kontaminacije mnogih predmeta okoliš. Određivanje olova u metalurškim proizvodima, biološkim materijalima, zemljištu itd. predstavlja poteškoće jer je obično praćen drugim dvovalentnim metalima. Da riješim ovo analitički problem Atomska apsorpcijska metoda određivanja postala je raširena zbog dostupnosti opreme, visoke osjetljivosti i dovoljne točnosti.
Prehrambeni proizvodi mogu sadržavati ne samo korisne tvari, već i prilično štetne i opasne za ljudsko tijelo. Stoga je glavni zadatak analitičke kemije kontrola kvalitete hrane.
Naime, ovaj rad koristi atomsku apsorpcijsku metodu za određivanje olova u kavi.
1. Pregled literature
1.1 Kemijska svojstva olova
U periodnom sustavu D.I. Olovo po Mendeljejevu nalazi se u IV skupini, glavnoj podskupini, i ima atomsku masu 207,19 Olovo u svojim spojevima može biti u oksidacijskom stupnju +4, ali za njega je najkarakterističnije +2.
U prirodi se olovo javlja u obliku raznih spojeva od kojih je najvažniji olovni sjaj PbS. Prevalencija olova u Zemljina kora je 0,0016 tež. %.
Olovo je plavkasto-bijeli teški metal gustoće 11,344 g/cm 3. Vrlo je mekan i lako se reže nožem. Talište olova 327.3 O C. Na zraku se olovo brzo prekriva tankim slojem oksida koji ga štiti od daljnje oksidacije. U nizu napona olovo dolazi neposredno prije vodika; njegov normalni potencijal je - 0,126 V.
Voda sama po sebi ne reagira s olovom, ali u prisutnosti zraka, olovo se postupno uništava vodom i nastaje olovni hidroksid:
Pb+O 2+ H2 O=2Pb(OH) 2
Međutim, kada dođe u dodir s tvrdom vodom, olovo se prekriva zaštitnim filmom netopivih soli (uglavnom olovnog sulfata i bazičnog olovnog karbonata) koji sprječava daljnje djelovanje vode i stvaranje hidroksida.
Razrijeđena klorovodična i sumporna kiselina ne djeluju na olovo zbog slabe topljivosti odgovarajućih olovnih soli. Olovo se lako otapa u dušičnoj kiselini. Organske kiseline, osobito octena kiselina, također otapaju olovo u prisutnosti atmosferskog kisika.
Olovo se također otapa u alkalijama, tvoreći plumbite.
1.2 Fiziološka uloga olova
Metabolizam olova u ljudi i životinja vrlo je malo proučavan. Biološka uloga također nije potpuno jasno. Poznato je da olovo u tijelo ulazi hranom (0,22 mg), vodom (0,1 mg) i prašinom (0,08 mg). Tipično, sadržaj olova u tijelu muškarca je oko 30 µg%, a kod žena oko 25,5 µg%.
S fiziološkog gledišta, olovo i gotovo svi njegovi spojevi otrovni su za ljude i životinje. Olovo se, čak iu vrlo malim dozama, nakuplja u ljudskom tijelu, a njegov toksični učinak postupno se povećava. Kada dođe do trovanja olovom, na desnima se pojavljuju sive mrlje i funkcije su poremećene. živčani sustav, postoji bol u unutarnji organi. Akutno trovanje dovodi do teških oštećenja jednjaka. Za ljude koji rade s olovom, njegovim legurama ili spojevima (na primjer, tiskarski radnici), trovanje olovom je profesionalna bolest. Opasna doza za odraslu osobu je u rasponu od 30-60 g Pb (CH3COO) 2 * 3H 2O .
1.3 Priprema uzorka
Odabir i priprema laboratorijskih uzoraka provodi se sukladno normativno tehničkoj dokumentaciji za ovu vrstu proizvoda. Iz kombiniranog laboratorijskog uzorka uzimaju se dva paralelna uzorka.
Proizvodi s visokim udjelom šećera (slastice, džemovi, kompoti) tretiraju se sumpornom kiselinom (1: 9) u omjeru od 5 cm. 3 kiseline na 1 g suhe tvari i inkubira 2 dana.
Proizvodi s udjelom masti od 20-60% (sir, sjemenke uljarica) tretiraju se dušičnom kiselinom (1:
) na temelju 1,5 cm 3 kiseline na 10 g suhe tvari i inkubira 15 minuta.
Uzorci se suše u pećnici na 150 O C (ako nema agresivnih kiselih para) na električnom štednjaku s niskom temperaturom. Za ubrzanje sušenja uzoraka može se koristiti istovremeno zračenje uzoraka IR lampom.
Osušeni uzorci pažljivo se pale na električnom štednjaku ili plinskom plameniku dok ne prestane ispuštanje dima, čime se sprječava paljenje i emisija.
Stavite lončiće u hladnu električnu peć i povećajte temperaturu za 50 O Svakih pola sata zagrijte pećnicu na 450 O C. Na ovoj temperaturi nastavlja se mineralizacija dok se ne dobije sivi pepeo.
Pepeo ohlađen na sobnu temperaturu navlaži se kap po kap dušičnom kiselinom (1:
) na bazi 0,5-1 cm 3 izvagane kiseline, isparene u vodenoj kupelji i osušene na električnom štednjaku na laganoj vatri. Stavite pepeo u električnu peć i dovedite mu temperaturu na 300 O C i drži 0,5 sati.Ovaj ciklus (tretiranje kiselinom, sušenje, pepeljenje) može se ponoviti nekoliko puta.
Mineralizacija se smatra završenom kada pepeo postane bijel ili blago obojen bez pougljenjenih čestica.
Mokra mineralizacija. Metoda se temelji na potpunoj razgradnji organska tvar uzoraka pri zagrijavanju u smjesi koncentriranih dušična kiselina, sumpornu kiselinu i vodikov peroksid te je namijenjen za sve vrste prehrambenih proizvoda, maslaca i životinjskih masti.
Odvagani dio tekućeg i kašastog proizvoda dodaje se u tikvicu s ravnim dnom, kvašeći stijenke čaše od 10-15 cm 3bidestilirana voda. Uzorak možete uzeti izravno u tikvicu s ravnim dnom.
Uzorak krutih i pastoznih proizvoda uzme se na filtar bez pepela, zamota u njega i stavi staklenim štapićem na dno tikvice s ravnim dnom.
Uzorci pića uzimaju se pipetom, prenose u Kjeldahlovu tikvicu i upare na električnom kuhalu do 10-15 cm3 .
Odvagani dio suhih proizvoda (želatina, jaje u prahu) stavi se u tikvicu i doda 15 cm 3bidestilirane vode, promiješajte. Želatina se ostavi 1 sat da nabubri.
Mineralizacija uzorkaMineralizacija uzoraka sirovina i prehrambenih proizvoda osim biljnih ulja, margarina, jestivih masti:
U tikvicu se dodaje dušična kiselina za izračunavanje 10 cm 3na svakih 5 g pripravka i inkubirati najmanje 15 minuta, zatim dodati 2-3 čiste staklene kuglice, zatvoriti kruškolikim čepom i zagrijavati na električnom štednjaku, prvo slabo, zatim jače, uz isparavanje sadržaja tikvice. do volumena od 5 cm3 .
Ohladite tikvicu, dodajte 10 cm 3dušične kiseline, ispariti do 5 cm 3. Ovaj ciklus se ponavlja 2-4 puta dok smeđe pare ne prestanu.
Dodajte 10 cm u tikvicu 3dušična kiselina, 2 cm 3sumporne kiseline i 2 cm 3vodikov peroksid na svakih 5 g proizvoda (mineralizacija mliječnih proizvoda provodi se bez dodavanja sumporne kiseline).
Za uklanjanje ostataka kiseline dodajte 10 cm 3dvostruko destilirane vode, zagrijavati do pojave bijelih para i zatim kuhati još 10 minuta. Cool. Dodavanje vode i zagrijavanje se ponavlja još 2 puta.
Ako se stvori talog, dodajte 10 cm 3bidestilirane vode, 2 cm 3sumporna kiselina, 5 cm 3 klorovodične kiseline i kuhati dok se talog ne otopi uz dolijevanje vode koja isparava. Nakon otapanja taloga, otopina se upari u vodenoj kupelji do vlažnih soli.
Mineralizacija biljnih ulja, margarina, jestivih masti:
dovesti kemiju hrane
Tikvica s uzorkom se zagrijava na električnom štednjaku 7-8 sati dok ne nastane viskozna masa, ohladi se i 25 cm 3dušične kiseline i ponovno pažljivo zagrijte, izbjegavajući snažno pjenjenje. Nakon prestanka pjenjenja dodajte 25 cm 3dušične kiseline i 12 cm 3vodikovog peroksida i zagrijava dok se ne dobije bezbojna tekućina. Ako tekućina potamni, povremeno dodajte 5 cm 3dušične kiseline, nastavljajući zagrijavanje do završetka mineralizacije. Mineralizacija se smatra završenom ako otopina nakon hlađenja ostane bezbojna.
Ekstrakcija kiseline. Metoda se temelji na ekstrakciji toksičnih elemenata razrijeđenim (1:
) volumno solnom kiselinom ili razrijeđen (1:2) volumno dušičnom kiselinom i namijenjen je biljnim i maslačnim uljima, margarinu, jestivim mastima i sirevima.
Ekstrakcija se provodi u uzorku proizvoda otpornom na toplinu. Dodajte 40 cm u tikvicu pomoću cilindra. 3otopina klorovodične kiseline u dvostruko destiliranoj vodi (1:
) po volumenu i istom količinom dušične kiseline (1:2). U tikvicu se doda nekoliko staklenih kuglica, u nju se umetne hladnjak, stavi na električni štednjak i kuha 1,5 sat od trenutka vrenja. Zatim se sadržaj tikvice polako ohladi na sobnu temperaturu bez uklanjanja hladnjaka.
Tikvica s ekstrakcijskom smjesom maslaca, masti ili margarina s kiselinom stavlja se u hladnu vodenu kupelj da se mast učvrsti. Stvrdnuta mast se probuši staklenim štapićem, tekućina se filtrira kroz filtar navlažen kiselinom kojom se ekstrahira u kvarcnu ili porculansku zdjelu. Masnoća koja je ostala u tikvici se rastopi u vodenoj kupelji, doda se 10 cm 3kiseline, protresti, ohladiti, nakon hlađenja mast se kalcinira i tekućina se kroz isti filter prelije u istu posudu, zatim ispere 5-7 cm. 3bidestilirana voda.
Ekstrakcijska smjesa biljnog ulja i kiseline se prenosi u lijevak za odjeljivanje. Tikvica se ispere 10 cm 3kiseline, koja se ulijeva u isti lijevak. Nakon odvajanja faza, donji vodeni sloj se izlije kroz filter natopljen kiselinom u kvarcnu ili porculansku posudu, filter se ispere 5-7 cm 3bidestilirana voda.
Ekstrakcijska smjesa sira i kiseline filtrira se kroz filtar natopljen kiselinom u kvarcnu ili porculansku zdjelu. Tikvica se ispere 10 cm 3kiseline, koja se filtrira kroz isti filter, zatim se filter ispere 5-7 cm 3bidestilirana voda.
Procijeđeni ekstrakt pažljivo se ispari i pougljeni na električnom štednjaku, a zatim pepe u električnoj pećnici.
1.4 Metode određivanja olova
1.4.1 Koncentracija tragova iona olova korištenjem nanometarskih čestica titanijevog dioksida (anataza) u svrhu njihovog naknadnog određivanja atomskom emisijskom spektrometrijom s induktivno spregnutom plazmom s elektrotermalnim isparavanjem uzorka
Spektrometrija atomske emisije induktivno spregnute plazme ( ISP-AES) -široko korištena i vrlo obećavajuća metoda elementarne analize. Međutim, ima neke nedostatke, uključujući relativno nisku osjetljivost detekcije, nisku učinkovitost raspršivanja, spektralne interferencije i druge efekte matrice. Stoga ICP-AES ne ispunjava uvijek zahtjeve moderna znanost i tehnologije. Kombinacija ICP-AES s elektrotermalnim isparavanjem uzorka (ETI-ICP-AES) značajno proširuje mogućnosti metode. Optimiziranjem temperatura pirolize i isparavanja, elementi analita mogu se uzastopno ispariti, odvajajući ih od matrice uzorka. Ova metoda ima prednosti visoke učinkovitosti uvođenja uzorka, mogućnosti analize malih količina uzoraka, niskih apsolutnih granica detekcije i mogućnosti izravne analize čvrstih uzoraka.
Alati i uvjeti analize.Korišten je ICP generator snage 2 kW i frekvencije 27 ± 3 MHz; ISP plamenik; grafitna peć WF-1A; difrakcijski spektrometar RO5-2 s difrakcijskom rešetkom od 1300 linija/mm s linearnom disperzijom od 0,8 nm/mm; pH metar Mettle Toledo 320-S; sedimentacijska centrifuga model 800.
Standardne otopine i reagensi.Temeljne standardne otopine s koncentracijom od 1 mg/ml pripremaju se otapanjem odgovarajućih oksida (spektroskopske čistoće) u razrijeđenoj HCl, nakon čega slijedi razrjeđivanje s vodom do zadanog volumena. Suspenzija politetrafluoretilena dodana je svakoj standardnoj otopini do koncentracije od 6% w/v.
Koristili smo Triton X-100 reagens grade (SAD). Preostali korišteni reagensi bili su spektroskopske čistoće; dvostruko destilirana voda. Nanočestice titanijevog dioksida promjera manjeg od 30 nm.
Metoda analize.Potreban volumen otopine koja sadrži metalne ione stavi se u graduiranu epruvetu od 10 ml i pH se podesi na 8,0 pomoću 0,1 M HCl i Vodena otopina NH 3. Zatim se u epruvetu doda 20 mg nanočestica titanijevog dioksida. Protresite epruvetu 10 minuta. (preliminarni pokusi su pokazali da je to dovoljno za postizanje adsorpcijske ravnoteže). Epruveta se ostavi 30 minuta, zatim se tekuća faza ukloni centrifugom. Nakon ispiranja taloga vodom, doda se 0,1 ml 60% politetrafluoretilenske suspenzije, 0,5 ml 0,1% otopine agara, 0,1 ml. Triton X-100 i razrijeđen s vodom do 2,0 ml. Smjesa se zatim raspršuje pomoću ultrazvučnog vibratora 20 minuta kako bi se postigla homogenost suspenzije prije nego što se uvede u isparivač. 20 μl suspenzije doda se u grafitnu peć nakon zagrijavanja i stabilizacije ICP-a. Nakon sušenja, pirolize i isparavanja, para uzorka se prenosi u ICP strujom plina nosača (argona); snimaju se signali atomske emisije. Prije svakog ubrizgavanja uzorka, grafitna peć se zagrijava na 2700°C kako bi se očistila.
Primjena metode.Razvijena metoda koristi se za određivanje Pb 2+u uzorcima prirodne jezerske i riječne vode. Uzorci vode su filtrirani kroz membranski filter od 0,45 µm odmah nakon uzorkovanja i zatim analizirani.
1.4.2 Određivanje koncentracije kombinacije olova u stvarnom vremenu nakon čega slijedi HPLC reverzne faze
Instrumenti i reagensi. Dijagram HPLC sustava s koncentracijom u stvarnom vremenu ("on-line") prikazan je na slici 1.1. Sustav se sastoji od pumpe Waters 2690 Alliance (na dijagramu 2), pumpe Waters 515 (1), pumpe Waters 996 detektor s nizom fotodioda (7), šestokraki prekidač (4), uređaj za ubrizgavanje velikog volumena (drži do 5,0 ml uzorka) (3) i kolone (5,6). Kolona za koncentriranje bila je Waters Xterra™ RP 18(5 µm, 20 x 3,9 mm), Waters Xterra™ RP analitička kolona 18(5 µm, 150 x 3,9 mm). pH je određen pH metrom Beckman F-200, a optička gustoća mjerena je spektrofotometrom Shimadzu UV-2401.
Slika 1.1Shema sustava koncentracije u stvarnom vremenu pomoću prekidača
Sve otopine su pripremljene korištenjem ultračiste vode dobivene korištenjem Milli-Q50 Sp Reagent Water System (Millipore Corporation). Standardna otopina olova (P) koncentracije 1,0 mg/ml, radne otopine koncentracije iona 0,2 μg/ml pripremaju se razrjeđivanjem standardnih. Upotrijebite tetrahidrofuran (THF) za HPLC (Fisher Corporation), pufersku otopinu pirolidin-octene kiseline s koncentracijom od 0,05 mol/L. Prije upotrebe stakleno posuđe je dugo namakano u 5% otopini dušične kiseline i isprano čistom vodom.
Eksperimentalna tehnika. Potreban volumen standardne otopine ili uzorka dodaje se u odmjernu tikvicu od 25 cm. 3, dodajte 6 ml otopine T 4CPP s koncentracijom 1 x10 -4mol/l u THF i 4 ml puferske otopine pirolidin-octene kiseline koncentracije 1 x 10 -4mol/l i pH 10, razrijediti vodom do oznake i dobro promiješati. Smjesa se zagrijava u kipućoj vodenoj kupelji 10 minuta. Nakon hlađenja, razrijedite do oznake THF za naknadnu analizu. Otopina (5,0 ml) se uvodi u dozator i šalje u kolonu za koncentriranje pomoću mobilne faze A brzinom od 2 cm3/min. Po završetku koncentriranja eliminacijom šesteroputnog ventila dolazi do keliranja metala s T 4CPP adsorbirani na vrhu kolone za koncentriranje eluiraju se protokom mobilnih faza A i B brzinom od 1 ml/min c obrnuti smjer i šalje u analitički stupac. Trodimenzionalni kromatogram snimljen je u području valne duljine maksimalne apsorpcije 465 nm pomoću detektora s nizom fotodioda.
1.4.3 Stripping voltametrijsko određivanje olova korištenjem sustava staklenih ugljičnih elektroda
Instrumenti i reagensi.Za studije smo koristili sustav elektroda, koji je bio sklop od tri identične elektrode od staklenog ugljika (GC) (indikator, pomoćna, usporedba) utisnute u zajedničko tetrafluoroetilensko kućište. Duljina svake elektrode koja viri iz kućišta je 5 mm. Površina jednog od njih, odabranog kao indikatora, elektrokemijski je obrađena asimetričnom strujom gustoće u rasponu od 0,1-5 kA/m 2preporučuje se za metale. Optimalno vrijeme obnavljanja površine utvrđeno je eksperimentalno i iznosilo je 10-20 s. Indikatorska elektroda služila je kao anoda, a elektroda od nehrđajućeg čelika kao katoda. Koristili smo 0,1 M vodene otopine kiselina, soli, lužina, kao i 0,1 M otopine lužina ili soli u smjesi organskih otapala s vodom u volumnom omjeru 1:19. Stanje obrađene površine promatrano je vizualno mikroskopom Neophot 21 s povećanjem od oko 3000.
Metoda analize.Nakon obrade, elektrodni sklop je korišten za određivanje 3x10 -6M odvod (II) striping voltametrijom prema pozadini od 1*10 -3M HNO 3. Nakon elektrolize na – 1,5 V tijekom 3 minute uz miješanje magnetskom miješalicom, snimljen je voltamogram na polarografu PA-2. Potencijal anodnog vrha olova ostao je konstantan i iznosio je -0,7 V. Brzina skeniranja linearnog potencijala bila je 20 mV/s, amplituda skeniranja bila je 1,5 V, trenutna osjetljivost bila je 2 * 10-7. A/mm.
Vodene otopine LiNO 3, NaNO 3, KNO 3kao elektrolit za obradu, omogućuju postizanje stabilnih visina već u drugom mjerenju sa zadovoljavajućom obnovljivošću (2,0, 2,9 odnosno 5,4%). Najveća osjetljivost očitanja postiže se korištenjem elektrolita s manjim kationom.
1.4.4 Određivanje atomske apsorpcije olova doziranjem suspenzija karboniziranih uzoraka upotrebom aktivnog ugljena koji sadrži Pd kao modifikatora
Analitička mjerenja provedena su na atomskom apsorpcijskom spektrometru SpectrAA-800 s elektrotermalnim raspršivačem GTA-100 i autosamplerom PSD-97 (Varian, Australija). Koristili smo grafitne cijevi s pirokozama i integriranom platformom (Varian, Njemačka), žarulje sa šupljom katodom za olovo (Hitachi, Japan) i kadmij (C Varian, Australija). Mjerenja integralne apsorpcije s korekcijom za neselektivnu apsorpciju svjetlosti (deuterijski sustav) provedena su pri širini spektralnog proreza od 0,5 nm i valnoj duljini od 283,3 nm. Kao zaštitni plin poslužio je argon "najvišeg stupnja". Temperaturni program za rad raspršivača dat je u tablici 1.1
Stol 1.1 Temperaturni program za rad elektrotermalnog raspršivača GTA-100
Stupanj Temperatura, °Csušenje 190sušenje 2120piroliza1300hlađenje50atomizacija23OOčišćenje2500
Pripravci koji sadrže paladij na bazi aktivnog ugljena i karboniziranih ljuski lješnjaka proučavani su kao modifikatori za atomsko apsorpcijsko određivanje Pb u grafitnoj peći. Sadržaj metala u njima bio je 0,5-4%. Za procjenu promjena koje se događaju s komponentama sintetiziranih modifikatora pod redukcijskim uvjetima primijenjenim tijekom analize, materijali su tretirani vodikom na sobnoj temperaturi.
Otopina s poznatom koncentracijom Pb pripremljena je razrjeđivanjem GSO br. 7778-2000 i br. 7773-2000 s 3% HNO 3. Raspon koncentracija radnih standardnih otopina elementa za konstruiranje kalibracijskih ovisnosti bio je 5,0-100 ng/ml. Za pripremu otopina korištena je deionizirana voda .
Pri konstruiranju krivulja pirolize i atomizacije koristili smo standardnu otopinu elementa i karbonizirani „Standardni uzorak sastava mljevenog zrna pšenice ZPM-01“. U prvom slučaju dodaje se 1,5 ml standardne otopine elementa (50 ng/ml Pd u 5% HNO 3) i 10-12 mg aktivnog ugljena koji sadrži paladij; suspenzija je homogenizirana i dozirana u grafitnu peć. U drugom je pripremljenoj suspenziji karboniziranog uzorka dodana ista količina modifikatora (5-10 mg uzorka u 1-2 ml 5% HNO3 ).
1.4.5 Fotometrijsko određivanje i koncentracija olova
U radu je korišten olovni acetat analitičke čistoće. Spojevi (slika 1, koji su dibazične kiseline) dobiveni su azo sprezanjem otopine 2-hidroksi-4(5)-nitrofenildiazonijevog klorida i odgovarajućeg hidrazona. Otopine formazana u etanolu pripremljene su preciznim vaganjem.
Optička gustoća otopina mjerena je na spektrofotometru Beckman UV-5270 u kvarcnim kivetama (l = 1 cm). Koncentracija vodikovih iona mjerena je ionometrom I-120M.
Reagensi reagiraju s ionima olova, tvoreći obojene spojeve. Batokromni učinak tijekom stvaranja kompleksa je 175 - 270 nm. Na kompleksiranje utječe priroda otapala i struktura reagensa (slika 1).
Optimalni uvjeti za određivanje olova su medij voda-etanol (1:
) i pH 5,5-6,0, stvoren puferskom otopinom amonijevog acetata. Granica detekcije za olovo je 0,16 µg/ml. Trajanje analize 5 min.
Najzanimljivija je uporaba formazana kao reagensa za koncentraciju i naknadno fotometrijsko određivanje olova. Suština koncentracije i naknadnog određivanja olova (II) pomoću formazana je da se kompleks olova ekstrahira iz vodeno-etanolne otopine u prisutnosti iona Ni, Zn, Hg, Co, Cd, Cr, Fe otopinom kloroforma. od formazana.
Za usporedbu koristili smo metodu određivanja olova sulfarsazenom (GOST, MU izdanje 15, br. 2013-79). Rezultati analize rješenja modela primjenom dviju metoda dani su u tablici 1.2. Usporedba varijanci primjenom F-kriterija pokazala je da Fexp< Fтеор (R= 0,95; f 1=f 2= 5); To znači da su varijance homogene.
Stol 1.2 rezultati određivanja olova u modelnim otopinama (n=6; P=0,95)
Uvedeno, µg/mlFoundFoundFexpF teorsulfarsazen, µg/mlS r formazan, µg/mlS r 4,14 2,10 3,994,04 ±0,28 2,06±0,29 3,92 ±0,17 0,29 3,92 ±0,172,8 5,5 1,74,14 ±0,07 2,10 ±0,08 3,99 ± 0,072,1 *10 -2 2.5*10-2 2.1*10-23.97 3.57 3.374.53
2. Eksperimentalni dio
Mjerni instrumenti, reagensi i materijali:
Pri izvođenju ove metode koriste se sljedeći mjerni instrumenti, uređaji, reagensi i materijali:
· Atomski apsorpcijski spektrometar
· Spektralna svjetiljka sa šupljom katodom
· Kompresor za dovod komprimiranog zraka
· Mjenjač - prema GOST 2405
· Laboratorijske čaše, zapremine 25-50 cm3 - prema GOST 25336
· Mjerne tikvice druge klase točnosti kapaciteta 25-100 cm3
· Laboratorijski lijevci prema GOST 25336
· Destilirana voda
· Koncentrirana dušična kiselina, x. h., GOST 4461-77
· Standardna otopina olova (c = 10-1 g/l)
Uvjeti utvrđivanja:
§ Valna duljina pri određivanju odvoda? = 283,3 nm
§ Širina proreza monokromatora 0,1 nm
§ Struja žarulje 10 mA
Metoda mjerenja:
Atomska apsorpcijska spektroskopija temelji se na apsorpciji zračenja u optičkom području od nepobuđenih slobodnih atoma olova koji nastaju kada se analizirani uzorak unese u plamen na valnoj duljini ? = 283,3 nm.
Sigurnosni zahtjevi:
Prilikom izvođenja svih operacija potrebno je strogo poštivati sigurnosna pravila pri radu u kemijskom laboratoriju, koja odgovaraju GOST 126-77 "Osnovna sigurnosna pravila u kemijskom laboratoriju", uključujući pravila za siguran rad s električnim uređajima s naponom do 1000 volti.
Priprema otopina za kalibraciju olova:
Otopine se pripremaju pomoću standardne otopine olova s koncentracijom
c= 10-1 g/l.
Za izradu kalibracijske krivulje upotrijebite otopine sljedećih koncentracija:
*10-4, 3*10-4, 5*10-4, 7*10-4, 10*10-4g/l
Standardna otopina volumena 10 cm 3dodati u tikvicu od 100 ml i napuniti do oznake destiliranom vodom. U 5 odmjernih tikvica zapremnine 100 ml dodajte 1, 3, 5, 7, 10 ml međuotopine (otopina koncentracije 10 -2g/l). Nadopuniti destiliranom vodom do oznake. Konstruirajte gradacijski graf u koordinatama A, y. e od s, g/l
Tablica 2.1 Rezultati mjerenja
koncentracija, g/lSignal, u. e. 0,000130,0003150,0005280,0007390,001057
Priprema uzorka:
Uzimam uzorak kave težine 1,9975 g.
Dodam u čašu od 100 ml.
Uzorak otopim u 20 ml koncentrirane dušične kiseline.
Isparavam sadržaj čaše u vodenoj kupelji do pola izvornog volumena, povremeno miješajući.
Otopina u čaši nakon isparavanja je mutna, stoga pomoću laboratorijskog lijevka i papirnatog filtra filtriram sadržaj čaše u čašu od 25 ml.
Procijeđenu otopinu dodam u tikvicu od 25 ml i destiliranom vodom dovedem do oznake.
Temeljito promiješam sadržaj tikvice.
Dio otopine iz tikvice dodam u pipetu koja služi kao uzorak za određivanje sadržaja olova.
Da bi se odredila nepoznata koncentracija, otopina se unosi u atomizer i nakon 10-15 sekundi bilježe se očitanja uređaja. Prosječna očitanja uređaja ucrtana su na ordinatnu os kalibracijskog grafikona, a odgovarajuća vrijednost koncentracije, sh g/l, nalazi se na apscisnoj osi
Za izračun koncentracije u uzorku koristim formulu za izračun:
S =0,025*Sh*10-4*1000/ Mnav (kg)
Tablica 2.2 Rezultati mjerenja
ProbaSignal, u. e. ProsjekC x , g/l 123 kava15141514,666672,9*10 -4sir00000jabuke sok00000grožđa sok00000krema3222.333337.8*10 -5voda00000šampon00000
Na temelju tabličnih podataka izračunavam koncentraciju olova u uzorcima:
Uzorak MPC, mg/kg kave 10 vrhnja
C (Pb u uzorku kave) = 3,6 mg/kg
C (Pb u uzorku kreme) = 0,98 mg/kg
zaključke
U radu su opisane metode određivanja olova različitim fizikalnim i kemijskim metodama.
Prikazane su metode pripreme uzoraka za niz prehrambenih objekata.
Na temelju literaturnih podataka odabrana je najprikladnija i optimalna metoda za određivanje olova u raznim prehrambenim proizvodima i prirodnim objektima.
Korištenu metodu karakterizira visoka osjetljivost i točnost, uz izostanak reakcije na prisutnost drugih elemenata, što omogućuje dobivanje pravih vrijednosti sadržaja željenog elementa s visok stupanj pouzdanost.
Odabrana metoda također omogućuje provođenje istraživanja bez posebnih poteškoća u pripremi uzorka i ne zahtijeva maskiranje drugih elemenata. Osim toga, metoda vam omogućuje određivanje sadržaja drugih elemenata u ispitnom uzorku.
Na temelju eksperimentalnog dijela možemo zaključiti da sadržaj olova u Black Card kavi ne prelazi maksimalno dopuštenu koncentraciju, stoga je proizvod pogodan za prodaju.
Popis korištene literature
1. Glinka N.I. Opća kemija. - M.: Nauka, 1978. - 403 str.
Zolotov Yu.A. Osnove analitičke kemije. - M.: Viši. škola; 2002. - 494 str.
Remy G. Tečaj opća kemija. - M: ur. stranim lit., 1963. - 587 str.
GOST br. 30178 - 96
Yiping Hang. // Časopis. analit him., 2003, T.58, br. 11, str.1172
Liang Wang. // Časopis. analit him., 2003, T.58, br. 11, str.1177
Nevostruev V.A. // Časopis. analit khim., 2000, T.55, br. 1, str.79
Burilin M.Yu. // Časopis. analit khim., 2004, T.61, br. 1, str.43
Maslakova T.I. // Časopis. analit khim., 1997, T.52, br. 9, str.931
1. Određivanje kao sulfida. Začeci ove metode i njena prva kritička procjena sežu u početak našeg 20. stoljeća. Boja i stabilnost sola PbS ovise o veličini čestica disperzne faze, na koju utječu priroda i koncentracija otopljenih elektrolita, reakcija medija i način pripreme. Stoga se ovi uvjeti moraju strogo pridržavati.
Metoda nije vrlo specifična, posebno u alkalna sredina, ali je konvergencija rezultata u alkalnim otopinama bolja. U kiselim otopinama osjetljivost određivanja je manja, ali se može malo povećati dodavanjem elektrolita, npr. NH 4 C1, u analizirani uzorak. Selektivnost određivanja u alkalnom mediju može se poboljšati uvođenjem maskirajućih kompleksirajućih sredstava.
2. Određivanje u obliku kompleksnih klorida. Već je naznačeno da kompleksi Pb klora apsorbiraju svjetlost u UV području, a koeficijent molarne ekstinkcije ovisi o koncentraciji Cl iona - U 6 M otopini HCl maksimumi apsorpcije Bi, Pb i Tl dovoljno su udaljeni od svakog drugi, što omogućuje njihovo istovremeno određivanje apsorpcijom svjetlosti na 323, 271 i 245 nm, redom. Optimalni raspon koncentracija za određivanje Pb je 4-10*10-4%.
3. Određivanje nečistoća Pb u koncentriranoj sumpornoj kiselini temelji se na korištenju karakteristične apsorpcije pri 195 nm u odnosu na standardnu otopinu, koja se priprema otapanjem olova u H2S04 (posebne čistoće).
Određivanje organskim reagensima.
4. U analizi različitih prirodnih i industrijskih objekata, fotometrijsko određivanje Pb pomoću ditizona, zbog svoje visoke osjetljivosti i selektivnosti, zauzima vodeće mjesto. U razne opcije postojeće metode Fotometrijsko određivanje Pb provodi se na valnoj duljini maksimalne apsorpcije ditizona ili olovo ditizonata. Opisane su i druge varijante ditizonske metode: fotometrijska titracija bez razdvajanja faza i neekstrakcijska metoda za određivanje olova u polimerima, u kojoj se kao reagens koristi otopina ditizona u acetonu, koja se prije upotrebe razrijedi vodom do koncentracije organske komponente 70%.
5. Određivanje olova reakcijom s natrijevim dietilditiokarbamatom. Olovo se lako ekstrahira pomoću CCl4 u obliku bezbojnog dietilditiokarbamata pri različitim pH vrijednostima. Dobiveni ekstrakt se koristi u neizravnoj metodi za određivanje Pb, koja se temelji na stvaranju ekvivalentne količine žuto-smeđeg bakrenog dietilditiokarbamata kao rezultat izmjene s CuS04.
6. Određivanje reakcijom s 4-(2-piridilazo)-rezorcinolom (PAR). Visoka stabilnost kompleksa crvenog Pb s PAR i topljivost reagensa u vodi su prednosti metode. Za određivanje Pb u nekim predmetima, primjerice u čeliku, mesingu i bronci, metoda koja se temelji na stvaranju kompleksa s ovim azo spojem je poželjnija od ditizonske. Međutim, on je manje selektivan i stoga, u prisutnosti interferirajućih kationa, zahtijeva prethodno odvajanje HD metodom ili ekstrakciju olovo dibenzilditiokarbamata ugljikovim tetrakloridom.
7. Određivanje reakcijom s 2-(5-kloropiridip-2-azo)-5-dietilaminofenolom i 2-(5-bromopiridil-2-azo)-5-dietilaminofenolom. Oba reagensa tvore 1:1 komplekse s Pb s gotovo identičnim spektrofotometrijskim karakteristikama.
8. Određivanje reakcijom sa sulfarsazenom. Metoda koristi stvaranje crvenkasto-smeđeg kompleksa topljivog u vodi sastava 1: 1 s maksimumom apsorpcije na 505-510 nm i molarnim koeficijentom ekstinkcije od 7,6 * 103 na ovoj valnoj duljini i pH 9-10.
9. Određivanje reakcijom s arsenazom 3. Ovaj reagens u pH području 4-8 stvara plavi kompleks sastava 1:1 s olovom s dva apsorpcijska maksimuma - na 605 i 665 nm.
10. Određivanje reakcijom s difenilkarbazonom. Po osjetljivosti reakcije, pri ekstrakciji kelata u prisutnosti KCN, a po selektivnosti približava se ditizonu.
11. Indirektna metoda određivanja Pb pomoću difenilkarbazida. Metoda se temelji na taloženju olovnog kromata, njegovom otapanju u 5% HCl i fotometrijskom određivanju dikromne kiseline reakcijom s difenilkarbazidom pomoću filtra s maksimalnim prijenosom na 536 nm. Metoda je dugotrajna i nije baš precizna.
12. Određivanje reakcijom s ksilenol narančastim. Xylenol oranž (KO) tvori kompleks 1:1 s olovom, čija optička gustoća doseže svoju granicu na pH 4,5-5,5.
13. Određivanje reakcijom s bromopirogalpol crvenilom (BPK) u prisutnosti senzibilizatora. Kao senzibilizatori koriste se difenilgvanidinij, benziltiuronij i tetrafenilfosfonij kloridi koji povećavaju intenzitet boje, ali ne utječu na položaj apsorpcijskog maksimuma na 630 nm, a cetiltrimetilamonij i cetilpiridinij bromidi na pH 5,0.
14. Određivanje reakcijom s glicintimol modrilom. Kompleks s glicintimol plavim (GBL) sastava 1:2 ima apsorpcijski maksimum na 574 nm i odgovarajući molarni koeficijent ekstinkcije od 21300 ± 600.
15. Određivanje s metiltimol modrilom provodi se pod uvjetima sličnim onima za stvaranje kompleksa s GTS. Što se tiče osjetljivosti, obje reakcije su bliske jedna drugoj. Apsorpcija svjetlosti mjeri se pri pH 5,8-6,0 i valnoj duljini od 600 nm, što odgovara položaju maksimuma apsorpcije. Molarni koeficijent ekstinkcije je 19 500. Smetnje od mnogih metala eliminiraju se maskiranjem.
16. Određivanje reakcijom s EDTA. EDTA se koristi kao titrant u bezindikatorskim i indikatorskim fotometrijskim titracijama (PT). Kao i kod vizualne titrimetrije, pouzdani FT s otopinama EDTA moguć je pri pH > 3 i koncentraciji titranta od najmanje 10-5 M.
Luminescentna analiza
1. Određivanje Pb organskim reagensima
Predložena je metoda u kojoj se intenzitet kemiluminiscencijske emisije mjeri u prisutnosti Pb uslijed katalitičke oksidacije luminola s vodikovim peroksidom. Metoda je korištena za određivanje od 0,02 do 2 μg Pb u 1 ml vode s točnošću od 10%. Analiza traje 20 minuta i ne zahtijeva prethodnu pripremu uzorka. Osim Pb, reakciju oksidacije luminola kataliziraju tragovi bakra. Metoda, koja je mnogo složenija u svom hardverskom dizajnu, temelji se na korištenju efekta gašenja fluorescencije derivata fluores-132 i vrijedna je u stvaranju kelata s olovom. Selektivnija u prisutnosti mnogih geokemijskih satelita Pb, iako manje osjetljiva, prilično je jednostavna metoda koja se temelji na povećanju intenziteta fluorescencije vodenoplavog lumogena u mješavini dioksana i vode (1:1) u prisutnosti Pb.
2. Metode niskotemperaturne luminiscencije u smrznutim otopinama. Zamrzavanje otopine najlakše se rješava u metodi za određivanje olova u HC1, koja se temelji na fotoelektričnom snimanju zelene fluorescencije kloridnih kompleksa na -70°C.
3. Analiza izboja luminiscencije tijekom odmrzavanja uzoraka. Metode ove skupine temelje se na pomaku spektra luminiscencije pri odmrzavanju analiziranog uzorka i mjerenju uočenog povećanja intenziteta zračenja. Maksimalna valna duljina spektra luminescencije pri -196 i -70°C je 385 odnosno 490 nm.
4. Predložena je metoda koja se temelji na mjerenju analitičkog signala na 365 nm u kvazilinijskim spektru luminescencije CaO-Pb kristalnog fosfora ohlađenog na temperaturu tekućeg dušika. Ovo je najosjetljivija od svih luminescentnih metoda: ako se aktivator nanese na površinu tableta (150 mg CaO, promjer 10 mm, pritisak prešanja 7-8 MN/m2), tada je granica detekcije na spektrografu ISP-51 0,00002 μg. Metoda se odlikuje dobrom selektivnošću: 100-struki višak Co, Cr(III), Fe (III), Mn(II), Ni, Sb (III) i T1 (I) ne ometa određivanje Pb . Bi se također može odrediti istovremeno s Pb.
5. Određivanje olova luminiscencijom kloridnog kompleksa sorbiranog na papiru. U ovoj se metodi kombinira luminiscentna analiza s odvajanjem Pb od interferirajućih elemenata pomoću prstenaste kupke. Određivanje se provodi na uobičajenoj temperaturi.
Elektrokemijske metode
1. Potenciometrijske metode. Koristi se izravno i neizravno određivanje olova - titracija acidobaznim, kompleksometrijskim i taložnim reagensima.
2. Elektrogravimetrijske metode koriste taloženje olova na elektrodama, nakon čega slijedi vaganje ili otapanje.
3. Kulometrija i kulometrijska titracija. Kao titranti koriste se elektrogenerirani sulfhidrilni reagensi.
4. Volt-amperometrija. Klasična polarografija, koja kombinira brzinu s prilično visokom osjetljivošću, smatra se jednom od najprikladnijih metoda za određivanje Pb u rasponu koncentracija od 10-s-10 M. U velikoj većini radova olovo se određuje redukcijskom strujom Pb2+ do Pb° na živinoj kapajućoj elektrodi (DRE), obično se javlja reverzibilno i u difuzijskom načinu. U pravilu su katodni valovi dobro izraženi, a polarografski maksimumi se posebno lako suzbijaju želatinom i Tritonom X-100.
5. Amperometrijska titracija
Kod amperometrijske titracije (AT) točka ekvivalencije određena je ovisnošću trenutne vrijednosti elektrokemijske transformacije Pb i (ili) titranta pri određenoj vrijednosti potencijala elektrode o volumenu titranta. Amperometrijska titracija točnija je od konvencionalne polarografske metode, ne zahtijeva obaveznu kontrolu temperature ćelije i manje ovisi o karakteristikama kapilare i indiferentnog elektrolita. Treba napomenuti da AT metoda ima veliki potencijal, jer je analiza moguća pomoću elektrokemijske reakcije koja uključuje i sam Pb i titrant. Iako je ukupno vrijeme utrošeno na izvođenje AT veće, to se u potpunosti nadoknađuje činjenicom da nema potrebe za kalibracijom. Titracija se koristi s otopinama kalijevog dikromata, kloranilne kiseline, 3,5-dimetildimerkapto-tiopirona, 1,5-6 is (benziliden)-tio-karbohidrazona, tiosalicilamida.
Fizikalne metode određivanja olova
Olovo se određuje atomskom emisijskom spektroskopijom, atomskom fluorescentnom spektrometrijom, atomskom apsorpcijskom spektrometrijom, rendgenskim metodama, radiometrijskim metodama, radiokemijskim i mnogim drugim.
Stranice:
UDK 543.(162:543 42:546.815
NJU. Kostenko, M.G. Christiaisen, E.N. Butenko
FOTOMETRIJSKO ODREĐIVANJE MIKRO KOLIČINA OLOVA U VODI ZA PIĆE POMOĆU SULFONAZE III
Proučavano je kompleksiranje Pb(P) sa sulfonazom III i na temelju dobivenih podataka razvijena je metoda za fotometrijsko određivanje olova u vodi za piće nakon prethodnog ekstrakcijskog koncentriranja u obliku kompleksa s diti:unom.
Problem ekološke čistoće sirovina ima veliki značaj za proizvodnju prehrambenih proizvoda. Stoga je kontrola kvalitete vode za piće, kao jednog od glavnih sastojaka raznih pića, vrlo važna, a stvaranje novih selektivnih, osjetljivih i brzih metoda za fotometrijsko određivanje toksičnih metala vrlo je važno. Među posljednjima, jedan od najopasnijih za ljudsko zdravlje je olovo. Vrijednost njegove najveće dopuštene koncentracije u raznim namirnicama je 0,1 - 10 mg/kg, au vodi za piće 0,03 mg/dm3.
Za fotometrijsko određivanje olova predložen je velik broj organskih reagensa. Glavne karakteristike metoda dane su u tablici.J.Ove metode uglavnom nisu dovoljno selektivne. Stoga standardna metoda određivanja olova u vodi za piće uključuje njegovu prethodnu ekstrakciju u obliku kompleksa s ditizonom. Zatim se tijekom ekstrakcije trakom dodaje sulfarsazen i mjeri se optička gustoća kompleksaPb(II) s ovim reagensom,
Reagens bis-sulfon ili sulfonazo III (SFAZ.HSR)koristi se za određivanje malih količina galija, skandijuma, indija i barija - / .
Molarni omjerPb(II) - SFAZ u kompleksu (jednak 1:1) potvrđuje konstantnost vrijednosti konstante K pod različitim uvjetima za njezino određivanje (tablica 2).
Složene vrijednosti koncentracije potrebne za izračunePbH2R:u uvjetima ravnoteže određena je jednadžbom
= (A-ekCr-0 / (êk - eR)■ ja,
Gdje }