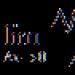органична химия молекулна изология
Вече е общоприето, че една права линия, свързваща два атома, означава една двуелектронна връзка (проста връзка), образуването на която отнема една валентност от всеки от свързаните атоми, две линии - една четириелектронна връзка (двойна връзка), три линии - една шестелектронна връзка (тройна връзка).
Изображението на съединение с известен ред на връзките между всички атоми, използващи връзки от този тип, се нарича структурна формула:
За спестяване на време и място често се използват съкратени формули, в които някои от връзките се подразбират, но не се изписват:
Понякога, особено в карбоцикличните и хетероцикличните серии, формулите се опростяват още повече: не само някои връзки не се изписват, но и някои от въглеродните и водородните атоми не се изобразяват, а само се подразбират (в пресечните точки на линиите); опростени формули:
Тетраедричен модел на въглеродния атом
Основните идеи за химическата структура, заложени от А. М. Бутлеров, бяха допълнени от Van't Hoff и Le Bel (1874), които развиха идеята за пространственото разположение на атомите в органична молекула и повдигнаха въпроса за пространствената конфигурация. и конформация на молекулите. Трудът на Вант Хоф "Химия в космоса" (1874) бележи началото на плодотворно направление в органичната химия - стереохимия, тоест изследване на пространствената структура.
Ориз. 1 - Модели на Van't Hoff: метан (a), етан (b), етилен (c) и ацетилен (d)
Вант Хоф предлага тетраедричен модел на въглеродния атом. Според тази теория четирите валенции на въглеродния атом в метана са насочени към четирите ъгъла на тетраедъра, в центъра на който е въглероден атом, а във върховете са водородни атоми (a). Етанът, според van't Hoff, може да си представим като два тетраедъра, свързани с върхове и свободно въртящи се около обща ос (6). Моделът на молекулата на етилена се състои от два тетраедъра, свързани с ръбове (c), а молекулите с тройна връзка са представени чрез модел, в който тетраедрите са в контакт с равнини (d).
Модели от този тип се оказаха много успешни и за сложни молекули. Те все още се използват успешно днес за обяснение на редица стереохимични въпроси. Теорията, предложена от van't Hoff, въпреки че е приложима в почти всички случаи, обаче не дава обосновано обяснение на вида и природата на свързващите сили в молекулите.
Иновативен начин за разработване на технологии за създаване на нови лекарства
Първо се създава компютърен модел на обекта и компютърното моделиране се използва за формиране на молекули на мястото на изследването. Моделът може да бъде 2D или 3D.
Инфрачервени спектри на молекули
За разлика от видимите и ултравиолетовите диапазони, които се дължат главно на преходите на електрони от едно стационарно състояние в друго ...
Изследване на структурата на органичните съединения с помощта физични методи
Всички възможни позиции на молекулите в триизмерното пространство се свеждат до транслационно, ротационно и осцилаторно движение. Молекула, състояща се от N атома, има само 3N степени на свобода на движение...
Симулационен метод в химията
В момента можете да намерите много различни дефиниции на понятията "модел" и "моделиране". Нека разгледаме някои от тях. „Моделът се разбира като показване на факти, неща и отношения от определена област на знанието под формата на по-проста ...
Научни основиреология
Състоянието на напрежение и деформация на тялото обикновено е триизмерно и е нереалистично да се опишат свойствата му с прости модели. Но в онези редки случаи, когато едноосните тела се деформират...
В допълнение към наблюдението и експеримента в познаването на природния свят и химията голяма роляигра на симулация. Една от основните цели на наблюдението е да се търсят закономерности в резултатите от експериментите...
Разтваряне на твърди вещества
За по-голямата част от процесите кинетичната функция е инвариантна по отношение на концентрацията на активния реагент и температурата. С други думи, всяка стойност на безразмерното време x съответства на добре дефинирана стойност...
Изчисляване на квантово-химични параметри на PAS и определяне на зависимостта "структура-активност" на примера на сулфонамиди
Рефрактометричен метод за анализ в химията
Синтез и анализ на CTS в производството на бензин
Химичен моделпроцесът на каталитичен крекинг има много сложен изглед. Помислете за най-простата от реакциите, протичащи по време на процеса на крекинг: СnН2n+2 > CmH2m+2 + CpH2p...
Синтез на химико-технологична система (ХТС)
Производствените процеси са разнообразни по своите характеристики и степен на сложност. Ако процесът е сложен и дешифрирането на механизма му изисква много усилия и време, се използва емпиричен подход. Математически модели...
Сравнение на плунжерния поток и реакторите с пълно смесване при изотермична работа
7.1. Фигурата показва експеримент, показващ, че телата се разширяват при нагряване. Оградете с химикал на фигурата предмета, който е бил нагрят в този опит - топка или пръстен. Обосновете отговора.
7.2. Изберете правилното твърдение.
Според модерни идеи, когато колбата с вода изстине, нивото на водата в тръбата спада, защото ... . 
7.3. Веществата са изградени от малки частици. Какви явления и експерименти потвърждават това?
7.4. Таблицата показва точните данни за промяната на обема на водата V от времето t при нагряване.
Отговори на въпросите.
а) Може ли да се твърди, че през цялото време на наблюдение водата в колбата се е нагрявала равномерно? Обяснете отговора.
б) Как се променя обемът на водата при нагряване?

8.1. Изберете правилното твърдение.
Ако нагреете нокътя, той се удължава и става по-дебел. Това се случва, защото при нагряване ... . 
8.2. Напишете думите молекула, капка, атом в такъв ред, че всеки следващ елемент да е част от предишния.
8.3. Фигурата показва модели на молекули вода, кислород и въглероден диоксид. Всички молекули съдържат кислороден атом (черен). Попълнете празнините в текста.

8.4. Измерете дължината на ръката си от лакътя до малкия пръст и сравнете получената стойност с размера на водната молекула.
9.1. Попълнете празнините в текста. „През ____ английският ботаник Робърт Браун, изследвайки през микроскоп ...“

9.2. Фигурата показва схематично молекулите на течност, заобикалящи зърно боя, поставено в тази течност. Стрелките показват посоките на движение на молекулите на течността в определен момент от време.

9.3. Обърнете внимание на тези явления, които са пример за Брауново движение.
9.4. Фигурата показва прекъсната линия, по която прашинка се движеше във въздуха за няколко секунди.

а) Обяснете защо прашинката променя посоката си на движение много пъти през времето, в което е наблюдавана.
Поради сблъсък с молекули на въздуха и други прахови частици.
б) На фигурата отбележете точките, в които праховите частици са засегнати от заобикалящите ги молекули.
10.1. В стъклен цилиндър отгоре се налива чиста вода, а в дъното през тясна тръба се излива разтвор на меден сулфат. Цилиндърът е в покой постоянна температура. Покажете на снимката как ще изглежда съдържанието на цилиндъра на различни интервали от време.

10.2. Две еднакви гумено топчесвързани с прозрачен маркуч (вижте фиг.), а лявата топка и в двата случая е пълна с водород (оцветете водорода в синьо), дясната е празна на фигура a и пълна с въздух на фигура b (оцветете въздуха в зелено). Маркучът между топките е захванат със скоба.

10.3. Задраскайте една от маркираните думи, за да получите правилното обяснение на описания експеримент.

10.4. Домашен експеримент.
Поставете на дъното на чаша студена водакубче захар, но не разбърквайте. Запишете колко време ви отне да откриете наличието на захарни молекули на повърхността на водата в чашата и какъв вид "устройство" сте използвали.
11.1. Попълнете пропуските в текста, като използвате думите: по-силен; по-слаб; атракция; отблъскване.

11.2. Начертайте линии, за да свържете явленията и техните обяснения.

11.3. Задраскайте една от маркираните думи, за да получите правилното обяснение на описания експеримент.

11.4. Довършете изречението, за да получите правилното обяснение на явлението.
11.5. Попълнете празнините в текста. „В ежедневието често се сблъскваме с явленията на намокряне и ненамокряне.“

12.1. Какво състояние на материята се характеризира със следните характеристики?
Днес ще проведем урок не само по моделиране, но и по химия и ще направим модели на молекули от пластилин. Пластилиновите топки могат да бъдат представени като атоми, а обикновените кибрит или клечки за зъби ще ви помогнат да покажете структурни връзки. Този метод може да се използва от учители при обяснение на нов материал по химия, родители - при проверка и изучаване домашна работаи самите деца, които се интересуват от темата. Вероятно няма по-лесен и достъпен начин за създаване на визуален материал за мисловна визуализация на микрообекти.
Представители на света на органичните и неорганична химиякато пример. По аналогия с тях могат да бъдат реализирани други структури, основното е да се разбере цялото това разнообразие.
Материали за работа:
- пластилин от два или повече цвята;
- структурни формули на молекули от учебника (при необходимост);
- кибрит или клечки за зъби.
1. Подгответе пластелин за извайване на сферични атоми, които ще образуват молекули, както и кибрит - за представяне на връзките между тях. Естествено, по-добре е атомите от различни видове да се показват в различен цвят, така че да е по-ясно да си представите конкретен обект от микросвета.
2. За да направите топки, отщипете необходимия брой порции пластилин, омесете в ръцете си и разточете фигурите в дланите си. За скулптуриране на органични въглеводородни молекули можете да използвате по-големи червени топки - това ще бъде въглерод, а по-малките сини - водород.

3. За да оформите молекула метан, поставете четири кибрита в червената топка, така че да са насочени към върховете на тетраедъра.

4. Поставете сини топки върху свободните краища на клечките. Молекулата на природния газ е готова.

5. Подгответе две еднакви молекули, за да обясните на детето как да получи молекулата на следващия представител на въглеводородите - етан.

6. Свържете двата модела, като премахнете един кибрит и две сини топки. Итън е готов.

7. След това продължете вълнуващия урок и обяснете как възниква образуването на множествена връзка. Отстранете двете сини топки и удвоете връзката между въглеродните атоми. По подобен начин можете да заслепите всички въглеводородни молекули, необходими за заемане.

8. Същият метод е подходящ за скулптуриране на молекулите на неорганичния свят. Същите топки от пластилин ще помогнат за изпълнението на плана.

9. Вземете централния въглероден атом - червената топка. Поставете две клечки в нея, като зададете линейната форма на молекулата, прикрепете две сини топки към свободните краища на клечките, които в този случай представляват кислородни атоми. Така имаме линейна молекула въглероден диоксид.

10. Водата е полярна течност, а нейните молекули са ъглови образувания. Те са съставени от един кислороден атом и два водородни атома. Ъгловата структура се определя от несподелената двойка електрони на централния атом. Може да се изобрази и като две зелени точки.

Те са толкова завладяващи творчески уроцитрябва да се практикува с деца. Учениците на всяка възраст ще се заинтересуват от химията, ще разберат по-добре темата, ако в процеса на обучение им бъде предоставена визуална помощ, направена от собствените им ръце.

Органична химия.
2.1 Тема: " Теория на структурата на органичните съединения "
2.1.1. Основните положения на теорията за структурата на органичните съединения и класификацията на органичните съединения.
1. Естествени и синтетични органична материя. Малко от историята на органичната химия. Общи свойства на органичните вещества (състав, тип химична връзка, кристална структура, разтворимост, отношение към нагряване в присъствието на кислород и без него).
2. Теория на структурата на органичните съединения от А. М. Бутлеров. Развитие на теорията и нейното значение.
3. Класификация на органичните вещества.
Органичните вещества получиха името си, защото първите от изследваните вещества от тази група бяха част от живите организми. Повечето от известните в момента органични вещества не се срещат в живите организми, те се получават (синтезират) в лаборатория. Следователно се разграничават естествени (естествени) органични вещества (въпреки че повечето от тях вече могат да бъдат получени в лабораторията), а органичните вещества, които не съществуват в природата, са синтетични органични вещества. Тези. наименованието "органични вещества" е историческо и няма специално значение. Всички органични съединения са съединения на въглерода. Органичните вещества включват въглеродни съединения, с изключение на тези, изучавани в курса на неорганичната химия прости веществаобразувани от въглерод, неговите оксиди, въглеродна киселина и нейните соли. С други думи: органичната химия е химията на въглеродните съединения.
Разказразвитие на органичната химия:
Берцелиус, 1827 г., първият учебник по органична химия. Виталисти. Учението за "жизнената сила".
Първите органични синтези. Wehler, 1824, синтез на оксалова киселина и урея. Kolbe, 1845, оцетна киселина. Бертло, 1845 г., дебел. Бутлеров, 1861 г., захарно вещество.
Но като наука органичната химия започва със създаването на теория за структурата на органичните съединения. Значителен принос за него имат немският учен Ф. А. Кекуле и шотландецът А. С. Купър. Но решаващият принос несъмнено принадлежи на руския химик А. М. Бутлеров.
Сред всички елементи въглеродът се отличава със способността си да образува стабилни съединения, в които неговите атоми са свързани помежду си в дълги вериги с различни конфигурации (линейни, разклонени, затворени). Причината за тази способност: приблизително същата енергия на връзката на C-C и C-O (за други елементи енергията на втория е много по-висока). В допълнение, въглеродният атом може да бъде в един от трите вида хибридизация, образувайки съответно единични, двойни или тройни връзки не само помежду си, но и с кислородни или азотни атоми. Вярно е, че много по-често (почти винаги) въглеродните атоми са свързани с водородни атоми. Ако едно органично съединение съдържа само въглерод и водород, тогава съединенията се наричат въглеводороди. Всички други съединения могат да се разглеждат като производни на въглеводороди, в които някои водородни атоми са заменени с други атоми или групи от атоми. Така че по-точно определение е: Органичните съединения са въглеводороди и техните производни.
Има много органични съединения - повече от 10 милиона (неорганични около 500 хиляди). Съставът, структурата и свойствата на всички органични вещества имат много общо.
Органичните вещества имат ограничен качествен състав. Задължително C и H, често O или N, по-рядко халогени, фосфор, сяра. Други елементи се включват много рядко. Но броят на атомите в една молекула може да достигне милиони и молекулна масаможе да е много голям.
Структурата на органичните съединения.защото състав - неметали. => химическа връзка: ковалентен. Неполярни и полярни. Йонните са много редки. => Най-често кристалната решетка молекулярно.
са често срещани физични свойства : ниска точка на кипене и топене. Сред органичните вещества има газове, течности и топими твърди вещества. Често е летлив, може да има миризма. Обикновено безцветен. Повечето органични вещества са неразтворими във вода.
са често срещани Химични свойства :
1) при нагряване без достъп на въздух всички органични вещества се „овъгляват“, т.е. в този случай се образуват въглища (по-точно сажди) и някои други неорганични вещества. Има разкъсване на ковалентни връзки, първо полярни, след това неполярни.
2) При нагряване в присъствието на кислород всички органични вещества лесно се окисляват, а крайните продукти на окислението са въглероден диоксид и вода.
Характеристики на хода на органичните реакции.Молекулите участват в органични реакции, по време на реакцията трябва да се разкъсат някои ковалентни връзки и да се образуват други. Следователно химичните реакции с участието на органични съединения обикновено са много бавни, за осъществяването им е необходимо да се използват повишени температура, налягане и катализатори.Неорганичните реакции обикновено включват йони, реакциите протичат много бързо, понякога мигновено, при нормална температура. Органичните реакции рядко водят до високи добиви (обикновено под 50%). Те често са обратими, освен това могат да възникнат не една, а няколко реакции, които се конкурират помежду си, което означава, че реакционните продукти ще бъдат смес от различни съединения. Следователно формата на записване на органичните реакции също е малко по-различна. Тези. не използвайте химични уравнения, и схемите химична реакция, в които няма коефициенти, но условията на реакцията са посочени подробно. Също така е обичайно да се записват имената на организациите под уравнението. вещества и вид реакция.
Но като цяло органичните вещества и реакции се подчиняват общи законихимия, а органичните вещества се превръщат в неорганични или могат да се образуват от неорганични. Което още веднъж подчертава единството на света около нас.
Основни положения на теорията химическа структураизложено от младия А. М. Бутлеров на Международния конгрес на естествоизпитателите през 1861 г
1). Атомите в молекулите са свързани помежду си в определен ред, в съответствие с тяхната валентност. Последователността на свързващите атоми се нарича химическа структура .
Валентността е способността на атомите да образуват определен брой връзки (ковалентни). Валентността зависи от броя на несдвоените електрони в атома на елемента, тъй като ковалентните връзки се образуват поради общи електронни двойки, когато електроните са сдвоени. Въглеродът във всички органични вещества е четиривалентен. Водород - 1, Кислород - P, азот - W, сяра - P, хлор - 1.
Методи за изобразяване на органични молекули.
Молекулярна формула - условно изображениесъстава на веществото. H 2 CO 3 - въглена киселина, C 12 H 22 O 11 - захароза. Такива формули са удобни за изчисления. Но те не дават информация за структурата и свойствата на материята. Следователно дори молекулните формули в органичните вещества са написани по специален начин: CH 3 OH. Но много по-често те използват структурни формули. Структурната формула отразява реда на свързване на атомите в молекулата (т.е. химичната структура).А в основата на всяка органична молекула лежи Въглеродният скелет е верига от взаимосвързани ковалентни връзкивъглеродни атоми.
Електронни формулимолекули - връзките между атомите са показани като двойки електрони.
Пълната структурна формула е показана с тирета, показващи всички връзки. Химическа връзка, образувана от една двойка електрони, се нарича единична връзка и е представена с едно тире в структурната формула. Двойна връзка (=) се образува от две двойки електрони. Тройната (≡) се образува от три двойки електрони. И общият брой на тези връзки трябва да съответства на валентността на елемента.
 В кондензирана структурна формула тиретата на единичните връзки се пропускат и атомите, свързани с определен въглероден атом, се записват непосредствено след него (понякога в скоби).
В кондензирана структурна формула тиретата на единичните връзки се пропускат и атомите, свързани с определен въглероден атом, се записват непосредствено след него (понякога в скоби).
Скелетните формули са още по-съкратени. Но те се използват по-рядко. Например:

Структурните формули отразяват само реда на свързване на атомите. Но молекулите на органичните съединения рядко имат равнинна структура. Обемното изображение на молекулата е важно за разбирането на много химични реакции. Образът на молекула се описва с помощта на понятия като дължина на връзката и ъгъл на връзката. Освен това е възможно свободно въртене около единични облигации. Визуално представяне се осигурява от молекулярни модели.
GBPOU NSO "Коливански аграрен колеж"
Инструкционна технологична карта №1
според ОУД. единадесет Химия
професии 35.01.23 Господарка (в) на имението, 19.01.04 Бейкър
Раздел 1: Органична химия
Тема 1.1: Основни понятия на органичната химия и теорията за структурата на органичните съединения.
Длъжност : Изработване на модели на молекули - представители на различни класове органични съединения.
Цел на работата:
обобщават и систематизират знанията на учениците за теорията на структурата на органичните съединения;
консолидират способността за съставяне на структурни формули на въглеводороди;
Ученикът трябва да постигне следните резултати:
лично:
− чувство на гордост и уважение към историята и постиженията на родната химическа наука; химически компетентно поведение в професионална дейности в ежедневието при работа с химикали, материали и процеси;
− готовност за продължаване на образованието и повишаване на квалификацията в избраната професионална дейност и обективно осъзнаване на ролята на химическите компетенции в това;
− способността да се използват постиженията на съвременната химическа наука и химични технологииза подобряване на собственото интелектуално развитиев избраната професионална дейност;
метасубект:
− използването на различни видове когнитивна дейност и основни интелектуални операции (поставяне на проблеми, формулиране на хипотези, анализ и синтез, сравнение, обобщение, систематизиране, идентифициране на причинно-следствени връзки, търсене на аналози, формулиране на заключения) за решаване на проблем, използването на основни методи на познание (наблюдение, научен експеримент) за изучаване на различни аспекти на химически обекти и процеси, които трябва да се срещнат в професионално направление;
− използването на различни източници за получаване на химическа информация, способността да се оцени нейната надеждност с цел постигане на добри резултати в професионалната област;
предмет :
− формирането на идеи за мястото на химията в съвременната научна картина на света;
Разбиране на ролята на химията за формиране на хоризонта и функционална грамотност на човек за решаване на практически проблеми;
− владеене на фундаментални химични понятия, теории, закони и закономерности;
Уверено използване на химическа терминология и символи;
− владеене на основните методи на научно познание, използвани в химията: наблюдение, описание, измерване, експеримент;
Способност за обработка, обяснение на резултатите от експерименти и извеждане на изводи;
− желание и способност за прилагане на методи на познанието при решаване на практически проблеми;
− формирането на способността да се дават количествени оценки и да се правят изчисления според химични формулии уравнения;
− познаване на правилата за безопасност при използване химически вещества;
− формирането на собствена позиция по отношение на химическата информация, получена от различни източници.
Форма на обучение : индивидуален
Времева норма: 2 часа
Оборудване на работното място : Набор от модели на молекули с топка и пръчка, таблица „Ограничени въглеводороди“, периодична таблица, диаграми с инструкции, тетрадки
Литература:
Средства за обучение: вербален (вербален), визуален
Мерки за безопасност: са запознати с правилата за безопасност на работното място и в офиса.
Въглеводородите са органични съединения, съставени от въглеродни и водородни атоми. Въглеродният атом във всички органични съединениячетиривалентен. Въглеродните атоми могат да образуват прави, разклонени, затворени вериги. Свойствата на веществата зависят не само от качествения и количествения състав, но и от реда, в който атомите са свързани помежду си. Вещества, които имат еднаква молекулна формула, но различни структури, се наричат изомери. Префиксите показват суматади - две,три - три,тетра - четири;цикло - означава затворен.
Суфиксите в името на въглеводородите показват наличието на множествена връзка:
en
единична връзка между въглеродните атоми(C - C);
en
двойна връзка между въглеродните атоми(С=С);
в
тройна връзка между въглеродните атоми(СЪС
=
СЪС);
диен
две двойни връзки между въглеродни атоми(C \u003d C - C \u003d C);
радикали:метил-СН 3 ; етил-С 2 з 5 ; хлор-Cl; бром -Br.
Пример. Направете модел на молекулата на пропана.
молекула пропан° С 3 з 8 съдържа три въглеродни атома и осем водородни атома. Въглеродните атоми са свързани един с друг. Наставка– en показва наличието на единична връзка между въглеродните атоми. Въглеродните атоми са подредени под ъгъл от 109 28 минути.
Молекулата има формата на пирамида. Начертайте въглеродните атоми като черни кръгове, водородните атоми като бели кръгове и хлорните атоми като зелени кръгове.
Когато изобразявате модели, спазвайте съотношението на размерите на атомите.
моларна масанамерете с помощта на периодичната таблица
Г-ЦА 3 з 8 ) = 12 3 + 1 8 = 44 g/mol.
За да назовете въглеводород, трябва:
Изберете най-дългата верига.
Число, започващо от ръба, който е най-близък до радикалната или множествената връзка.
Посочете радикала, ако указват няколко радикала. (номер преди заглавието).
Назовете радикала, като започнете с най-малкия радикал.
Назовете най-дългата верига.
Посочете позицията на кратната връзка. (Числото след името).
Пример

Когато компилирате формули по име, трябва:
Определете броя на въглеродните атоми във веригата.
Определете позицията на кратната връзка. (Числото след името).
Определете позицията на радикалите. (номер преди заглавието).
Запишете формулите на радикалите.
Накрая определете броя и подредете водородните атоми.
Работен ред
Задача номер 1 . Направете модели на молекули:
1) редица алкани: метан, етан, бутан, пентан, хексан, хептан, октан, нонан и декан;
2) Циклоалкани: циклопропан,циклопен
3) 2-метилпропан,
4) 1,2-дихлороетан.
Скицирайте молекулярните модели в тетрадката си. Напишете структурните формули на тези вещества. Намерете техните молекулни тегла.
Задача номер 2. Наименувайте веществата:

Задача номер 3. Съставете структурен формули на веществата:
а) бутен-2, напишете неговия изомер;
б) 3,3-диметилпентин-1.
име обща формуланаситени въглеводороди.
Кои вещества се наричат хомолози, кои изомери?
Лектор: Рачковская А.И.